-
下列与化学反应能量变化相关的叙述正确的是
A.生成物能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
难度: 简单查看答案及解析
-
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH
CH3COO-+H+对于该平衡,下列叙述正确的是
A.加入少量NaOH固体,平衡向逆反应方向移动
B.升高温度,平衡向正反应方向移动
C.加入水稀释,溶液中c(H+)一定增大
D.加入少量CH3COONa固体,平衡向正反应方向移动
难度: 简单查看答案及解析
-
对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A、υ(W)=3υ(Z) B、2υ(X)=3υ(Z) C、2υ(X)=υ(Y) D、3υ(W)=2υ(X)
难度: 简单查看答案及解析
-
在298K、100kPa时,已知:2H2O(g)=O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)=2HCl(g) ΔH2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) ΔH3
则⊿H3与⊿H1和⊿H2间的关系正确的是
A、⊿H3=⊿H1+2⊿H2 B、⊿H3=⊿H1+⊿H2
C、⊿H3=⊿H1-2⊿H2 D、⊿H3=⊿H1-⊿H2
难度: 简单查看答案及解析
-
下列说法不正确的是
A.在化学反应进行的过程中放出或吸收的热量称为反应热。
B.在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热。
C.对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量。
D.在101Kpa时,1mol物质完全燃烧生成稳定氧化物时,所放出的热量叫做该物质的燃烧热。
难度: 简单查看答案及解析
-
下列溶液一定呈碱性的是
A.溶液中c(OH-)>c(H+) B.溶液中含有OH‑离子
C.滴加甲基橙后溶液显红色 D.滴加甲基橙后溶液显黄色
难度: 简单查看答案及解析
-
已知H2 (g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为
A.-44.2kJ·mol-1 B.+44.2kJ·mlo-1 C.-330kJ·mol-1 D.+330kJ·mlo-1
难度: 简单查看答案及解析
-
在一定温度下体积固定的密闭容器中,当下列物理量:
①混合气体的压强 ② 气体的总物质的量 ③混合气体的密度④B的物质的量浓度
不再变化时,能表明可逆反应A(s)+2B(g)
C(g)+D(g)已达平衡的是
A.①② B. ③④ C. ①④ D. 只有④
难度: 简单查看答案及解析
-
已知H2(g)+Br2(l)=2HBr(g);△H=-72KJ/mol,蒸发1molBr2(l)需要吸收的能量为30KJ,其他的相关数据如下表:
H2(g)
Br2(g)
HBr(g)
1mol分子中的化学键断裂时需要吸收的能量/kJ
436
a
369
则表中a为
A.404 B. 260 C.230 D.200
难度: 简单查看答案及解析
-
已知:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) △H=74.9 kJ·mol-1,下列说法中正确的是
A.该反应中熵变、焓变皆大于0
B.该反应是吸热反应,因此一定不能自发进行
C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
难度: 简单查看答案及解析
-
用水稀释0.1mol/L醋酸溶液时,溶液中随着水量的增加而减小的是
A.c(H+)/c(CH3COOH) B.c(CH3COOH)/c(H+)
C.c(H+)和c(OH-)的乘积 D.H+的物质的量
难度: 简单查看答案及解析
-
硫代硫酸钠溶液与稀硫酸反应的化学方程式为: Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
实验
反应温度/℃
Na2S2O3溶液
稀H2SO4
H2O
V/mL
c/(mol·L-1)
V/mL
c/(mol·L-1)
V/mL
A
25
5
0.1
10
0.1
5
B
25
5
0.2
5
0.2
10
C
35
5
0.1
10
0.1
5
D
35
5
0.2
5
0.2
10
难度: 简单查看答案及解析
-
已知:101kPa时的辛烷的燃烧热为5518kJ·mol-1,强酸与强碱在稀溶液中发生反应时的
中和热57.3kJ·mol-1,则下列热化学方程式书写正确的是
①C8H18(l)+ 25/2 O2(g)=8CO2(g)+9H2O(l);△H=+5518kJ·mol-1
②C8H18(l)+ 25/2 O2(g)=8CO2(g)+9H2O(l);△H=-5518kJ·mol-1
③H++OH-=H2O;△H=-57.3kJ·mol-1
④NaOH(aq)+1/2 H2SO4(aq)= 1/2 Na2SO4(aq)+H2O(l);△H=+57.3kJ·mol-1
A.①③ B.②③ C.②④ D.只有②
难度: 简单查看答案及解析
-
I2在KI溶液中存在下列平衡:I2(aq)+I-
I3-(aq)。测得不同温度下该反应的平衡常数K如下表:
t/℃
5
15
25
35
50
K
1100
841
680
533
409
下列说法正确的是
A.反应I2(aq)+I-
I3-(aq)的ΔH>0
B.其他条件不变,升高温度,溶液中c(I3-)减小
C.该反应的平衡常数表达式是K=c(I2)·c(I-)/c(I3-)
D.25℃时,向溶液中加入少量KI固体,平衡常数K小于680
难度: 简单查看答案及解析
-
常温下,pH=2的NaOH溶液与pH=1的HC1溶液按一定比例混合,所得溶液pH=2,则NaOH溶液与HC1溶液的体积比为
A.9:2 B.2:9 C.1:9 D.10:1
难度: 简单查看答案及解析
-
一定条件下,可逆反应:X(g) + 3Y(g)
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3 (均不为零),反应达到平衡时, X、Y、Z的浓度分别为0.1mol•L-1、0.3 mol•L-1、0.08 mol•L-1.则下列判断不正确的是
A、c1∶c2== 1∶3
B、平衡时,Y和Z生成速率之比为3∶2
C、X、Y的转化率不相等
D、c1的取值范围为0< c1< 0.14 mol•L-1
难度: 简单查看答案及解析
-
下图表示反应N2(g)+3H2(g) == 2NH3 (g);△H﹤0在某一时间段中反应速率与反应过程的曲线关系图。下列说法正确的是
A.氨气的体积分数最高的一段时间为t5—t6
B.t2—t3和t3—t4时间段氨气的体积分数相等
C.t1时刻改变的条件是降低温度
D.t4—t5时间段平衡向正反应方向移动
难度: 简单查看答案及解析
-
某探究小组在某温度下测定溶液的pH时发现:0.01mol·L-1的NaOH溶液中,由水电离出的
c(H+)·c(OH-)=10-22,则该小组在该温度下测得0.1mol·L-1NaOH溶液的pH应为
A.13 B.12 C.11 D.10
难度: 简单查看答案及解析
-
在一定温度下,向容积固定不变的密闭容器中充入a mol NO2,发生如下反应:2NO2(g)
N2O4(g);△H<0。达平衡后再向容器中充入amol NO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是
A.相对平均分子质量增大 B.NO2的转化率提高
C.NO2的质量分数增大 D.反应放出的总热量大于原来的2倍
难度: 简单查看答案及解析
-
20、25℃时,向V mL PH=a的盐酸中,滴加10V mL pH=b的NaOH溶液,所得溶液中Cl—的物质的量恰好等于Na+的物质的量,则a+b的值是
A.15 B.14 C.13 D.不能确定
难度: 简单查看答案及解析
-
CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是________
(2)已知在101kPa时,CO的燃烧热为283kJ/mol。相同条件下,若2 molCH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是________。
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强。
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为
(保留2位小数)。
②若燃烧后气体体积缩小了a/4mL,则a与b关系的数学表达式是________。
难度: 简单查看答案及解析
-
(10分,每空2分)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示。请认真观察右图,然后回答问题。
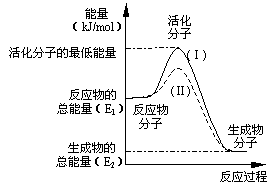
(1)图中所示反应是_________(填“吸热”或“放热”)反应,该反应________(填“需要”或“不需要”)加热,该反应的△H=____________(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+0.5 O2(g)=H2O(g);△H=-241.8 kJ/mol
该反应的活化能为167.2 kJ/mol,则其逆反应的活化能为____________________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(Ⅰ)相比,活化能大大降低,活化分子的百分数增多,反应速率加快,你认为最可能的原因是_________________________。
难度: 简单查看答案及解析
-
(10分,每空2分)在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)
C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
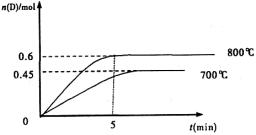
(1)800℃时。0—5min内,以B表示的平均反应速率为________。
(2)能判断该反应达到化学平衡状态的依据是________。
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K=________,该反应为________反应(填吸热或放热)
(4)700℃时,某时刻测得体系中各物质的量如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应________进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
难度: 简单查看答案及解析
-
(12分,每空2分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定过氧化氢的含量。
请填写下列空白:
(1)移取10.00 mL密度为ρg/mL的过氧化氢溶液至250mL ___________(填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。

(3) 滴定时,将高锰酸钾标准溶液注入______________________(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是_________。
(4) 重复滴定三次,平均耗用cmol/L KMnO4标准溶液VmL,则原过氧化氢溶液中过氧化氢的质量分数为______________________________________。
(5) 若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
难度: 简单查看答案及解析