-
有关溴乙烷的下列叙述中,正确的是
A. 在溴乙烷中滴入AgNO3溶液,立即有淡黄色沉淀生成
B. 溴乙烷不溶于水,能溶于大多数有机溶剂
C. 溴乙烷与NaOH的醇溶液反应,可生成乙醇
D. 溴乙烷通常用溴与乙烷直接反应来制取
难度: 中等查看答案及解析
-
如图,a、b是石墨电极,通电一段时间后,b极附近溶液显红色。下列说法正确的是( )
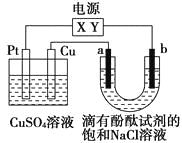
A. X极是电源负极,Y极是电源正极
B. a极的电极反应是2Cl--2e-=Cl2↑
C. 电解过程中CuSO4溶液的pH逐渐增大
D. Pt极上有6.4 g Cu析出时,b极产生2.24 L(标准状况)气体
难度: 中等查看答案及解析
-
25℃时,水的电离达到平衡:H2O
H++OH-;ΔH>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量盐酸,平衡逆向移动,c(OH-)增大
D.将水加热,Kw增大,pH不变,呈中性
难度: 中等查看答案及解析
-
下列叙述正确的是
A. 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B. 25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7
C. 25℃时,0.1 mol·L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱
D. 0.1 mol AgCl和0.1 mol AgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-)
难度: 中等查看答案及解析
-
25 ℃时,有下列四种溶液:
①
②
③
④
0.1 mol·L-1氨水
pH=11氨水
0.1 mol·L-1盐酸
pH=3盐酸
下列说法中正确的是( )
A. ①稀释到原来的100倍后,pH与②相同
B. 等体积①③混合、等体积②④混合所得的溶液都呈酸性
C. ①②中分别加入少量CH3COONa固体,
 的值都变小
的值都变小D. ③④稀释到原来的100倍后,稀释后④溶液中的pH大
难度: 中等查看答案及解析
-
常温下,向10mlbmol·L-1的CH3COOH溶液中滴加等体积的0.01mol·L-1的NaOH溶液,充分反应后溶液中c(CH3COO-)=c(Na+),下列说法不正确的是
A. b>0.01
B. 混合后溶液呈中性
C. CH3COOH的电离常数Ka=
D. 向CH3COOH溶液中滴加NaOH溶液的过程中,水的电离程度逐渐减小
难度: 中等查看答案及解析
-
下列有关氟氯烃的说法中,不正确的是( )
A. 氟氯烃是一种含氟和氯的卤代烃
B. 氟氯烃的化学性质稳定,有毒
C. 氟氯烃大多无色、无臭、无毒
D. 在平流层中,氟氯烃在紫外线照射下,分解产生的氯原子可引发损耗臭氧层的循环反应
难度: 中等查看答案及解析
-
将有机物完全燃烧,生成CO2和H2O。将12 g 该有机物的完全燃烧产物通过浓H2SO4,浓H2SO4增重14.4 g,再通过碱石灰,碱石灰增重26.4 g。则该有机物的分子式为( )
A. C4H10 B. C2H6O
C. C3H8O D. C3H8
难度: 中等查看答案及解析
-
下列有关实验的说法错误的是( )
A. 在蒸馏实验中,温度计的水银球位于支管口处是为了测出馏分的沸点
B. 用结晶法分离硝酸钾和氯化钠的混合物,用分液法分离水和硝基苯的混合物
C. 在重结晶的实验中,使用短颈漏斗趁热过滤是为了减少被提纯物质的损失
D. 作为重结晶实验的溶剂,杂质在此溶液中的溶解度受温度影响应该很大
难度: 中等查看答案及解析
-
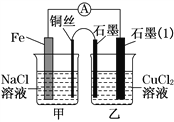
某小组为研究原电池原理,设计如图装置,下列叙述正确的是
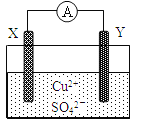
A. 若X为Fe,Y为Cu,铁为正极
B. 若X为Fe,Y为Cu,电子由铜片流向铁片
C. 若X为Fe,Y为C,碳棒上有红色固体析出
D. 若X为Cu,Y为Zn,锌片发生还原反应
难度: 中等查看答案及解析
-
电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下。下列说法不正确的是( )
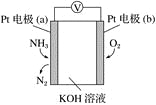
A. O2在电极b上发生还原反应
B. 溶液中OH-向电极a移动
C. 反应消耗的NH3与O2的物质的量之比为4∶5
D. 负极的电极反应式为2NH3-6e-+6OH-===N2+6H2O
难度: 中等查看答案及解析
-
下列有关同分异构体数目的叙述不正确的是( )
A. 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
B. 与
互为同分异构体的芳香族化合物有6种
C. 含有5个碳原子的某饱和链烃,其一氯取代物可能有8种
D. 菲的结构式为
,它与硝酸反应,可生成5种一硝基取代物
难度: 中等查看答案及解析
-
下列现象中,不是因为发生化学反应而产生的是( )
A.乙烯使酸性KMnO4溶液褪色
B.将苯滴入溴水中,振荡后水层接近无色
C.乙烯使溴的四氯化碳溶液褪色
D.甲烷与氯气混合,光照一段时间后黄绿色消失
难度: 中等查看答案及解析
-
某同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4 +8H2O设计如下原电池,盐桥中装有饱和KCl溶液。下列说法正确的是

A. b电极上发生还原反应
B. 外电路电子的流向是从a到b
C. 电池工作时,盐桥中的SO42-移向甲烧杯
D. a电极上发生的反应为:MnO4-+8H++5e- = Mn2++4H2O
难度: 困难查看答案及解析
-
下列事实:
①NaHSO4溶液呈酸性;
②长期使用化肥(NH4)2SO4会使土壤酸性增大,发生板结;
③加热能增加纯碱的去污能力;
④配制 CuCl2 溶液,用稀盐酸溶解CuCl2固体;
⑤NaHS溶液中c(H2S)>c(S2-);
⑥氯化铵溶液可作焊药去除金属制品表面的锈斑;
⑦加热FeCl3·6H2O晶体,往往得不到FeCl3固体。
其中与盐类的水解有关的叙述有( )
A. 7项 B. 6项 C. 5项 D. 4项
难度: 中等查看答案及解析
-
一定温度下,难溶电解质的饱和溶液中存在着沉淀溶解平衡,已知:
物质
Fe(OH)2
Cu(OH)2
Fe(OH)3
Ksp(25 ℃)
8.0×10-16
2.2×10-20
4.0×10-38
25 ℃时,对于含Fe2(SO4)3、FeSO4和CuSO4各0.5 mol的1 L混合溶液,根据上表数据判断,下列说法不正确的是( )
A. 在pH=5的溶液中,Fe3+不能大量存在
B. 混合溶液中c(SO
)∶[c(Fe3+)+c(Fe2+)+c(Cu2+)]>5∶4
C. 向混合溶液中逐滴加入0.1 mol·L-1NaOH溶液,最先看到红褐色沉淀
D. 向混合溶液中加入适量氯水,并调节pH到3~4过滤,可获较纯净的CuSO4溶液
难度: 中等查看答案及解析
-
已知25 ℃时,Ka(HF)=6.0×10-4,Ksp(MgF2)=5.0×10-11。现向1 L 0.2 mol·L-1 HF溶液中加入 1 L 0.2 mol·L-1 MgCl2溶液。下列说法中正确的是( )
A. 25 ℃时,0.1 mol·L-1 HF溶液中pH=1
B. 0.2 mol·L-1 MgCl2溶液中离子浓度关系为2c(Mg2+)=c(Cl-)>c(H+)=c(OH-)
C. 2HF(aq)+Mg2+(aq)
MgF2(s)+2H+(aq),该反应的平衡常数K=1.2×107
D. 该反应体系中有MgF2沉淀生成
难度: 中等查看答案及解析
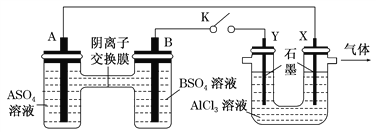
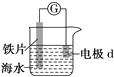
 (NaCl)____________________________________________;
(NaCl)____________________________________________;