-
下列变化中,属于化学变化的是( )
A.干冰升华 B.灯管发亮 C.铁丝弯曲 D.酒精燃烧
难度: 中等查看答案及解析
-
决定元素种类的是( )
A.中子数 B.质子数 C.核外电子数 D.最外层电子数
难度: 中等查看答案及解析
-
下列图标中,表示“禁止烟火”的是( )

A B C D
难度: 简单查看答案及解析
-
保持氢气化学性质的粒子是( )
A.H B. H2O C.2H D.H2
难度: 中等查看答案及解析
-
下列物质中,属于氧化物的是( )
A.MnO2 B.NaCl C.NaOH D.H2SO4
难度: 简单查看答案及解析
-
下列做法中,不利于保护水资源的是( )
A.使用节水型马桶 B.生活污水任意排放
C.合理使用农药和化肥 D.工业废水处理达标后排放
难度: 简单查看答案及解析
-
下列物质中,能用作磷肥的是( )
A.K2SO4 B.CO(NH2)2 C.NH4NO3 D.Ca(H2PO4)2
难度: 简单查看答案及解析
-
有人通过闻茶的方法就能判断出茶的产地。人们能够闻到茶香的原因是( )
A.分子之间有间隔 B.分子在不断运动
C.分子的质量和体积都很小 D.分子是由原子构成的
难度: 简单查看答案及解析
-
下列物质放在敞口容器中一段时间后,质量明显减少的是( )
A.氢氧化钠 B.浓硫酸 C.浓盐酸 D.碳酸钙
难度: 简单查看答案及解析
-
下列物品所使用的主要材料为有机合成材料的是( )

A.纯棉帽子 B.塑料盆 C.不锈钢餐具 D. 玻璃杯
难度: 简单查看答案及解析
-
火星的土壤呈弱碱性。如果火星具备作物生长的条件,则将下列作物带到火星上,能种植成活的是( )
作物
茶树
棉花
水稻
甘草
适宜生长的pH
5.0~5.5
6.0~6.8
6.0~7.0
7.2~8.5
A.茶树 B.棉花 C.水稻 D.甘草
难度: 简单查看答案及解析
-
锰元素的相关信息如图所示。下列说法中正确的是( )
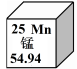
A.属于金属元素 B.核内中子数为25
C.核外电子数为30 D.在地壳中的含量为54.94%
难度: 简单查看答案及解析
-
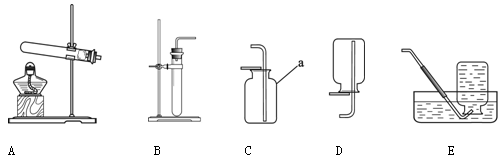
下列实验操作中,不正确的是( )

A.倾倒液体 B.闻气体的气味 C.稀释浓硫酸 D.加热液体
难度: 简单查看答案及解析
-
下列操作中,能鉴别空气、氧气和二氧化碳3瓶气体的是( )
A.观察气体颜色 B.插入燃着的木条
C.闻气体的气味 D.倒入澄清石灰水
难度: 中等查看答案及解析
-
将下列固体分别放入水中,溶液温度明显降低的是( )
A.食盐 B.烧碱 C.生石灰 D.硝酸铵
难度: 中等查看答案及解析
-
下列化学方程式中,书写正确的是( )
A.2P+5O2 点燃P2O5 B.H2SO4 + NaOH
NaSO4 + H2O
C.CO2 + 2NaOH
Na2CO3 + H2O D.2KMnO4 △K2MnO4 + MnO2 + O2
难度: 简单查看答案及解析
-
三氧化铬(CrO3)常用于金属镀铬。工业上用重铬酸钠(Na2Cr2O7)制造三氧化铬,反应的化学方程式为Na2Cr2O7+X
2CrO3+Na2SO4+H2O,其中X的化学式是( )
A.H2S B.SO2 C.H2SO4 D.H2SO3
难度: 中等查看答案及解析
-
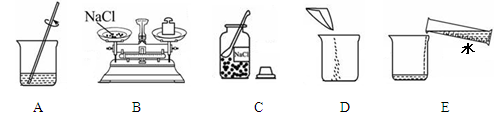
下列实验方案中,不能达到实验目的的是( )
选项
实验目的
实验方案
A
鉴别硬水和软水
加肥皂水搅拌
B
除去氯化钠固体中的少量碳酸钠
加入适量稀盐酸,充分反应后,蒸发
C
分离碳酸钠和氢氧化钠的混合物
加入过量氢氧化钙溶液,过滤
D
探究燃烧的条件之一:温度达到着火点
用导管分别对准浸没在热水和冷水中的白磷通氧气
难度: 困难查看答案及解析
-
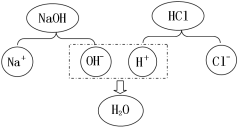
工业上用甲、乙制备化学肥料丙,同时有丁生成。根据下列微观示意图得出的结论中,正确的是( )

①甲的化学式为NH3 ②乙、丙、丁都是氧化物
③丙中氮、氢元素质量比为7:1 ④参加反应的甲、乙质量比为17:44
A.① B.①③ C. ①④ D. ②④
难度: 简单查看答案及解析
-
科学家正在研究如下图所示的循环体系。

从图中分析得出的下列结论正确的是( )
①该技术符合低碳经济的理念 ②该过程所用的催化剂一定是二氧化锰
③该体系有一种可循环利用的物质是氢气 ④该技术有助于缓解全球面临的能源危机
⑤二氧化碳与氢气在复合催化剂条件下反应的产物是混合物
A.①②④ B.①③⑤ C.②③⑤ D.①④⑤
难度: 简单查看答案及解析
-
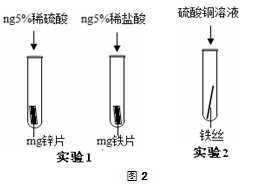
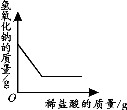
下列四个图像中,能正确反映对应变化关系的是( )
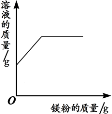
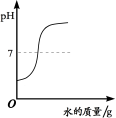
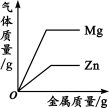
A.向一定量的稀盐酸中加入过量的镁粉
B.向一定量的稀盐
酸中加入足量的水稀释
C.向两份完全相同的稀盐酸中分别加入锌粉、镁粉
D.向一定量氢氧化钠溶液中滴加稀盐酸
难度: 困难查看答案及解析
-
肾病患者需要食用低钠盐的食品。目前,市场供应的低钠盐多为苹果酸钠盐(C4H5O5Na)。每日食用6 g苹果酸钠盐,人体摄入的钠元素质量与等量食盐中钠元素质量之比为( )
A.6:5 B.71:266 C.104:39 D.39:104
难度: 中等查看答案及解析