-
下列物质按酸、碱、盐、有机物、混合物顺序排列的是
A. 硝酸、苛性钠、明矾、四氯化碳、氯水
B. 碳酸氢钠、消石灰、食盐、酒精、合金
C. 醋酸、纯碱、碳酸钙、苯、石油||
D. 硫酸、生石灰、高锰酸钾、甲烷、石油
难度: 中等查看答案及解析
-
下列物质的水溶液能导电而本身不属于电解质的是
A. 乙醇 B. 液态氯化氢 C. 三氧化硫 D. 硫酸镁
难度: 中等查看答案及解析
-
下列有关化学实验操作正确的是

A. 检验K+的存在 B. 干燥CO2 C. 分离酒精与水 D. 蒸发食盐水
难度: 中等查看答案及解析
-
下列各组混合物中,能用分液漏斗进行分离的是
A. 溴和四氯化碳 B. 色拉油和水
C. 乙醇和水 D. 汽油和煤油
难度: 简单查看答案及解析
-
下列有关“化学与生活”的叙述正确的是
A. Fe(OH)3胶体无色、透明,能产生丁达尔现象
B. 六水氯化钙可用作食品干燥剂
C. 雾霾是一种分散系,分散剂是空气,带活性炭口罩防雾霾的原理是吸附原理
D. 用含硅胶、铁粉的透气小袋与食品一起密封包装, 该过程没有发生化学反应
难度: 中等查看答案及解析
-
下列化学反应中,属于氧化还原反应的是
A. CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
B. NaCl+AgNO3=AgCl↓+NaNO3
C. CaCO3
CaO+CO2↑
D. 2Na + 2H2O =2NaOH + H2↑
难度: 简单查看答案及解析
-
瓦斯中甲烷与氧气的质量比为1:4时极易爆炸,此时甲烷与氧气的体积比为( )
A. 1:4 B. 1:2 C. 1:1 D. 2:1
难度: 中等查看答案及解析
-
在化合、分解、置换、复分解等四类反应中,只选用同一类反应,不能实现的变化是
A. Cu→Cu(OH)2 B. MgCO3→Mg(OH)2
C. FeCl3→Fe2(SO4)3 D. C→H2CO3
难度: 中等查看答案及解析
-
在无土栽培时,需用0.5 mol·L-1 NH4Cl、0.16 mol·L-1 KCl、0.24 mol·L-1 K2SO4配制而成的营养液。若用KCl、NH4Cl和(NH4)2SO4三种固体来配制1 L营养液,则需此三种固体物质的量分别为
A. 0.4 mol、0.5 mol、0.12 mol B. 0.66 mol、0.5 mol、0.24 mol
C. 0.64 mol、0.5 mol、0.24 mol D. 0.64 mol、0.02 mol、0.24 mol
难度: 中等查看答案及解析
-
将标准状况下的a L HCl(g)溶于1 L水中,得到密度为ρ g·cm-3的盐酸溶液,则该盐酸的物质的量浓度为
A.
mol·L-1 B.
mol·L-1
C.
mol·L-1 D.
mol·L-1
难度: 困难查看答案及解析
-
NA表示阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4L乙醇的分子数约为NA
B. 14gN2和CO的混合气体中所含原子数为NA
C. 48gO2和O3的混合气体中所含的原子数为3NA
D. 1mo1·L-1的MgC12溶液中,C1-离子的数目为2 NA
难度: 中等查看答案及解析
-
下列实验操作完全正确的是
编号
实验
操作
A
用浓硫酸配制一定浓度的稀硫酸
准确量取浓硫酸,将浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中。
B
除去BaSO4中的少量BaCO3
加入足量盐酸,充分反应后,过滤、洗涤、干燥
C
量取盐酸溶液
用25 mL量筒量取4.0 mol/L的盐酸5.62 mL
D
取出分液漏斗中所需的上层液体
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
某同学在实验室进行了如图所示的实验,下列说法中错误的是
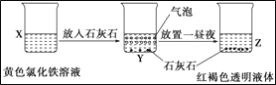
A. 利用过滤的方法,可将Z中固体与液体分离
B. X、Z烧杯中分散质相同
C. Y中产生的气体为CO2
D. Z中分散系能产生丁达尔效应
难度: 中等查看答案及解析
-
下列实验设计方案错误的是
A. 除去CO2气体中混有的HCl:饱和碳酸氢钠溶液
B. 分离碘和CCl4的混合物:分液
C. 区分NaCl和KCl溶液:焰色反应
D. 检验某未知溶液中的SO42-:加入稀硝酸酸化的BaCl2溶液
难度: 中等查看答案及解析
-
在浓度均为4.0 mol·L-1的盐酸和硫酸各100 mL溶液中,分别加入等质量的锌粉,充分反应后生成气体体积比为2∶3,则加入锌粉的质量是
A. 6.5 g B. 13.0 g C. 19.5 g D. 26.0 g
难度: 困难查看答案及解析