-
M和N两溶液分别含有下列十二种离子中的五种和七种离子:K+、Na+、H+、NH4+、Fe3+、A13+、Cl-、OH-、NO3-、S2-、CO32-、SO42-.己知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子应该是( )
A.Cl-、SO42-、NO3-
B.S2-、Cl-、SO42-
C.CO32-、NO3-、S2-
D.OH-、CO32-、SO42-难度: 中等查看答案及解析
-
CO2在大气中含量增加是产生“温室效应”的主要原因.下列反应中,不属于自然界缓解“温室效应”的是( )
A.CO2+H2O=H2CO3
B.Ca(OH)2+CO2=CaCO3↓+H2O
C.CaCO3+CO2+H2O=Ca(HCO3)2
D.6nCO2+12nH2O(C6H10O5)n+7nH2O+6nO2
难度: 中等查看答案及解析
-
用Cu(OH)2胶体做电泳实验时,阴极附近蓝色加深,往此胶体中加入下列物质时,不发生凝聚的是( )
①硫酸镁溶液 ②硅酸胶体 ③氢氧化铁胶体 ④葡萄糖溶液.
A.①②
B.②③
C.③④
D.①④难度: 中等查看答案及解析
-
已知阿佛加德罗常数为NA,下列说法正确的是( )
①1L 0.1mol/L氨水中NH3•H2O与NH4+微粒个数之和为0.1NA
②在同温同体积时,气体的质量越大,则压强越大
③8.4克NaHCO3中含有阴离子数目小于0.1NA
④31g 白磷中含有6NA个P-P键
⑤密闭容器中,氢气与足量氮气充分反应,生成17克氨时,转移电子数为3NA
⑥25℃时1LpH=7的醋酸与醋酸钠的混合溶液中,有10-7NA个水分子电离
⑦46gNO2和N2O4混合气体中含有原子数为3NA
⑧a mol H2SO4(浓)加入bmolZn粉反应后,无金属剩余,则反应结束时转移电子数共2bNA.
A.①②④
B.①⑥⑦
C.③⑤
D.⑤⑥⑦⑧难度: 中等查看答案及解析
-
利用碱性氧化性溶液的氧化作用,在钢铁表面形成一层深蓝色的Fe3O4(也可表示为FeFe2O4)薄膜,保护内部金属免受腐蚀,这种方法叫做烤蓝.烤蓝时发生如下反应:
①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑
②Na2FeO2+NaNO2+H2O-Na2Fe2O4+NH3↑+NaOH(未配平)
③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH
下列说法中正确的是( )
A.Fe3O4既可看作是氧化物,又可看作是亚铁盐
B.反应②配平后,H2O的化学计量数为3
C.反应③中,Na2Fe2O4是氧化剂,Na2FeO2是还原剂
D.以上三个反应都是氧化还原反应难度: 中等查看答案及解析
-
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
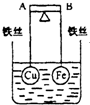
A.杠杆为导体和绝缘体时,均为A端高,B端低
B.杠杆为导体和绝缘体时,均为A端低,B端高
C.当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低
D.当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高难度: 中等查看答案及解析
-
在恒温、恒容条件下有下列气体反应:2A(g)+2B(g)⇌C(g)+2D(g).现分别从两条途径建立平衡:Ⅰ.A和B的起始浓度均为2mol/L;Ⅱ.C和D的起始浓度分别为2mol/L和4mol/L.下列叙述正确的是( )
A.最终达到平衡时,两个体系内混合气体的平均分子量相同
B.最终达到平衡时,Ⅰ中C(A)小于Ⅱ中C(A)的
C.最终达到平衡时,途径Ⅰ的反应时间等于途径Ⅱ的反应时间的
D.最终达到平衡时,途径Ⅰ混合气体的密度为途径Ⅱ混合气体密度的难度: 中等查看答案及解析
-
用惰性电极电解2L1mol/L硫酸铜溶液,在电路中通过0.5mol电子后,将电源反接,电路中又通过1mol电子,此时溶液中,H+浓度是(设溶液的体积不变)( )
A.1.5mol/L
B.0.75mol/L
C.0.5mol/L
D.0.25mol/L难度: 中等查看答案及解析