-
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液难度: 中等查看答案及解析
-
下列物质属于非电解质的是( )
A.金属钠
B.CaCl2
C.H2SO4
D.SO2难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.3.01×1023个SO2分子的质量为32g
B.CH4的摩尔质量为16g
C.1molH2O的质量为18g/mol
D.标准状况下,1mol任何物质体积均为22.4L难度: 中等查看答案及解析
-
在容量瓶上无需有的标记是( )
A.刻度线
B.温度
C.浓度
D.规格(容量)难度: 中等查看答案及解析
-
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( )
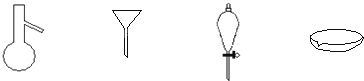
A.蒸馏、蒸发、萃取、过滤
B.蒸馏、过滤、萃取、蒸发
C.萃取、过滤、蒸馏、蒸发
D.过滤、蒸发、萃取、蒸馏难度: 中等查看答案及解析
-
下列电离方程式错误的是( )
A.K2CO3=2K++CO32-
B.NaOH=Na++OH-
C.KClO3=K++Cl-+3O2-
D.NH4Cl=NH4++Cl-难度: 中等查看答案及解析
-
物质的量相等的两种气体,必然( )
A.体积相同
B.均为22.4L
C.原子数相同
D.分子数相同难度: 中等查看答案及解析
-
同温同压下,等质量的下列气体所占有的体积最大的是( )
A.SO2
B.CH4
C.CO2
D.O2难度: 中等查看答案及解析
-
胶体区别于其他分散系的本质特征是( )
A.胶体的分散质能通过滤纸空隙,而浊液的分散质不能
B.产生丁达尔现象
C.分散质粒子直径在1nm~100nm之间
D.胶体在一定条件下能稳定存在难度: 中等查看答案及解析
-
下列数量的物质中含原子数最多的是( )
A.4℃时5.4mL水
B.标准状况下5.6L二氧化碳
C.0.4mol氧气
D.10g氖难度: 中等查看答案及解析
-
下列溶液中Cl-浓度与50mL 1mol•L-1 AlCl3溶液中Cl-浓度相等的是( )
A.150mL 1.5mol•L-1的NaCl溶液
B.75mL 2mol•L-1的NH4Cl溶液
C.150mL 1mol•L-1的KCl溶液
D.75mL 1mol•L-1的FeCl3溶液难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A.碳酸钙和盐酸反应CO32-+2H+=H2O+CO2↑
B.向氢氧化钡溶液中加硫酸溶液Ba2++SO42-=BaSO4↓
C.向稀盐酸溶液中加铁3Fe+6H+=2Fe3++3H2↑
D.向硝酸银溶液中加盐酸Ag++Cl-=AgCl↓难度: 中等查看答案及解析
-
如图为反应Fe+CuSO4═FeSO4+Cu中电子转移的关系图,则图中的元素甲、乙分别表示( )
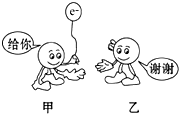
A.Fe Cu
B.Cu S
C.Fe O
D.Fe S难度: 中等查看答案及解析
-
1molSO2和1molSO3具有相同的①分子数 ②原子数 ③S原子数 ④O原子数( )
A.①②
B.①③
C.①④
D.②④难度: 中等查看答案及解析
-
为了实现下列各变化,需还原剂物质的是( )
A.KClO3→O2
B.NH4+→NH3
C.Fe→FeCl3
D.CO2→CO难度: 中等查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是( )
A.K+、Cu2+、NO3-、SO42-
B.Na+、Ba2+、CO32-、NO3-
C.Na+、H+、Cl-、CO32-
D.Mg2+、H+、C1-、OH-难度: 中等查看答案及解析
-
在一定温度和压强下,1体积X2气体与3体积Y2气体化合生成2体积气体化合物,则该气体化合物的化学式为( )
A.X2Y3
B.XY3
C.XY
D.X3Y难度: 中等查看答案及解析
-
相同体积的氯化钠、氯化镁、氯化铝溶液分别与过量的硝酸银溶液反应,所生成的沉淀物质的量相同,则原氯化钠、氯化镁、氯化铝溶液的物质的量浓度之比为( )
A.6:3:2
B.3:2:1
C.6:3:1
D.1:2:3难度: 中等查看答案及解析
-
为了除去粗盐中的Ca2+,Mg2+,SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序( )
①过滤; ②加过量NaOH溶液; ③加适量盐酸;
④加过量Na2CO3溶液; ⑤加过量BaCl2溶液.
A.④②⑤①③
B.④①②⑤③
C.②⑤④①③
D.①④②⑤③难度: 中等查看答案及解析
-
在无土栽培液中,每升溶液需用0.5mol NH4Cl溶液、0.16mol KCl溶液、0.24molK2SO4溶质作为培养液,若用KCl、NH4Cl和(NH4)2SO4三种物质来配制1.00L上述营养液,所需三种盐的物质的量是( )
A.0.4mol、0.5mol、0.12mol
B.0.66mol、0.5mol、0.24mol
C.0.64mol、0.5mol、0.24mol
D.0.64mol、0.02mol、0.24mol难度: 中等查看答案及解析
-
已知下列反应可以发生:Br2+2NaI=2NaBr+I2,Cl2+2NaBr=2NaCl+Br2,则关于Cl2,Br2,I2氧化性强弱说法中,正确的是( )
A.氧化性:I2>Br2>Cl2
B.氧化性:Br2>I2>Cl2
C.氧化性:Cl2>Br2>I2
D.氧化性:I2>Cl2>Br2难度: 中等查看答案及解析