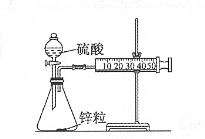
-
已知4NH3 + 5O2 = 4NO + 6H2O(g),若反应速率分别是ν(NH3)、ν(O2)、ν(NO)、ν(H2O)(单位:mol•L-1•min-1)。下列关系正确的是
A.
ν(NH3)=ν(O2) B.
ν(O2)=ν(H2O)
C.
ν(NH3)=ν(H2O) D.
ν(O2)=ν(NO)
难度: 中等查看答案及解析
-
某一反应物的浓度是1.0 mol/L,经过20 s后,它的浓度变成了0.2 mol/L,在这20 s用该物质浓度变化表示的化学反应速率为
A.0.04 B.0.04 mol/(L·s)
C.0. 08 mol/(L · s) D.0.04 mol/L
难度: 中等查看答案及解析
-
化学反应速率是通过实验测定的,下列化学反应速率的测量中,测量依据不可行的是
选项
化学反应
测量依据(单位时间内)
A
2NO2
N2O4
颜色深浅
B
Zn+H2SO4=ZnSO4+H2
H2体积
C
CO(g)+H2O(g)=CO2(g)+H2(g)
压强变化
D
Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
沉淀质量
难度: 中等查看答案及解析
-
对于N2+3H2
 2NH3,下列不同物质表示的反应速率最大的是
2NH3,下列不同物质表示的反应速率最大的是A.v(N2)=0.01 mol·L-1· min-1 B.v(H2)=0.06 mol·L-1· min-1
C.v(NH3)=0.02 mol·L-1· min-1 D.v(H2)=0.002 mol·L-1· min-1
难度: 中等查看答案及解析
-
对反应A+B
AB来说,常温下按以下情况进行反应:①20 mL溶液中含A、B各0.01 mol;②50 mL溶液中含A、B各0. 05 mol;③0. 1 mol•L−1的A、B溶液各10 mL;④0. 3 mol•L−1的A、B溶液各50 mL。四者反应速率大小关系是
A.②>①>④>③ B.④>③>②>①
C.①>②>④>③ D.①>②>③>④
难度: 中等查看答案及解析
-
用下列实验装置和方法进行的相应实验,能达到实验目的的是
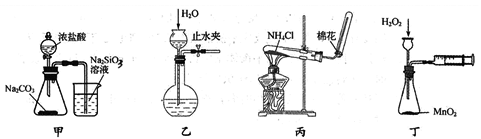
A.用甲装置比较盐酸、碳酸和硅酸的酸性强弱
B.用乙所示方法检验装置的气密性
C.用丙装置制备和收集氨气
D.用丁装置测定化学反应速率
难度: 中等查看答案及解析