-
下列有机物不能通过加成反应制取的是( )
A.CH3CH2Cl
B.CH2ClCH2Cl
C.CH3CH2OH
D.CH3COOH难度: 中等查看答案及解析
-
不能用溴水鉴别的是( )
A.甲烷、乙烯
B.苯、乙醇
C.乙醇、乙酸
D.苯、四氯化碳难度: 中等查看答案及解析
-
化学与我们的生活、社会密切相关,下列说法不正确的是( )
A.蛋白质遇浓硝酸变黄是发生了颜色反应
B.富含蛋白质的食物多属于酸性食物,蔬菜、水果多属于碱性食物
C.麻黄碱是一种天然药物,能增加人的兴奋程度,运动员可以使用
D.碘元素是人体神经系统发育所不可缺少的“智力元素”难度: 中等查看答案及解析
-
“绿色化学”是当今社会提出的一个新概念.在绿色化学工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%.以下反应最符合绿色化学,原子经济性要求的是( )
A.乙烯聚合为聚乙烯高分子材料
B.甲烷与氯气制备一氯甲烷
C.以铜和浓硝酸为原料生产硝酸铜
D.用二氧化硅制备高纯硅难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.煤的气化是化学变化,煤的液化是物理变化
B.甲烷是一种清洁燃料,可用作燃料电池的燃料
C.蔗糖与淀粉水解的最终产物都是葡萄糖
D.石油分馏可以得到乙烯、丙烯、甲烷等化工原料难度: 中等查看答案及解析
-
向淀粉中加入少量稀H2SO4,并加热.为了确定淀粉是否已水解或完全水解,所需下列试剂的组合正确的是①NaOH溶液,②银氨溶液,③新制Cu(OH)2碱性悬浊液,④碘水,⑤BaCl2( )
A.①⑤
B.②④
C.②③④
D.①③④难度: 中等查看答案及解析
-
下列化学用语表达正确的是( )
A.二氧化碳的电子式:
B.氯离子的结构示意图:
C.乙烯的结构简式:C2H4
D.质量数为18的氧原子:618O难度: 中等查看答案及解析
-
以下烃中二氯代物只有两种的是( )
A.(CH3)2CHCH3
B.CH3CH2CH3
C.CH3CH2CH2CH3
D.C(CH3)4难度: 中等查看答案及解析
-
关于化学键的下列叙述中正确的是( )
A.离子化合物不含共价键
B.共价化合物可能含有离子键
C.离子化合物中只含离子键
D.共价化合物不含离子键难度: 中等查看答案及解析
-
下表是元素周期表的一部分,有关说法正确的是( )
①a、b、e、f四种元素的元素的原子半径:e>f>b>a期
周
族IA IIA IIIA IVA VA VIA VIIA 2 a b 3 d e f g h i
②h、i两种元素阴离子的还原性:h>i
③a、g两种元素氢化物的稳定性:a>g
④d、e、f三种元素最高价氧化物对应的水化物的碱性依次增强
⑤八种元素中d元素的单质还原性最强,i元素的单质氧化性最强.
A.①③④
B.②③⑤
C.②④⑤
D.①③⑤难度: 中等查看答案及解析
-
短周期元素X、Y、Z和W的原子序数依次递增,且在同一周期,四种元素原子的最外层电子数之和为19,X和Y元素原子的原子序数比为6:7,X的最高正价是W的最低负价的绝对值的2倍.下列说法正确的是( )
A.X单质可以通过铝热法获得
B.Y的氧化物是良好的半导体材料
C.Z的氢化物比W的氢化物更稳定
D.X的最高价氧化物和Z的最高价氧化物化合的产物中有共价键和离子键难度: 中等查看答案及解析
-
下列金属的冶炼原理中不正确的是( )
A.2NaCl(熔融)2Na+Cl2↑
B.MgO+CMg+CO↑
C.Al2O3+3CO2Al+3CO2
D.2HgO2Hg+O2↑
难度: 中等查看答案及解析
-
如图所示为氢氧燃料电池的原理示意图,按照此图的提示,下列叙述不正确的是( )
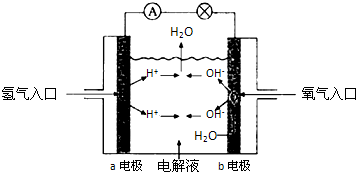
A.a电极是负极
B.b电极的电极反应为:4OH--4e-═2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置难度: 中等查看答案及解析
-
下列说法中不正确的是( )
A.化学反应中的能量变化,通常表现为热量的变化
B.反应物的总能量高于生成物的总能量时发生放热反应
C.Ba(OH)2•8H2O与NH4Cl的反应是吸热反应
D.木炭在氧气中的燃烧是吸热反应难度: 中等查看答案及解析
-
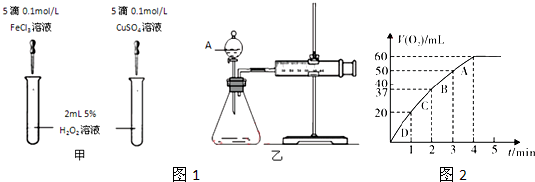
下列各组实验中,过氧化氢分解最快的是( )
H2O2的浓度(质量分数) 温度(℃) 催化剂的使用 A 2 10 使用MnO2 B 4 10 不使用 C 6 30 使用MnO2 D 6 30 不使用
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)在体积10L的密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(x)(反应物的消耗速率或产物的生成速率)可表示为( )
A.v(NH3)=0.010mol•L-1•s-1
B.v(O2)=0.0010mol•L-1•s-1
C.v(NO)=0.0010mol•L-1•s-1
D.v(H2O)=0.045mol•L-1•s-1难度: 中等查看答案及解析
-
在一定条件下,对于密闭容器中进行的可逆反应:N2+3H2
2NH3,下列说法中,能充分说明这一反应已经达到化学平衡状态的是( )
A.N2、H2与NH3的物质的量之比为1:3:2
B.N2、H2与NH3的浓度相等
C.各组分的浓度不再发生变化
D.反应停止,正、逆反应速率都等于零难度: 中等查看答案及解析
-
从南方往北方长途运输水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是( )
A.利用高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
B.利用高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C.利用高锰酸钾溶液的氧化性,催熟水果
D.利用高锰酸钾溶液杀死水果周围的细菌,防止水果霉变难度: 中等查看答案及解析
-
某有机物的结构为
 ,这种有机物不可能具有的性质是( )
,这种有机物不可能具有的性质是( )
A.能跟NaOH溶液反应
B.能使酸性KMnO4溶液褪色
C.能发生酯化反应
D.能发生水解反应难度: 中等查看答案及解析
-
验证某有机物中含有氧元素,应完成的实验内容是( )
A.只有验证它完全燃烧后产物只有H2O和CO2
B.测定该试样的质量及该试样完全燃烧后生成CO2和H2O的质量
C.测定完全燃烧时消耗有机物与生成的CO2、H2O的物质的量之比
D.只有测定其燃烧产物中H2O和CO2物质的量的比值难度: 中等查看答案及解析