-
下列实验操作中错误的是( )
A.用规格为10mL的量筒量取6mL的液体
B.用药匙或者纸槽把粉末状药品送入试管底部
C.过滤时玻璃棒的末端应轻轻的靠在三层的滤纸上
D.如果没有试管夹,可以临时手持试管给固体或液体加热难度: 中等查看答案及解析
-
小强在奥运五连环中填入了5种物质,使相连环物质间能发生反应,不相连环物质间不能发生反应.你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型和属于氧化还原反应的个数为( )
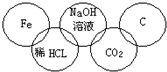
A.化合反应、3个
B.分解反应、2个
C.复分解反应、1个
D.置换反应、2个难度: 中等查看答案及解析
-
下列微粒只能作还原剂的是( )
A.S2-
B.Fe2+
C.Fe3+
D.H+难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.NaCl溶液在电流作用下电离成Na+和Cl-
B.溶于水后能够电离出H+的化合物都是酸
C.氯化氢溶于水能够导电,但液态氯化氢不能够导电
D.导电性强的溶液里自由移动离子数目一定比导电性弱的溶液里自由移动离子数目多难度: 中等查看答案及解析
-
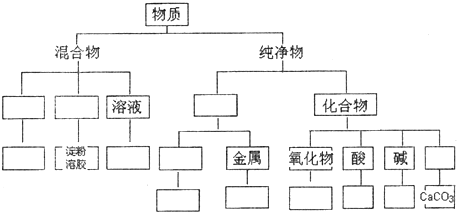
Na2CO3俗名纯碱,下面是对纯碱采用不同的分类法的分类,不正确的是( )
A.Na2CO3是盐
B.Na2CO3是碱
C.Na2CO3是钠盐
D.Na2CO3是碳酸盐难度: 中等查看答案及解析
-
“服用维生素C可使食物中的三价铁离子变成二价铁离子”这句话说明( )
A.维生素C本身被还原
B.维生素C具有还原性
C.维生素C具有氧化性
D.维生素C发生了还原反应难度: 中等查看答案及解析
-
关于胶体和溶液的区别,下列叙述中正确的是( )
A.溶液呈电中性,胶体带有电荷
B.溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸
C.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明显光带
D.溶液稳定,放置后不会生产沉淀,胶体不稳定,放置会生成沉淀难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.H++OH-=H2O表示所有强酸和强碱的反应
B.所有的离子方程式都可以表示一类反应
C.单质和氧化物在离子方程式中不能用离子符号表示
D.凡是易溶于水的化合物都可以写成离子形式难度: 中等查看答案及解析
-
将铁片放到下列溶液中,铁片溶解,溶液质量减轻的是( )
A.稀硫酸
B.硫酸铜溶液
C.稀盐酸
D.浓硝酸难度: 中等查看答案及解析
-
在酸性溶液中能大量共存的无色离子组是( )
A.K+、Mg2+、Cl-、MnO4-
B.Na+、Cu2+、CO32-、NO3-
C.K+、Na+、SO32-、Cl-
D.Na+、Mg2+、Cl-、SO42-难度: 中等查看答案及解析
-
将氢氧化钠溶液逐滴加入含有盐酸的AlCl3溶液时,图中曲线正确的是(x轴表示加入NaOH溶液的体积,y轴表示沉淀的量)( )
A.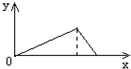
B.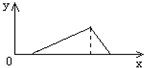
C.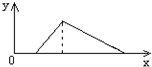
D.难度: 中等查看答案及解析
-
根据反应式:(1)2Fe3++2I-=2Fe2++I2,(2)Br2+2Fe2+=2Fe3++2Br-,判断下列离子的还原性由强到弱的顺序是( )
A.Br-、Fe2+、I-
B.I-、Fe2+、Br-
C.Br-、I-、Fe2+
D.Fe2+、I-、Br-难度: 中等查看答案及解析
-
有200mLMgCl2和AlCl3的混合溶液,其中Mg2+浓度为0.2mol•L-1,Cl-浓度为1.3mol•L-1.要使Mg2+全部转化为沉淀分离出来,至少需加4mol•L-1NaOH溶液的体积为( )
A.40mL
B.72mL
C.80mL
D.128mL难度: 中等查看答案及解析
-
一同学欲从量筒中取出部分液体,他先俯视凹液面的最低处,读数为50mL,倒出液体后,他又仰视凹液面的最低处,读数为10mL他实际倒出液体的体积为( )
A.40mL
B.大于40mL
C.小于40mL
D.不一定难度: 中等查看答案及解析
-
将氯化钠、三氯化铝、氯化亚铁、氯化铁四种溶液,通过一步实验就能加以区别的试剂是( )
A.KSCN
B.NaOH
C.BaCl2
D.HCl难度: 中等查看答案及解析
-
下列说法中正确的是( )
A.含氧的化合物一定是氧化物
B.酸根中一定含有氧元素
C.盐的组成中一定含有金属元素
D.碱性氧化物一定是金属氧化物难度: 中等查看答案及解析
-
下列有关Na2CO3和NaHCO3性质的比较中,正确的是( )
A.热稳定性:Na2CO3<NaHCO3
B.与同浓度的稀盐酸反应的快慢:Na2CO3>NaHCO3
C.等物质的量的Na2CO3和NaHCO3分别与过量盐酸反应,放出CO2质量:Na2CO3>NaHCO3
D.常温时溶解度:Na2CO3>NaHCO3难度: 中等查看答案及解析
-
某溶液中可能含有SO42-、CO32-、Cl-.为了检验其中是否含有SO42-,除BaCl2溶液外,还需要的溶液是( )
A.H2SO4
B.HCl
C.NaOH
D.NaNO3难度: 中等查看答案及解析
-
相同质量的两份铝粉,分别跟足量的稀H2SO4和NaOH溶液反应,生成的气体体积之比为( )
A.3:2
B.3:1
C.1:1
D.1:3难度: 中等查看答案及解析
-
下列关于金属铝的叙述中,说法不正确的是( )
A.Al是地壳中含量最多的元素
B.Al是比较活泼的金属,在化学反应中容易失去电子,表现还原性
C.铝箔在空气中受热可以熔化,且发生剧烈燃烧
D.铝箔在空气中受热可以熔化,由于氧化膜的存在,熔化的铝并不滴落难度: 中等查看答案及解析
-
向20mL2mol/LAlCl3溶液中,加入30mLNaOH溶液,充分反应后,得0.78g沉淀,则NaOH溶液的物质的量浓度为( )
A.1mol/L
B.2mol/L
C.4mol/L
D.5mol/L难度: 中等查看答案及解析
-
下列反应既是离子反应,又是氧化还原反应的是( )
A.氯化钠溶液中滴入硝酸银溶液
B.氢气还原氧化铜
C.铁片置于硫酸铜溶液中
D.一氧化碳的燃烧难度: 中等查看答案及解析
-
可用于判断碳酸氢钠溶液中混有碳酸钠的实验方法是( )
A.加热时有无气体放出
B.溶于水后滴加氯化钡稀溶液,有白色沉淀生成
C.滴加盐酸时有无气泡放出
D.溶于水后滴加澄清石灰水,有白色沉淀生成难度: 中等查看答案及解析
-
用FeCl3溶液腐蚀印刷电路板上铜箔的反应是:2Fe3++Cu=2Fe2++Cu2+.下列有关说法不正确的是( )
A.Cu是还原剂
B.Fe3+是氧化剂
C.氧化性:Cu2+>Fe3+
D.该反应属于离子反应难度: 中等查看答案及解析
-
在甲、乙两烧杯溶液中,共含有大量的Cu2+、Na+、H+、SO42-、CO32-、OH-等6种离子.已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( )
A.Cu2+、H+、SO42-
B.Na+、OH-、CO32-
C.CO32-、OH-、SO42-
D.Na+、H+、SO42-难度: 中等查看答案及解析