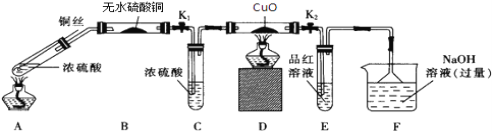
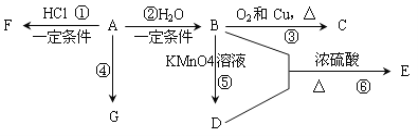
-
下列设备工作时,将化学能转化为电能的是
A
B
C
D




硅太阳能电池
铅蓄电池
燃气灶
电烤箱
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
化学与生活密切相关,下列说法正确的是( )
A. 医用酒精的浓度通常为95%
B. 漂白粉可以在敞口容器中长期存放
C. 常温下可用铁制容器贮藏运输浓硫酸
D. 干电池用完后,应回收并进行填埋处理
难度: 简单查看答案及解析
-
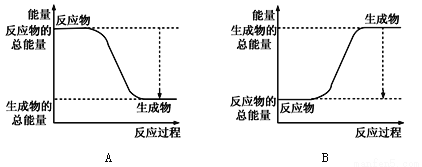
下列属于放热反应的是( )
A. 铝热反应 B. 煅烧石灰石(CaCO3)制生石灰(CaO)
C. C与CO2共热 D. Ba(OH)2·8H2O晶体与NH4Cl晶体反应
难度: 简单查看答案及解析
-
下列分子式只能表示一种物质的是( )
A. CH2Cl2 B. C4H10 C. C5H12 D. C6H12
难度: 简单查看答案及解析
-
反应C(s)+H2O(g)
CO(g)+H2(g)在一密闭容器中进行,下列条件的改变能加快反应速率的是( )
A. 增加C的量 B. 压缩容器体积
C. 保持容器体积不变,充入N2 D. 保持压强不变,降低容器内的温度
难度: 中等查看答案及解析
-
下列烯烃和H2O发生加成反应所得产物有同分异构体的是( )
A. CH3CH=CH2 B. CH3CH=CHCH3
C. CH2=CH2 D. (CH3)2C=C(CH3)2
难度: 简单查看答案及解析
-
巴豆酸的结构简式为CH3—CH = CH—COOH。下列关于该物质的说法不正确的是( )
A. 分子式为C4H6O2
B. 含有两种不同的官能团
C. 能发生氧化、取代、加成、酯化等反应
D. 分子中所有原子有可能在同一平面
难度: 中等查看答案及解析
-
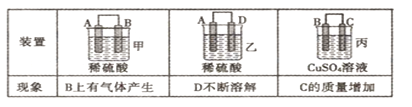
下列实验操作不当的是( )
A. 用稀硫酸和锌粒制取H2时,加几滴CuSO4溶液以加快反应速率
B. 利用酸性高锰酸钾溶液除甲烷中的少量乙烯
C. 用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有Na+
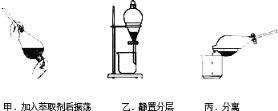
D. 向溴水中加入苯,可以萃取溴水中的溴
难度: 中等查看答案及解析
-
a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如右图所示。下列叙述正确的是( )
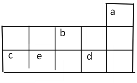
A. b元素除0价外,只有一种化合价
B. 五种元素中,c元素的化学性质最稳定
C. d气态氢化物溶于水,溶液显碱性
D. 元素原子半径大小:d<e<c
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
A. 1 mol乙烷和1 mol乙烯中,化学键数相同
B. 0.1 mol Na2O2与足量的二氧化碳反应转移的电子数为0.1 NA
C. 1.7g 羟基(-OH)所含电子的数目为NA
D. 56g Fe与足量的水蒸汽充分反应生成氢气,转移电子数为3 NA
难度: 困难查看答案及解析
-
制取一氯乙烷的最佳方法是 ( )
A. 乙烷和氯气反应
B. 乙烯和氯气反应
C. 乙烯和氯化氢反应
D. 乙烯和氢气反应后,所得产物再和氯气反应
难度: 中等查看答案及解析
-
列实验操作能达到实验目的的是( )
实验目的
实验操作
A
比较水和乙醇中氢的活泼性
分别将少量钠投入到盛有水和乙醇的烧杯中
B
配制稀硫酸
先将浓硫酸加入烧杯中,后倒入蒸馏水
C
除去Cu粉中混有的CuO
加入稀硝酸溶液,过滤、洗涤、干燥
D
证明SO2具有漂白性
把SO2通入紫色石蕊试液中
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大,其中X是组成有机物的基本骨架元素,常温下,Y的块状单质在Z的最高价氧化物对应水化物的浓溶液中会发生钝化。下列说法一定正确的是( )
A. 氧化物对应水化物的酸性:W>X
B. 单质沸点:W>Z
C. 最简单氢化物的稳定性:W>Z
D. Y、W形成的化合物中既含有离子键,又含有共价键
难度: 中等查看答案及解析
-
某烷烃相对分子质量为72,跟氯气反应生成的一氯代物只有一种,该烷烃是( )
A. 丁烷 B. 己烷 C. 2—甲基丁烷 D. 2,2—二甲基丙烷
难度: 简单查看答案及解析
-
Al-Ag2O电池是一种可用作水下动力的优良电源,其原理如图所示。该电池工作时总反应式为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则下列说法错误的是 ( )
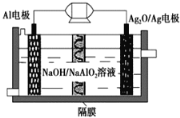
A. 工作时正极发生还原反应,且正极质量逐渐减小
B. 当电极上生成1.08 g Ag时,电路中转移的电子为0.01 mol
C. Al电极做负极,电极反应式为:Al-3e-=Al3+
D. 工作时电解液中的Na+移向Ag2O/Ag电极
难度: 困难查看答案及解析