-
用特殊方法把固体物质加工到纳米级(1nm~100nm,1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的微粒直径和这种粒子具有相同数量级的是( )
A. 溶液 B. 悬浊液 C. 胶体 D. 乳浊液
难度: 简单查看答案及解析
-
下列实验操作中错误的是( )
A. 萃取操作时,萃取剂必须与水不互溶
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 分液操作时,分液漏斗中下层溶液从下口放出,上层液体从上口倒出
D. 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
难度: 简单查看答案及解析
-
从硫元素的化合价态上判断,下列物质中的硫元素不能表现氧化性的是
A. Na2S B. S C. SO2 D. H2SO4
难度: 简单查看答案及解析
-
化学实验有助于理解化学知识,形成化学观念。下列实验操作正确的是( )
A. 称量药品
 B. 过滤
B. 过滤
C. 分离乙醇和水
 D. 收集二氧化硫
D. 收集二氧化硫
难度: 简单查看答案及解析
-
某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,则该溶液中( )
A. 一定有
B. 可能有
或
C. 一定无
D. 还可能有
难度: 中等查看答案及解析
-
在物质分类上,Ba(OH)2(固态)、CuSO4(固态)、CH3COOH(液态)等可归为一类,下列物质中还可以和他们归为一类的是( )
A. 75%的酒精溶液 B. 硝酸钠
C. Fe(OH)3胶体 D. 豆浆
难度: 中等查看答案及解析
-
下列关于物质分类的依据中不正确的是( )
A. KNO3是电解质,因为KNO3能溶于水
B. 豆浆是胶体,因为豆浆中分散质粒子的大小在1~100nm之间
C. Na2O2是氧化物,因为Na2O2由两种元素组成,其中一种是氧元素
D. H2SO4是酸,因为H2SO4在水溶液中电离产生的阳离子全部是H+
难度: 简单查看答案及解析
-
农药波尔多液不能用铁或铝的容器贮存,是因为铁或铝能跟该农药中的硫酸铜发生化学反应,该反应属无机物反应基本类型中的( )
A. 置换反应 B. 分解反应 C. 化合反应 D. 复分解反应
难度: 简单查看答案及解析
-
下列说法正确的是:( )
A. 如果5.6L N2含有n个氮分子,则NA一定约为4n
B. 18g水中含有的电子数是8NA
C. 在100mL 0.5mol/L盐酸溶液中含有氯化氢分子数为0.05NA
D. 15g
含有8mol电子
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 0.3mol氢气中所含的氢原子数目为0.3NA
B. 标准状况下,4.48L水中所含水分子的数目为0.2NA
C. 0.2mol/L CaCl2溶液中所含氯离子的数目为0.4NA
D. 2.3g钠与足量水反应,生成钠离子的数目为0.1NA
难度: 简单查看答案及解析
-
在含有大量Na+、OH-、
的溶液中,还可能大量存在的离子是( )
A. Ca2+ B. Fe3+ C.
D.
难度: 简单查看答案及解析
-
下列溶液中c(Cl-)与50mL 1mol/L的氯化铝溶液中的c(Cl-)相等的是( )
A. 150mL 1mol/L氯化钠溶液 B. 75mL 2mol/L氯化铵溶液
C. 150mL 3mol/L氯化钾溶液 D. 75mL 2mol/L氯化钡溶液
难度: 简单查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A. 锌粒与稀盐酸反应:Zn+2H+=Zn2++H2↑
B. 溴化钠溶液与氯气反应:Br﹣+Cl2=Cl﹣+Br2
C. 氢氧化铜与稀硫酸反应:OH﹣+H+=H2O
D. 钠与水反应:Na++2H2O=Na++2OH﹣+H2↑
难度: 中等查看答案及解析
-
除去下列括号内的杂质,所加试剂和操作均正确的是( )
选项
需除杂的物质
试剂
操作
A
NaCl(Na2CO3)
水
蒸发结晶
B
CaCO3(CaCl2)
水
过滤
C
Zn(Cu)
稀盐酸
过滤
D
CO2(HCl)
饱和NaOH溶液
将气体通过洗气瓶
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列关于铝的叙述中不正确的是( )
A. 铝是地壳里含量最多的金属元素
B. 常温下铝不与氧气反应,所以铝抗腐蚀
C. 铝既能和强酸反应也能与强碱反应
D. 铝的还原性比钠弱
难度: 简单查看答案及解析
-
关于反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O的说法正确的是
A. HCl是氧化剂 B. KMnO4在反应中被氧化
C. 每生成1 mol Cl2转移2 mol e- D. 该反应中HCl只体现出酸性
难度: 中等查看答案及解析
-
吸进人体内的氧有2%转化为氧化性极强的活性氧,活性氧能加速人体衰老,被称为“生命杀手”,中国科学家尝试用Na2SeO3清除人体内的活性氧,则Na2SeO3的作用是( )
A. 还原剂 B. 氧化剂
C. 既是氧化剂又是还原剂 D. 以上均不是
难度: 简单查看答案及解析
-
海水提溴过程中,将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生作用以达到富集的目的,化学反应为Br2+SO2+2H2O=2HBr+H2SO4,下列说法正确的是( )
A. Br2在反应中表现氧化性
B. SO2在反应中被还原
C. Br2在反应中失去电子
D. 1mol Br2在反应中得到1mol电子
难度: 简单查看答案及解析
-
将一小块钠投入到盛有硫酸铜溶液的小烧杯中,不可能观察到的现象是( )
A. 溶液中出现蓝色浑浊
B. 钠块熔成小球浮在水面四处游动
C. 有气体产生
D. 有红色的铜被置换出来
难度: 中等查看答案及解析
-
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反应中镁和铝的( )
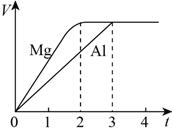
A. 物质的量之比为1:1 B. 质量之比为4:3
C. 摩尔质量之比为2:3 D. 反应速率铝大于镁
难度: 中等查看答案及解析
-
已知有如下反应:
①
+Cl2=Br2+
,②
+5Cl-+6H+=3Cl2+3H2O,
③2FeCl3+2KI=2FeCl2+2KCl+I2,④2FeCl2+Cl2=2FeCl3。
下列各微粒氧化能力由强到弱的顺序正确的是( )
A.
>
>Cl2>Fe3+>I2 B.
>Cl2>
>I2>Fe3+
C.
>
>Cl2>Fe3+>I2 D.
>
>Fe3+>Cl2>I2
难度: 中等查看答案及解析
-
将40mL 1.5mol·L-1的CuSO4溶液与30mL 3mol·L-1的NaOH溶液混合,生成浅蓝色沉淀,假如溶液中c(Cu2+)或c(OH-)都已变得很小,可忽略,则生成沉淀的组成可表示为( )
A. Cu(OH)2 B. CuSO4·Cu(OH)2
C. CuSO4·2Cu(OH)2 D. CuSO4·3Cu(OH)2
难度: 中等查看答案及解析
-
由Na2SO4和NaNO3组成的混合物88g溶于水配制成1L溶液,此溶液中Na+的浓度为1.2mol/L,则原混合物中NaNO3的质量为
A. 17g B. 34g C. 25.5g D. 51g
难度: 中等查看答案及解析