-
在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。以下反应最符合绿色化学原子经济要求的是
A.乙烯聚合为聚乙烯高分子材料 B.甲烷与氯气制备一氯甲烷
C.以铜和浓硝酸为原料生产硝酸铜 D.用二氧化硅制备高纯硅
难度: 中等查看答案及解析
-
下列说法中正确的一组是
A.H2和D2互为同素异形体;
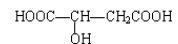
B.
和
互为同分异构体;
C.正丁烷和异丁烷是同系物;
D.
和
是同一种物质
难度: 中等查看答案及解析
-
把100mL 2mol/L的H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率而不影响生成H2的总量,可在反应物中加入适量的
A.硫酸铜溶液 B.硝酸钠溶液 C.醋酸钠溶液 D.氢氧化钠溶液
难度: 中等查看答案及解析
-
下列用水就能鉴别的一组物质是
A.苯、己烷、四氯化碳 B.苯、乙醇、四氯化碳
C.硝基苯、乙醇、四氯化碳 D.硝基苯、乙醇、乙酸
难度: 中等查看答案及解析
-
对铜—锌—稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是①锌片溶解了32.5克 ②锌片增重了32.5克 ③铜片上析出1克氢气④铜片上析出1mol氢气
A. ①③ B.①④ C. ②③ D. ②④
难度: 中等查看答案及解析
-
两种元素可以形成AB2型共价化合物的是
A.无中子的原子与最外层有6个电子的短周期元素的原子
B.核电荷数分别为12和17的元素
C.ⅣA族和ⅥA族原子半径最小的元素
D.最高正价都为奇数的两种短周期元素
难度: 中等查看答案及解析
-
冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或H2、CO)法;③活泼金属置换法;④电解法。这四种方法在工业上均有应用。古代有:(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜。现代有:(Ⅲ)铝热法炼铬;(Ⅳ)从光卤石中炼镁。对它们的冶炼方法的分析,不正确的是
A.(Ⅰ),① B.(Ⅱ),② C.(Ⅲ),③ D.(Ⅳ),④
难度: 中等查看答案及解析
-
下列各组中,不管以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳物质的量不变的是
A.乙烯(C2H4)和乙炔(C2H2) B.乙醇和丙醇(CH3CH2CH2OH)
C.乙醇和乙醚(C2H5OC2H5) D.甲醛( HCHO)和乙酸
难度: 中等查看答案及解析
-
氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量。在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A.Q1+ Q2<2Q3 B.Q1+ Q2>2Q3 C.Q1+ Q2<Q3 D.Q1+ Q2>Q3
难度: 中等查看答案及解析
-
巴豆酸的结构简式为CH3CH=CHCOOH 现有:①氯化氢,②溴水, ③纯碱溶液,④酸性KMnO4溶液, ⑤乙醇,试根据其结构特点,判断在一定条件下能与巴豆酸反应的物质组合是
A.只有②④⑤ B.只有①③④ C.只有①②③ D.都可以
难度: 中等查看答案及解析
-
下列关于有机物的说法中,正确的一组是
①“乙醇汽油”是在汽油里加入适量乙醇而成的一种燃料,它是一种新型化合物
②汽油、柴油和植物油都是碳氢化合物,完全燃烧只生成
③石油的分馏、煤的气化和液化都是物理变化。
④淀粉和纤维素水解的最终产物都是葡萄糖
⑤将ag铜丝灼烧成黑色后趁热插入乙醇中,铜丝变红,再次称量质量等于ag
⑥除去
中的少量
,可将混合气体通过盛有溴水的洗气瓶
A.③⑤⑥ B.④⑤⑥ C.①②⑤ D.②④⑥
难度: 中等查看答案及解析
-
在反应2SO2+O2
2SO3中,有a mol SO2和b mol O2参加反应,达到化学平衡状态时有c mol SO3生成,则SO2在平衡混合物中的体积分数为
A.
×100% B.
×100%
C.
×100% D.
%
难度: 中等查看答案及解析
-
下图是分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图。
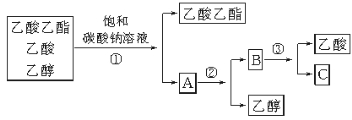
在上述实验过程中,所涉及的三次分离操作分别是
A.①蒸馏、②过滤、③分液 B.①分液、②蒸馏、③蒸馏
C.①蒸馏、②分液、③分液 D.①分液、②蒸馏、③结晶、过滤
难度: 中等查看答案及解析
-
正丁烷的二氯取代产物有几种
A.3种 B.4种 C.5种 D.6种
难度: 中等查看答案及解析
-
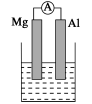
关于如图所示的原电池,下列说法正确的是
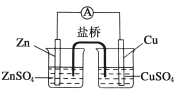
A. 锌电极发生还原反应,铜电极发生氧化反应
B.盐桥中的阴离子向硫酸铜溶液中迁移
C.电子从锌电极通过电流计流向铜电极
D.铜电极上发生的电极反应为2H++2e-===H2↑
难度: 中等查看答案及解析
-
几种短周期元素的原子半径及主要化合价如下表:
元素代号
X
Y
Z
W
原子半径/pm
160
143
70
66
主要化合价
+2
+3
+3、+5、-3
-2
下列叙述正确的是
A.X、Y元素的金属性 X<Y
B.一定条件下,Z单质与W的常见单质直接生成ZW2
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,W单质可以将Z单质从其氢化物中置换出来
难度: 中等查看答案及解析
-
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大。X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料。下列说法正确的是
A.Z与Y形成的化合物可作为耐高温材料
B.WY2能与碱反应,但不能与任何酸反应
C.原子半径按X、Y、Z、R、W的顺序依次增大
D.熔沸点:X2R>X2Y
难度: 中等查看答案及解析
-
下列方法中可以证明2HI(气)
H2(气)+I2(气)已达平衡状态的是
① 单位时间内生成n mol H2的同时生成n mol HI
② 一个H-H键断裂的同时有两个H-I键断裂
③温度和压强一定时混合气体密度不再变化
④ 反应速率υ(H2)=υ(I2)=0.5υ(HI)时
⑤ c(HI)=c(H2)=c(I2)=2:1:1
⑥ 温度和体积一定时,某一生成物浓度不再变化
⑦ 温度和体积一定时,容器内压强不再变化
⑧ 条件一定,混合气体的平均相对分子质量不再变化
⑨ 温度和体积一定时混合气体的颜色不再变化
A. ②③④⑤⑥ B. ②⑥⑦⑧⑨ C. ①②⑥⑧ D. ②⑥⑨
难度: 中等查看答案及解析
-
A、B分别为同一主族第三周期、第四周期的不同元素的原子,它们原子核内质子数均等于中子数。若A为ⅡA 族,其质量数为x,则B的质子数为Z;若A为ⅣA族,其质子数为y,则B的质量数为N。Z和N为下列哪一组值
A.Z:
+18,N:2y+18 B.Z:
+8, N:2y+18
C.Z:
+8, N:2y+36 D.Z:
+18, N:2y+36
难度: 中等查看答案及解析
-
丁烷有两种常见裂解方式,每种方式均分别生成一种烷烃和一种烯烃。若丁烷裂解率为90%,两种裂解方式生成的烯烃的质量相等,则裂解后所得混合气体中,相对分子质量最小的气体的体积分数约为
A. 19% B. 25% C. 36% D. 40%
难度: 中等查看答案及解析