-
化学与生活、生产密切相关,下列说法不正确的是
A. 用灼烧的方法可以区分蚕丝和人造纤维
B. 按照规定对生活废弃物进行分类放置有利于保护环境
C. 纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附
D. 光导纤维是无机非金属材料,合成纤维是有机高分子材料
难度: 简单查看答案及解析
-
NA为阿伏加德罗常数的值。下列说法正确的是
A. 1 mol H2和1 mol I2在加热条件下充分反应,生成HI的分子数为2NA
B. 10g质量分数为46%的乙醇溶液含有的氢原子数目为0.6NA
C. 20 mL 0.1 mol/L AlCl3溶液中,水解形成Al(OH)3胶体粒子数为0.002NA
D. 0.1molNa2O2和Na2O的混合物中含有的离子总数等于0.3NA
难度: 中等查看答案及解析
-
有机物W 在工业上常用作溶剂和香料,其合成方法如下:
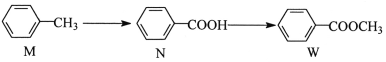
下列说法正确的是( )
A. M、N、W 均能发生加成反应、取代反应
B. N、W 组成上相差一个CH2原子团,所以互为同系物
C. W 属于酯类,能发生皂化反应
D. M 的二氯代物有8种
难度: 中等查看答案及解析
-
图中所示的装置图能够达到实验目的是( )
A.
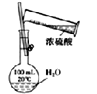 配制一定浓度的稀硫酸
配制一定浓度的稀硫酸B.
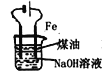 实验室制备Fe(OH)2
实验室制备Fe(OH)2C.
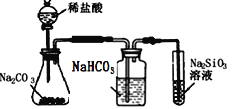 比较氯、碳、硅三种元素的非金属性强弱
比较氯、碳、硅三种元素的非金属性强弱D.
 加热熔融NaOH固体
加热熔融NaOH固体难度: 中等查看答案及解析
-
我国成功研制的一种新型可充放电AGDIB 电池(铝一石墨双离子电池)采用石墨、铝锂合金作为电极材料,以常规锂盐和碳酸酯溶剂为电解液。电池反应为CxPF6+LiyAl=Cx+LiPF6+Liy-1Al。放电过程如图,下列说法正确的是( )
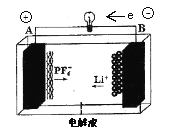
A. B为负极,放电时铝失电子
B. 电解液可以用常规锂盐和水代替
C. 充电时B 电极反应式为Cx+PF6--e-=CxPF6
D. 废旧AGDIB 电池“放电处理”时,若转移lmol 电子,石墨电极上可减轻7gLi
难度: 中等查看答案及解析
-
常温下,向浓度均为 0.1 mol∙L-1、体积均为 100 mL 的两种一元酸 HX、HY的溶液中,分别加入 NaOH,lg[c(H+)/c(OH-)]随加入 NaOH的物质的量的变化如图所示。下列说法正确的是
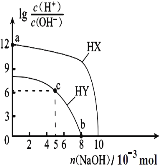
A. 常温下电离常数:HX<HY
B. a 点由水电离出的 c(H+)=10-12 mol∙L-1
C. c 点溶液中:c(Y-)>c(HY)
D. b 点时酸碱恰好完全中和
难度: 困难查看答案及解析
-
短周期主族元素X、Y、Z、W原子序数依次增大,原子序数之和为42,X原子的核外电子数等于Y的最外层电子数,Z是第IA元素,W是同周期非金属性最强的元素。下列说法正确的是
A. 单质的还原性:X>Z
B. 原子半径:r(X)<r(Y)<r(Z)<r(W)
C. Y、Z 组成的化合物中一定含有离子键
D. W的氧化物的水化物一定是强酸
难度: 中等查看答案及解析
 .
.