-
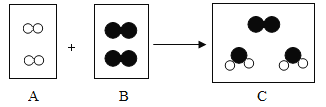
中华文明灿烂辉煌,在古代就有许多发明和创造。下列叙述中不涉及到化学变化的是 ( )
A. 烧制陶瓷 B. 制作石器 C. 粮食酿酒 D. 使用火药
难度: 简单查看答案及解析
-
在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表所示.关于此反应下列认识不正确的是( )
物质
甲
乙
丙
丁
反应前质量/g
1
20
15
2
反应后质量/g
m
29
0
8
A.m的值是1
B.甲可能是该反应的催化剂
C.该反应是分解反应
D.反应中乙、丁的质量比是29:8
难度: 中等查看答案及解析
-
下列实验基本操作正确的是( )
A.
 取用固体 B.
取用固体 B.  点燃酒精灯
点燃酒精灯C.
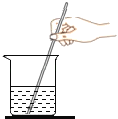 溶解固体 D.
溶解固体 D. 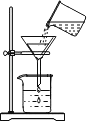 过滤
过滤难度: 简单查看答案及解析
-
海水是重要的资源,每千克海水中约含有钠10.62g、镁1.28g、钙0.40g等。这里的“钠、镁、钙”指的是( )
A.原子 B.分子 C.元素 D.单质
难度: 简单查看答案及解析
-
下列物质在氧气中燃烧,实验现象描述正确的是( )
A.木炭:产生绿色火焰 B.铁丝:发出耀眼的白光
C.镁带:火焰呈淡蓝色 D.硫粉:产生明亮的蓝紫色火焰
难度: 简单查看答案及解析
-
下列粒子结构示意图中,表示原子的是 ( )
A.
B.
C.
D.
难度: 简单查看答案及解析
-
从分子的角度分析并解释下列事实,说法不正确的是( )
序号
事实
解释
A
碘酒是混合物
由不同分子构械
B
端午节标飘香
分子在不断地运动
C
气体受热膨胀
温度升高,分子自身体积增大
D
碘受热升华
碘分子间的间隔增大
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
在化学反应前后,肯定不会变化的是( )
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的体积 ⑦物质的状态
A.②④⑤ B.①③④ C.①③④⑥ D.①③⑦
难度: 中等查看答案及解析
-
下列各图中“○”和“●”分别表示两种质子数不同的原子,其中能表示由两种化合物组成的混合物的图是( )
A.
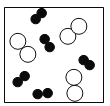 B.
B.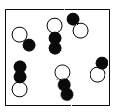 C.
C. D.
D.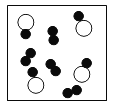
难度: 简单查看答案及解析
-
碳和一氧化碳都具有的化学性质是( )
①常温下都较稳定 ②都能在空气中燃烧 ③常温下都能与氧化铜反应 ④在一定的条件下都能夺取金属氧化物中氧 ⑤在反应中都表现出氧化性 ⑥在反应中都表现出还原性
A.②④⑥ B.①②④⑤ C.①②④⑥ D.①③④⑥
难度: 简单查看答案及解析