-
1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀,下列说法不正确的是
A. 该合金中铜与镁的物质的量之比是2 ︰1
B. 该浓硝酸中HNO3的物质的量浓度是14.0mol/L
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54沉淀时,加入NaOH溶液的体积是600mL
难度: 简单查看答案及解析
-
下列化学式与指定物质的主要成分对应正确的是
A. NaClO——漂白粉 B. NaHCO3——小苏打
C. CaCO3——熟石灰 D. KAl(SO4)2·12H2O——胆矾
难度: 中等查看答案及解析
-
我国晋代炼丹家葛洪所著《抱朴子》中记载有“丹砂烧之成水银”,其反应如下:HgS+O2=Hg+SO2。该反应属于
A. 置换反应 B. 复分解反应 C. 化合反应 D. 分解反应
难度: 简单查看答案及解析
-
2016年度国家最高科学技术奖获得者赵忠贤院士的主要贡献之一:发现液氮温区氧化物的超导电性。下列物质属于氧化物的是
A. O2 B. LiOH C. Cu2O D. NaHSO4
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是
A. 铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑
B. 氢氧化镁与硝酸溶液的反应:Mg(OH)2+2H+=Mg2++2H2O
C. 氯化钙溶液与碳酸钠溶液反应:Ca2++Na2CO3=CaCO3↓+2Na+
D. 硫酸铁溶液与足量铜的反应:2Fe3++3Cu=2Fe+3Cu2+
难度: 中等查看答案及解析
-
小王同学表演“桃花盛开”魔术时,将一个水槽倒扣在挂满潮湿白纸花的树枝上,白纸花逐渐变成粉红色,且越来越鲜艳。其奥秘是白纸花事先喷洒过酚酞溶液,而水槽内壁涂有
A. 浓盐酸 B. 浓硫酸 C. 浓烧碱 D. 浓氨水
难度: 简单查看答案及解析
-
2019年3月21日,江苏盐城天嘉宜化工有限公司化学储罐发生爆炸,因为涉事企业主要生产苯二胺及其系列产品,因此专家判断很可能是苯引起的爆炸,这次事件再一次为我们敲响了安全警钟。下列物质属于易燃液体的是
A. 高锰酸钾 B. 乙醇 C. 金属钠 D. 浓硫酸
难度: 简单查看答案及解析
-
下列自然资源的开发利用过程只涉及物理变化的是
A. 高炉炼铁 B. 海水晒盐 C. 水的电解 D. 粮食酿酒
难度: 中等查看答案及解析
-
下列气体既可用排水法收集,又可用向下排空气法收集的是
A. NO B. SO2 C. NH3 D. H2
难度: 简单查看答案及解析
-
根据海水中188O与168O的含量比可以推测古代海水的温度。188O与168O具有不同的
A. 中子数 B. 电子数 C. 质子数 D. 核电荷数
难度: 简单查看答案及解析
-
某溶液中含有大量的H+、NH4+、SO42-,该溶液中还可能大量存在的离子是
A. OH- B. HCO3- C. Ba2+ D. Mg2+
难度: 简单查看答案及解析
-
下列化学用语正确的是
A. 硫化氢的电子式:
B. 甲烷的分子式:C2H4O2
C. 铝离子的结构示意图:
 D. 硫酸钾的电离方程式:K2SO4=2K++SO4-2
D. 硫酸钾的电离方程式:K2SO4=2K++SO4-2难度: 中等查看答案及解析
-
2SO2+O2
2SO3是硫酸工业中的一个重要反应。下列关于该反应的说法正确的是
A. 使用催化剂能加快反应速率 B. 降低温度不能改变反应速率
C. 提高O2浓度能降低反应速率 D. SO2和O2能100%转化为SO3
难度: 中等查看答案及解析
-
下列属于只含共价键的化合物的是
A. N2 B. Na2O2 C. CO2 D. MgCl2
难度: 中等查看答案及解析
-
氯化溴(BrCl)化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,跟水反应的化学方程式为:BrCl+H2O=HCl+HBrO。下列有关BrCl的说法错误的是
A. BrCl具有较强的氧化性
B. 和NaOH溶液反应生成NaCl和NaBrO
C. 它能使湿润的淀粉碘化钾试纸变蓝
D. 与水反应时BrCl既是氧化剂又是还原剂
难度: 中等查看答案及解析
-
粗略测定草木灰中碳酸钾的含量并检验钾元素的存在,需经过称量、溶解、过滤、蒸发、焰色反应等操作。下列图示对应的操作规范的是
A. 称量
 B. 溶解
B. 溶解C. 蒸发
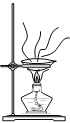 D. 焰色反应
D. 焰色反应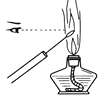
难度: 中等查看答案及解析
-
下列实验方法能达到目的的是
A. 用丁达尔效应鉴别Al(OH)3胶体和NaHSO4溶液
B. 用过滤的方法分离四氯化碳和水的混合物
C. 用Na2CO3溶液除去CO2中混有的少量HCl
D. 用KSCN溶液检验FeCl3溶液中是否含有Fe2+
难度: 中等查看答案及解析
-
下列选项中描述的过程能实现热能转化为化学能的是
A. 燃料电池
 B. 火力发电
B. 火力发电 C. 可燃冰燃烧
C. 可燃冰燃烧 D. 煅烧石灰石
D. 煅烧石灰石
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列说法正确的是
A. 1 mol N2含有的N原子数为2NA
B. 27 g Al变为Al3+时失去的电子数为NA
C. 1 L 1 mol·L-1MgCl2溶液中含有的Cl-数为NA
D. 常温常压下,11.2 L CO2中含有的原子数为1.5NA
难度: 中等查看答案及解析
-
下列有关物质用途的说法正确的是
A. 氢氧化钙可用来治疗胃酸过多 B. 活性炭可用作水处理时的杀菌剂
C. 铝制容器可用来储运浓硝酸 D. 氧化钠可用作潜水艇里氧气的来源
难度: 中等查看答案及解析
-
以海水为电解质的Mg-AgCl电池在军事上可用作电动鱼雷的电源,其电池反应的离子方程式为:2AgCl+Mg=Mg2++2Ag+2Cl-。该电池工作时,下列说法正确的是

A. 海水中的NaCl被氧化
B. Mg电极发生还原反应
C. 电流由Mg经外电路流向AgCl
D. 正极反应为AgCl+e-=Ag+Cl-
难度: 中等查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大。X的最高正价和最低负价代数和为零,Y、Z、W位于同一周期,Y的三价阳离子与氖原子具有相同的核外电子排布,Z与X位于同一主族, W的最外层电子数等于Y、Z最外层电子数之和。下列说法正确的是
A. 原子半径:r(W)>r(Y)>r(Z)>r(X)
B. Y、W的最高价氧化物对应的水化物能相互反应
C. Z的氧化物是制造太阳能电池板的主要材料
D. Z的简单气态氢化物的稳定性比X的强
难度: 中等查看答案及解析