-
随着人们生活质量的提高,废电池必须进行集中处理的问题提到议事日程,其主要原因是
A. 利用电池外壳的金属材料
B. 防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C. 不使电池中渗泄的电解液腐蚀其他物品
D. 回收其中石墨电极
难度: 中等查看答案及解析
-
关于铜锌稀硫酸原电池装置的叙述中,正确的是( )
A. 铜是阳极,铜片上有气泡产生 B. 铜片质量逐渐减少
C. 电流从锌片经导线流向铜片 D. 氢离子在铜片表面被还原
难度: 简单查看答案及解析
-
某原电池总反应离子方程式为:2Fe3++Fe = 3Fe2+,能实现该反应的原电池是( )
A. 正极为Cu,负极为Fe,电解质溶液为FeCl2
B. 正极为C,负极为Fe,电解质溶液为Fe(NO3)3
C. 正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3
D. 正极为Ag,负极为Fe,电解质溶液为CuSO4
难度: 中等查看答案及解析
-
如图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是( )
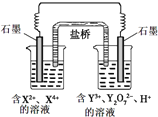
A. 左池电极反应式:X4+ + 2e- = X2+
B. 每消耗1mol Y2O72-,转移3mol电子
C. 左池中阴离子数目增加
D. 盐桥中阴离子移向右池
难度: 中等查看答案及解析
-
锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。某种锂电池的总反应式是Li+MnO2 = LiMnO2。下列说法正确的是( )
A. Li是负极,电极反应为Li-e-=Li+
B. Li是正极,电极反应为Li+e-=Li-
C. MnO2是负极,电极反应为MnO2+e-=MnO2-
D. Li是负极,电极反应为Li-2e-=Li2+
难度: 简单查看答案及解析
-
某同学将电解池工作时电子、离子流动方向及电极种类等信息表示在如图中,下列有关分析完全正确的是( )
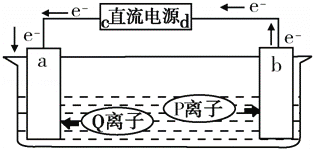
选项
A
B
C
D
a电极
阳极
阴极
阳极
阴极
d电极
正极
正极
负极
负极
Q离子
阳离子
阳离子
阴离子
阴离子
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
如图为用直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊溶液。下列实验现象中正确的是
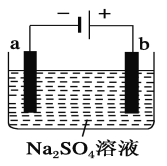
A. 逸出气体的体积,a电极的小于b电极的
B. 一电极逸出无味气体,另一电极逸出刺激性气味气体
C. a电极附近呈红色,b电极附近呈蓝色
D. a电极附近呈蓝色,b电极附近呈红色
难度: 中等查看答案及解析
-
根据下列实验事实:
(1)X+Y2+=X2++Y;(2)Z+2H2O
Z(OH)2+H2↑;(3)Z2+离子的放电能力比X2+弱;(4)由Y、W 作电极组成的原电池反应为:Y-2e-=Y2+,由此可知,X、Y、Z、W的还原性由强到弱的顺序是
A. X > Y > Z > W B. Y > X > W > Z
C. Z > X > Y > W D. Z > Y > X > W
难度: 中等查看答案及解析
-
金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是( )(已知:氧化性Fe2+<Ni2+<Cu2+)
A. 阳极发生还原反应,其电极反应式:Ni2++2e-=Ni
B. 电解质溶液为镍盐,电解过程中溶液的浓度不变
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 电解后,电解槽底部的阳极泥中只有Cu和Pt
难度: 中等查看答案及解析
-
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做 ( )
A. 阴极 B. 阳极 C. 正极 D. 负极
难度: 简单查看答案及解析
-
关于下列各装置图的叙述中不正确的是( )
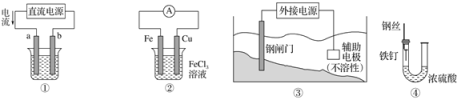
A. 用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B. 装置②的总反应是Cu+2Fe3+===Cu2++2Fe2+
C. 装置③中钢闸门应与外接电源的负极相连
D. 装置④中的铁钉几乎没被腐蚀
难度: 中等查看答案及解析
-
下列各容器中盛有海水,铁在其中被腐蚀时,由快到慢的顺序是( )
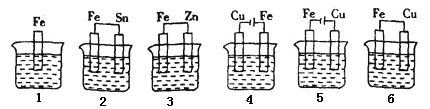
A. 4>2>1>3>5>6
B. 5>4>2>3>1>6
C. 4>6>2>1>3>5
D. 6>3>5>2>4>1
难度: 中等查看答案及解析
-
利用下图装置,可以模拟铁的电化学防护。下列说法正确的是( )
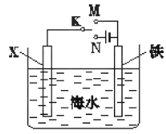
A. 若X为碳棒,为减缓铁的腐蚀,开关K应该置于M处
B. 若X为锌,开关K置于M处,该电化学防护法称为牺牲阳极的阴极保护法
C. 若X为碳棒,K与M连接时,一段时间后溶液的pH减小
D. 若X为锌,K与N连接时,X电极产生气泡
难度: 中等查看答案及解析
-
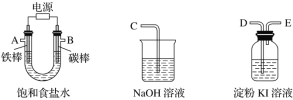
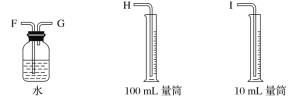
在通风橱中进行下列实验:
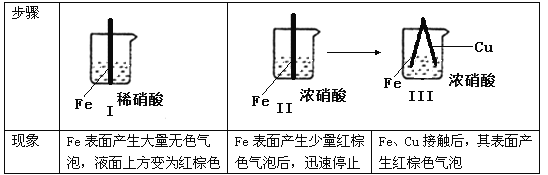
下列说法中不正确的是:
A. Ⅰ种气体有无色变红棕色的化学方程式为:2NO+O2=2NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
难度: 中等查看答案及解析
-
利用如图所示原电池可测量空气中Cl2含量,其中电解质是Ag+可以自由移动的固体物质。下列分析不正确的是( )
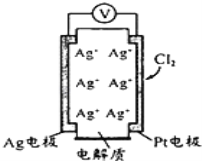
A. 电子经外电路流向Pt电极
B. 电池工作时,电解质中Ag+数目减少
C. 正极反应:C12+2e﹣+2Ag+=2AgCl
D. 空气中c(C12)越大,Ag极消耗速率越快
难度: 中等查看答案及解析
-
用惰性电极电解M(NO3)x的水溶液,当阴极增重a g时,在阳极上产生了b L气体(标况),则M的相对分子质量为( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
电浮选凝聚法处理酸性污水的工作原理如图所示,下列说法不正确是( )
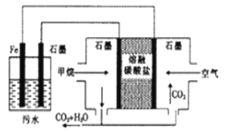
A. 铁电极的电极反应式为Fe-2e-=Fe2+
B. 通入甲烷的石墨的电极反应式为:CH4+4CO32-—8e- ==5CO2+2H2O
C. 为了增强的污水的导电能力,可向污水中加入适量食盐
D. 若左池石墨电极产生44.8L气体,则消耗0.5mol甲烷
难度: 困难查看答案及解析
-
将含有0.4 mol Cu(NO3)2和0.4 mol KCl的水溶液1 L,用惰性电极电解一段时间后,在一电极上析出19.2 g Cu;此时,在另一电极上放出气体的体积在标准状况下为(不考虑产生的气体在水中的溶解)( )
A. 3.36 L B. 5.6 L C. 6.72 L D. 13.44 L
难度: 中等查看答案及解析
-
下列有关金属腐蚀的说法中正确的是
①金属的腐蚀全部是氧化还原反应
②金属的腐蚀可分为化学腐蚀和电化学腐蚀,只有电化学腐蚀才是氧化还原反应
③因为二氧化碳普遍存在,所以钢铁的电化学腐蚀以析氢腐蚀为主
④无论是析氢腐蚀还是吸氧腐蚀,总是金属被氧化
A.①③ B.②③ C.①④ D.①③④
难度: 中等查看答案及解析
-
Cu2O是一种半导体材料,基于绿色化学理论设计的制取Cu2O的电解池示意图如图,电解总反应为2Cu+H2O
Cu2O+H2↑。下列说法正确的是( )
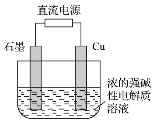
A. 石墨电极上产生氢气
B. 铜电极发生还原反应
C. 铜电极接直流电源的负极
D. 当有0.1 mol电子转移时,有0.1 mol Cu2O生成
难度: 中等查看答案及解析
-
以氨气代替氢气来研发氨燃料电池是当前科研的一个热点,氨燃料电池使用的电解质溶液是KOH溶液,电池反应为4NH3+3O2
2N2+6H2O。下列有关说法错误的是( )
A. 燃料电池的能量转化率一般比普通的电池高
B. 氨燃料电池在放电时,负极反应为2NH3-6e-+6OH-===N2+6H2O
C. 以氨气代替氢气的主要原因是氨气易液化、易储存
D. 氨燃料电池在充电时,在阴极N2得电子被氧化
难度: 中等查看答案及解析
-
控制适合的条件,将反应
设计成如右图所示的原电池。下列判断不正确的是
A. 反应开始时,乙中石墨电极上发生氧化反应
B. 反应开始时,甲中石墨电极上Fe3+被还原
C. 电流计读数为零时,反应达到化学平衡状态
D. 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极
难度: 中等查看答案及解析
-
下列关于铁制品保护措施的说法中不正确的有
A. 在自行车钢圈上镀上一层金属铬,摩擦部位加上机油或黄油
B. 在海轮的外壳上常焊有锌块,且定期更新
C. 相同条件下,马口铁(表层镀锡)与白铁(表层镀锌)相比,马口铁更为耐用
D. 在钢铁中加入锰、铬等金属,以改变钢铁结构起到保护作用
难度: 中等查看答案及解析
-
下列有机物中,不属于烃的衍生物的是
A.
B. CH3CH2NO2
C. CH2=CHBr D. CH3—CH3
难度: 简单查看答案及解析
-
下列有机化合物属于链状化合物,且含有两种官能团的是
A.
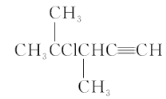 B.
B. 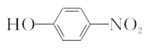
C.
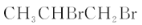 D.
D. 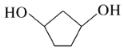
难度: 简单查看答案及解析