-
化学在生产生活中应用广泛,下列过程中发生化学变化的是()
A.
 干冰升华
干冰升华B.
 可燃冰燃烧
可燃冰燃烧C.
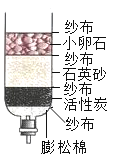 简易装置净水
简易装置净水D.
 制取蒸馏水
制取蒸馏水难度: 简单查看答案及解析
-
在2018年政府工作报告中李克强总理提出:我们要携手行动,建设天蓝、地绿、水清的美丽中国,下列措施不符合政府要求的是( )
A.积极推进新能源汽车的使用
B.合理使用化肥农药
C.减少使用煤等传统燃料
D.农作物秸秆就地焚烧做肥科
难度: 简单查看答案及解析
-
乳酸亚铁可用于治疗缺铁性贫血。已知乳酸亚铁的化学式为C6H10FeO6,下列关于乳酸亚铁说法正确的是
A.由三种非金属和一种金属组成
B.属于氧化物
C.组成元素中,铁元素质量分数最大
D.C6H10FeO6中C、O的质量比为3:4
难度: 中等查看答案及解析
-
下列实验操作错误的是( )
A.
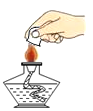 熄灭酒精灯
熄灭酒精灯B.
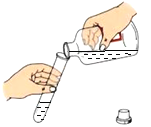 倾倒液体
倾倒液体C.
滴加液体
D.
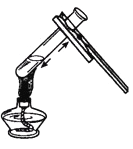 加热液体
加热液体难度: 简单查看答案及解析
-
元素周期表是学习和研究化学的重要工具,根据下列图示其说法错误的是()
A.氮元素和氧元素属于同一周期
B.氧元素的质子数是8
C.硫元素的相对原子质量为32.06g
D.三种元素均为非金属元素
难度: 简单查看答案及解析
-
水是生命之源,下列有关水的叙述不正确的是()
A.水的天然循环是通过其三态变化实现的
B.水是由氢气和氧气组成的
C.电解水时负极产生的是氢气
D.城市污水应该经过净化处理后再排放
难度: 简单查看答案及解析
-
在负载型钯基催化剂的作用下,通过氢气和氧气直接合成H2O2,其不仅原子利用率高、耗能低,而且副产物只生成水,其反应微观示意图如下,下列有关该反应的说法正确是( )

A.该反应属于化合反应
B.负载型钯基在反应前后化学性质发生变化
C.化学反应前后分子种类保持不变
D.该反应符合绿色化学理念
难度: 中等查看答案及解析
-
分类法是化学习中常用的方法之,下列概念符合图示关系的是( )

A
B
C
D
氧化物
氧化反应
纯净物
化合反应
化合物
化合反应
混合物
置换反应
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
从“特殊推向一般”是学习化学的种方法,下列推理正确的是( )
编号
特殊结论
一般结论
A
单质是由一种元素组成
由一种元素组成的物质一定是单质
B
氢气点燃前需验纯
可燃性气体点燃前都需验纯
C
CO2能使石蕊溶液变红
非金属氧化物都能使石蕊溶液变红
D
分子、原子是不是电性微粒
所有的微粒都不显电性
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
比较法是学习初中化学的一种方法。下列是初中化学课本中出现的重要实验,其中没有体现对比法的是
A.
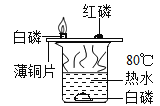 燃烧条件探究
燃烧条件探究B.
石蕊溶液变红
C.
 肥皂水区别硬水和软水
肥皂水区别硬水和软水D.
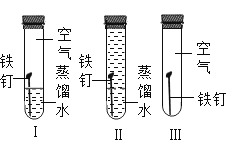 铁钉绣蚀
铁钉绣蚀难度: 中等查看答案及解析