-
在空气中长时间放置少量金属钠,最终产物是
A. Na2CO3 B. NaOH C. Na2O D. Na2O2
难度: 简单查看答案及解析
-
将钠、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积比是( )
A. 1∶2∶3 B. 6∶3∶2 C. 3∶1∶1 D. 1∶1∶1
难度: 困难查看答案及解析
-
将一小块钠投入盛50mL澄清饱和石灰水的烧杯里,不可能观察到的现象是( )
A. 钠熔成小球并在液面上游动 B. 有气体生成
C. 溶液底部有银白色物质生成 D. 溶液变浑浊
难度: 简单查看答案及解析
-
已知氧化性强弱顺序:Cl2> Br2> Fe3+>I2。下列反应不能发生的是( )
A. Br2+2I-= I2+2 Br- B. 2FeCl2+Cl2 = 2FeCl3
C. 2FeCl2+2HCl+I2 = 2FeCl3+2HI D. 2Fe3+ + 2I-= 2Fe2+ + I2
难度: 中等查看答案及解析
-
在实验室中,通常将金属钠保存在( )
A. 水中 B. 煤油中 C. 四氯化碳中 D. 汽油中
难度: 中等查看答案及解析
-
已知①中盛有一定量的碳酸钠溶液, 根据下图所示的实验过程,下列说法正确的是( )
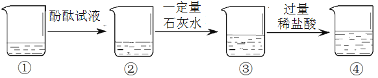
A. ②中溶液为无色
B. ③中溶液的溶质组成有2种情况
C. ④中溶液的溶质除酚酞外,还有3种
D. 加入过量稀盐酸后,③中只观察到沉淀消失,产生大量气泡
难度: 困难查看答案及解析
-
下列离子方程式正确的是( )
A. 石灰乳与过量碳酸氢钙溶液反应:HCO3—+Ca2++OH-==CaCO3↓+H2O
B. 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O(沸水)
Fe(OH)3(胶体)+3H+
C. 二氧化碳通入足量的氢氧化钠溶液:CO2 + OH-═ HCO3-
D. 氧化钠与盐酸反应:O2-+2H+ ==== H2O
难度: 中等查看答案及解析
-
下列各组离子中能大量共存,溶液呈现无色,且加入一小块钠后仍然能大量共存的是
A. K+、MnO4—、SO42—、H+ B. Ba2+、Na+、HCO3—、NO3—
C. Na+、NO3—、K+、Cl− D. Ca2+、NO3—、Cl−、CO32—
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
A. 28g以任意比组成的CO与N2混合气体中含有原子数为2NA
B. 将100mL0.1mol/L的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01 NA
C. 在H2O2 + Cl2 =2HCl + O2反应中,每生成32g氧气,则转移4NA个电子
D. 1L 1 mol/L 的盐酸中有NA 个HCl分子
难度: 中等查看答案及解析
-
一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3
2HNO3+4N2+9H2O,在反应中被氧化与被还原的氮原子数之比为
A. 5∶3 B. 5∶4 C. 1∶1 D. 3∶5
难度: 中等查看答案及解析
-
如果Fe3+、SO42-、Al3+和M四种离子以物质的量之比为2∶4∶1∶1共同存在于同一种溶液中,那么M可能是( )
A. Na+ B. OH- C. CO32- D. Cl-
难度: 简单查看答案及解析
-
常温常压下,用等质量的H2、CO、NH3、H2S分别吹出四个气球,其中气体为CO的是
A.
B.
C.
D.

难度: 中等查看答案及解析
-
下列变化中,必须加入还原剂才可以实现的是( )
A. KC1O3→KC1 B. CO→CO2 C. Fe2(SO4)3→FeSO4 D. Na2O2→NaOH
难度: 中等查看答案及解析
-
下列物质既能与烧碱溶液反应,又能与盐酸溶液反应的是( )
A. Na2O B. Na2CO3 C. NaOH D. NaHCO3
难度: 简单查看答案及解析
-
用0.3molNa2SO3恰好被0.1 mol氧化剂X2O72-氧化生成Na2SO4,则元素X在还原产物中的化合价是
A.+6 B.+3 C.+2 D.0
难度: 困难查看答案及解析
-
以下说法不正确的是( )
A. 常温下,在水中的溶解性:NaHCO3<Na2CO3
B. 等物质的量的Na2CO3、NaHCO3分别与足量盐酸反应产生的CO2质量相同
C. 铝箔加热至熔化,但熔化的铝并不滴落,原因是氧化铝的熔点比铝熔点高
D. 在实验室里,常用铝盐溶液与强碱溶液反应来制取氢氧化铝
难度: 简单查看答案及解析
-
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合溶液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )
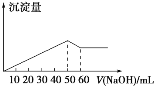
A. 6∶1 B. 3∶1 C. 2∶1 D. 1∶2
难度: 困难查看答案及解析