-
分类法在化学学科的发展中起了非常重要的作用,下列分类标准合理的是( )
A.根据水溶液是否能够导电将化合物分为电解质和非电解质
B.根据分散系是否有丁达尔现象将分散系分为溶液、胶体和浊液
C.根据氧化物的组成元素将氧化物分成酸性氧化物、碱性氧化物等
D.根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
难度: 简单查看答案及解析
-
下列各组离子在水溶液中能大量共存的是( )
A.酸性溶液中:K+、NO3﹣、Cl﹣、CO32﹣
B.澄清透明的溶液中:Na+、K+、MnO4﹣、AlO2﹣
C.在含大量Fe3+的溶液中:NH4+、Na+、Cl﹣、SCN﹣
D.能与金属铝反应放出H2的溶液:HCO3﹣、Na+、Mg2+、SO42﹣
难度: 简单查看答案及解析
-
科学史上每一次重大发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于( )
A.发现了元素周期律 B.提出了原子分子学说
C.揭示了燃烧的本质 D.提取了治疟药物青蒿素
难度: 简单查看答案及解析
-
下列常见物质的俗名与化学式对应正确的是( )
A.铜绿﹣CuSO4•5H2O
B.明矾一KAl(SO4)2•12H2O
C.苏打一 NaHCO3
D.铁红一Fe3O4
难度: 简单查看答案及解析
-
中国寓言故事蕴味深长。下列寓言的标题所表述的过程中包含化学变化的是
A.破釜沉舟 B.煮豆燃萁 C.刻舟求剑 D.愚公移山
难度: 中等查看答案及解析
-
用化学用语表示2Na+2H2O═2NaOH+H2↑中的相关微粒,其中正确的是( )
A.H2O的电子式:
B.中子数为10的氧原子:
O
C.Na+的结构示意图:
D.NaOH的电离方程式:NaOH═Na++O2﹣+H+
难度: 简单查看答案及解析
-
从海带中制取单质碘需要经过灼烧、溶解、过滤、氧化、萃取、分液、蒸馏等操作。下列图示对应的装置合理、操作规范的是
A.灼烧
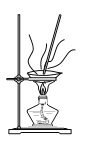 B.过滤
B.过滤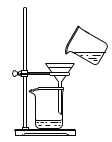
C.分液
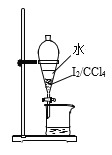 D.蒸馏
D.蒸馏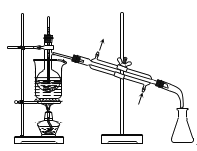
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.1mol钠离子所含电子数为10NA
B.常温常压下,22.4LCO2含有的分子数为NA
C.5.6g铁粉与足量稀硫酸反应转移电子数为0.3NA
D.常温下,1mol•L﹣1的Na2CO3溶液中含有Na+个数为2NA
难度: 简单查看答案及解析
-
元素的原子结构决定其性质和在元素周期表中的位置,下列说法正确的是( )
A.同一主族从上往下原子半径逐渐增大
B.氯化氢和氯化钠溶于水需克服相同类型的作用力
C.元素的最外层电子数一定等于元素的最高化合价
D.元素周期表中位于金属和非金属交界线附近的元素为过渡元素
难度: 简单查看答案及解析
-
根据下列实验操作和现象所得出的结论正确的是( )
选项
实验操作和现象
结论
A
向CuSO4溶液中加入铁粉,有红色固体析出
氧化性:Fe2+>Cu2+
B
在酒精灯上加热铝箔,铝箔熔化,熔化的铝并不滴落
熔点:氧化铝>铝
C
取等物质的量的Al和Fe分别与足量的盐酸反应,Al产生的氢气多
金属性:Al>Fe
D
将稀盐酸滴入碳酸钠溶液中,充分振荡,产生大量气泡
非金属性:Cl>C
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
下列有关物质性质与用途具有对应关系的是( )
A.Al2O3是两性氧化物,可用作耐高温材料
B.FeCl3溶液显酸性,可用于蚀刻铜制的电路板
C.CO2密度比空气大,可用作镁着火时的灭火剂
D.Mg(OH)2分解时吸收大量的热,可用作阻燃剂
难度: 简单查看答案及解析
-
关于反应2Na2O2+2H2O═4NaOH+O2的说法不正确的是( )
A.H2O和O2都是共价化合物
B.H2O和NaOH均含极性键
C.Na2O2和O2均含非极性健
D.Na2O2和NaOH都是离子化合物
难度: 简单查看答案及解析
-
用下列装置进行有关实验不能达到预期目的的是( )
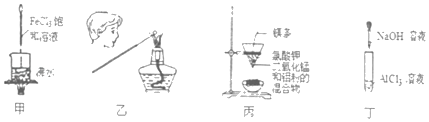
A.用甲装置可制得Fe(OH)3胶体
B.用乙装置确定所蘸取的物质中含有钾元素
C.用丙装置制少量金属锰
D.用丁装置观察Al(OH)3能溶于NaOH溶液中
难度: 简单查看答案及解析
-
Fe2(SO4)3溶液可除去煤中以黄铁矿[二硫化亚铁(FeS2)形式存在的硫元素,反应如下:7Fe2(SO4)3+FeS2+8H2O═15FeSO4+8H2SO4,下列说法不正确的是( )
A.该反应中Fe2(SO4)3为氧化剂
B.反应中每生成15 mol FeSO4转移15mol电子
C.滴加KSCN溶液可检验上述反应中Fe2(SO4)3是否消耗完
D.反应后的溶液中通入空气就能达到使Fe2(SO4)3再生的目的
难度: 简单查看答案及解析
-
实验室有一包白色固体,可能含有Na2CO3、NaHCO3和NaCl中的一种或多种。下列根据实验事实得出的结论正确的是( )
选项
实验操作和现象
结论
A
取一定量固体溶解,向溶液中通入足量的CO,观察到有晶体析出
原固体中一定含Na2CO3
B
取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成
原固体中一定含有Na2CO3
C
取一定量固体,溶解,向溶液中滴加适量AgNO3 溶液,观察有白色沉淀生成
原固体中一定含有NaCl
D
称取3.80g固体,加热至恒重,质量减少了0.620g。用足量稀盐酸溶解残留固体,充分反应后,收集到有0.88g气体
原固体中三种物质都有
A.A B.B C.C D.D
难度: 中等查看答案及解析