-
实验室制取气体选择收集方法时,下列气体性质不需考虑的是
A. 密度 B. 可燃性 C. 溶解性 D. 能否与水反应
难度: 中等查看答案及解析
-
下列实验现象,描述错误的是
A. 电解水时正极和负极产生气体的体积比为2:1
B. 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
C. 将一氧化碳通入灼热的氧化铁,红色粉末逐渐变为黑色粉末
D. 向硫酸铜溶液中滴加氢氧化钠溶液,产生蓝色沉淀
难度: 中等查看答案及解析
-
我国女科学家屠呦呦因发现青蒿素荣获2015年诺贝尔生理学或医学奖。青蒿素(C15H22O5)是一种用于治疗疟疾的药物。下列有关青蒿素的叙述正确的是( )
A. 从宏观上看:青蒿素分子由碳、氢、氧三种元素组成
B. 从微观上看:青蒿素中含有15个碳原子、22个氢原子和5个氧原子
C. 从变化上看:青蒿素在氧气中完全燃烧生成一氧化碳和水
D. 从质量上看:青蒿素中碳、氧元素的质量比为9:4
难度: 中等查看答案及解析
-
下列物质存放在烧杯中一段时间后,质量变小且不变质的是( )
A.烧碱 B.浓硫酸 C.浓盐酸 D.生石灰
难度: 中等查看答案及解析
-
下列物质由离子直接构成的是( )
A. 铜 B. 氧气 C. 水 D. 氯化钾
难度: 中等查看答案及解析
-
下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
A.
 B.
B.C.
D.
难度: 中等查看答案及解析
-
正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是( )
A.
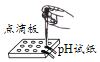 测定溶液pH B.
测定溶液pH B.配制溶液
C.
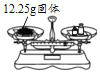 称量固体 D.
称量固体 D.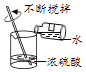 稀释浓硫酸
稀释浓硫酸难度: 中等查看答案及解析
-
我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如下图所示,下列说法正确的是( )
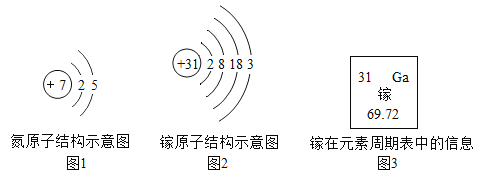
A.镓元素位于第三周期,属于金属元素 B.镓原子核内有31个中子
C.镓的相对原子质量是69.72g D.氮化镓的化学式为GaN
难度: 中等查看答案及解析
-
下列数据为常见水果的pH,其中酸性最强的是
A.
 柠檬pH(2~3) B.
柠檬pH(2~3) B. 橙子pH(3~4) C.
橙子pH(3~4) C. 西红柿pH(4~5) D.
西红柿pH(4~5) D. 西瓜pH(5~6)
西瓜pH(5~6)难度: 简单查看答案及解析
-
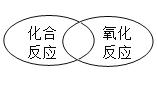
硅是信息技术的关键材料。从石英砂制取芯片的重要反应是SO2+2C
Si+2CO↑,该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
难度: 简单查看答案及解析
-
化学科学的发展为人类提供了更多的生活、生产资料,下面做法利用了物理变化的是( )
A.煤的焦化、气化、液化 B.用石灰浆涂抹墙壁后,表面有水珠生成
C.大棚蔬菜生产施用二氧化碳气体提高产量 D.海员蒸馏海水获取淡水
难度: 中等查看答案及解析
-
类推是一种重要的学习方法,但如果不具体问题具体分析就会产生错误的结论。下列类推结论错误的是( )
①CO能与Fe2O3反应生成Fe,CO也能与CuO反应生成Cu
②NaOH溶液能使无色酚酞试液变红色,Cu(OH)2也能使无色酚酞试液变红色
③碱的溶液呈碱性,则呈碱性的溶液一定是碱的溶液
④中和反应生成盐和水,但生成盐和水的反应不一定是中和反应
⑤活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属
A.②③⑤ B.①② C.③⑤ D.③④
难度: 困难查看答案及解析
-
下列选项中物质的俗名、化学式、类别、用途完全对应的是( )
A.纯碱 Na2CO3碱、制玻璃
B.生石灰 CaO氧化物、补钙剂
C.食盐 NaCl盐、除铁锈
D.火碱 NaOH碱、生产橡胶
难度: 中等查看答案及解析
-
通过观察下列实验现象,不能达到实验目的是( )
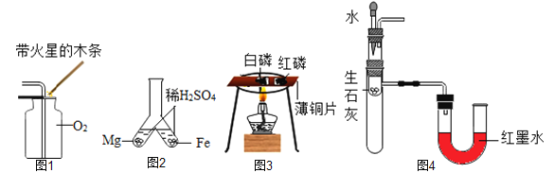
A.图1:收集氧气时,氧气的验满
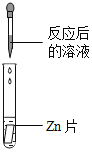
B.图2:比较镁与铁的金属活动性
C.图3:验证白磷的着火点低于红磷
D.图4:验证生石灰与水反应放热
难度: 中等查看答案及解析
-
现有a、b、c、d四种无色溶液,分别是碳酸钾溶液、硫酸溶液、氯化钡溶液、盐酸中的一种。两两混合后出现下图所示的现象,请确定a、b、c、d分别是
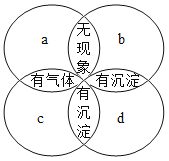
A.硫酸溶液、碳酸钾溶液、氯化钡溶液、盐酸
B.氯化钡溶液、盐酸、碳酸钾溶液、硫酸溶液
C.碳酸钾溶液、硫酸溶液、盐酸、氯化钡溶液
D.盐酸、硫酸溶液、碳酸钾溶液、氯化钡溶液
难度: 中等查看答案及解析
-
某化学兴趣小组对A、B、C、D四种未知溶液的成分进行了检验,检验结果见下表。其中检验结果不正确的是( )
组别
溶液中检验出的离子
A
K+、Na+、OH-、SO42-
B
Ba2+、Na+、Cl-、OH-
C
Cu2+、Mg2+、NO3-、Cl-
D
H+、NH4+、CO32-、SO42-
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
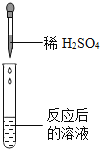
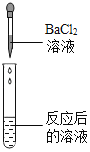
某化学兴趣小组利用如图装置进行实验:打开弹簧夹,将液体a滴入试管①中与固体b接触,若试管②中的导管口没有气泡产生,则液体a和固体b的组合可能是( )
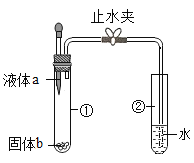
A.水和生石灰
B.稀盐酸和碳酸钠
C.水和硝酸铵
D.过氧化氢溶液和二氧化锰
难度: 中等查看答案及解析
-
现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价)。下列说法中不正确的是( )

A.生成氢气的质量:甲>乙>丙
B.相对原子质量:乙>丙>甲
C.金属活动性:乙>甲>丙
D.消耗硫酸的质量:甲>乙>丙
难度: 困难查看答案及解析
-
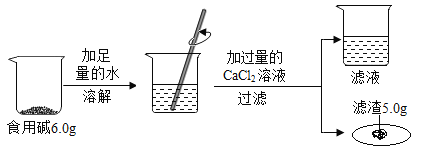
除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( )
选项
物质
选用试剂
操作方法
A
Fe2O3(Fe)
盐酸
浸泡、过滤、洗涤、烘干
B
CO(CO2)
NaOH溶液、浓硫酸
洗气、干燥
C
CaO(CaCO3)
水
过滤、烘干
D
NaCl(Na2CO3)
Ca(NO3)2溶液
溶解、过滤、蒸发、结晶
A.A B.B C.C D.D
难度: 中等查看答案及解析
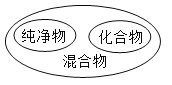 B.
B.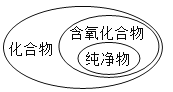 C.
C.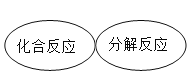 D.
D.