-
下列说法中正确的是
A. H2SO4的摩尔质量是98 g B. 1 mol H2O的质量是18 g/mol
C. 1 mol N2的体积是22.4 L D. Cl-的摩尔质量是35.5 g/mol
难度: 简单查看答案及解析
-
工业生产和日常生活中,如何减少二氧化碳排放已成为全世界关注的热点,低碳经济和低碳生活成为热门话题。以下做法与低碳要求不相适应的是
A.尽量不使用一次性竹、木筷子
B.多挖煤,多发电,加快经济发展
C.利用特殊材料建屋顶、墙面,充分利用太阳光照明
D.提倡骑自行车、乘公交车出行
难度: 简单查看答案及解析
-
下列物质的分类正确的是( )
碱
酸
盐
碱性氧化物
酸性氧化物
A
Na2CO3
H2SO4
Cu2(OH)2CO3
Fe2O3
SO3
B
NaOH
HCl
NaCl
Na2O
NO2
C
NaOH
NaHSO4
CaF2
MgO
SO2
D
KOH
HNO3
NaHCO3
CaO
CO2
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列类型的反应一定属于氧化还原反应的是
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
难度: 简单查看答案及解析
-
当光束通过蛋白质溶液时,可产生丁达尔效应,表明蛋白质溶液属于 ( )
A.纯净物 B.溶液 C.胶体 D.浊液
难度: 简单查看答案及解析
-
下列实验操作中,不能用于物质分离的是( )
A.
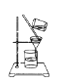 B.
B.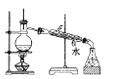
C.
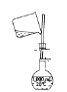 D.
D.
难度: 简单查看答案及解析
-
设阿伏加德罗常数的值为NA,则下列说法正确的是( )
A.常温常压下,11.2LCH4中含有的氢原子数等于2NA
B.标况下1molH2O的体积为22.4L
C.1mol Fe与足量盐酸充分反应失去电子数为3NA
D.1L 1mol·L-1K2CO3溶液中所含K+个数为2NA
难度: 简单查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是
A.NO3―、Ag+、H+、Cl― B.CO32―、Na+、Ca2+、NO3―
C.Mg2+、Cl―、OH―、CH3COO― D.Mg2+、SO42―、K+、Cl―
难度: 简单查看答案及解析
-
下列溶液中与50 mL 1 mol·L-1的FeCl3溶液中氯离子浓度相等的是( )
A.100 mL 3 mol·L-1 的KClO3 B.75 mL 2 mol·L-1 的NH4Cl
C.125 mL 2 mol·L-1 的CaCl2 D.150 mL 3 mol·L-1 的NaCl
难度: 简单查看答案及解析
-
下列物质无法通过单质直接化合生成的是 ( )
A.FeCl2 B.CO C.MgCl2 D.Al2O3
难度: 简单查看答案及解析
-
关于
的说法正确的是
A. 质量数为6 B. 质子数为6 C. 电子数为13 D. 中子数为6
难度: 简单查看答案及解析
-
对于某些离子的检验及结论一定正确的是( )
A. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42—
B. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32—
C. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
D. 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
难度: 中等查看答案及解析
-
下列反应的离子方程式正确的是( )
A.过氧化钠与水反应:2O22-+2H2O=O2↑+4OH-
B.NaHCO3溶液与盐酸溶液共热:HCO3- + H+ == H2O + CO2↑
C.钠与水反应:Na + H2O ==Na+ + OH- + H2↑
D.氯化铁溶液刻蚀铜电路板:Fe3++Cu=Cu2++Fe2+
难度: 简单查看答案及解析
-
下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.Zn+CuSO4=ZnSO4+Cu B.3CO+Fe2O3
2Fe+3CO2
C.AgNO3+KCl=AgCl↓+KNO3 D.2KMnO4
K2MnO4+MnO2+O2↑
难度: 简单查看答案及解析
-
某试管中盛有碘的水溶液,加入少量的CCl4,充分振荡,静置片刻后( )
A.整个溶液变蓝色 B.整个溶液显紫红色 C.上层无色,下层紫红色 D.上层紫红色,下层无色
难度: 中等查看答案及解析
-
氯碱工业制备的碱为( )
A.NaOH B.Na2CO3 C.Ca(OH)2 D.NaHCO3
难度: 简单查看答案及解析
-
在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质。下列实验现象和结论一致且正确的是
A.加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在
B.溶液呈黄绿色,且有刺激性气味,说明有HClO分子存在
C.加入AgNO3溶液产生白色沉淀,说明有Cl-分子存在
D.加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在
难度: 中等查看答案及解析
-
日常生活和工业生产中常用到漂白剂。下列物质没有漂白作用的是( )
A.HClO B.Na2O2 C.新制氯水 D.CaCl2
难度: 简单查看答案及解析
-
以下实验操作正确的是
A.用量筒量取5.0 mL浓硫酸并直接在量筒中稀释
B.用嘴吹灭燃着的酒精灯火焰
C.称量NaOH固体时,将药品直接放在托盘上
D.给烧瓶里的液体加热时,垫上石棉网
难度: 简单查看答案及解析
-
下列粒子既有氧化性又有还原性的是( )
A.Mg B.Na+ C.Fe2+ D.Cl-
难度: 简单查看答案及解析
-
下列过程,观察不到颜色变化的是( )
A.HCl气体通入滴有酚酞的水溶液
B.往NaOH溶液中滴入FeCl3溶液
C.NH3气通过湿润的红色石蕊试纸
D.往AgNO3溶液中加入KCl溶液
难度: 简单查看答案及解析
-
对于反应3Cl2+6NaOH===5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A. Cl2是氧化剂,NaOH是还原剂
B. 被氧化的Cl原子和被还原的Cl原子的个数之比为5∶1
C. Cl2既是氧化剂又是还原剂
D. 每生成1个氧化产物转移6个电子
难度: 中等查看答案及解析
-
下列物质与其用途相符合的是 ( )
①HClO-----作消毒剂 ②NaHCO3----医疗上治疗胃酸过多 ③AgI----人工降雨
④Na2O2----呼吸面具的供氧剂 ⑤淀粉----检验I2的存在 ⑥MgO----作耐高温材料
A.②③④⑤ B.①②③④ C.②③④⑤⑥ D.全部
难度: 简单查看答案及解析
-
下列实验方法错误的是( )
A.用稀盐酸清洗做焰色反应的铂丝
B.用酒精萃取碘水中的碘
C.实验室制取Cl2时用NaOH溶液吸收多余的Cl2防止污染大气
D.可以用加热的方法鉴别白色的Na2CO3 和NaHCO3固体
难度: 简单查看答案及解析
-
下列对于Na2O、Na2O2的比较正确的是 ( )
A.Na2O、Na2O2都是钠的氧化物,都是碱性氧化物
B.Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C.Na2O、Na2O2阴阳离子个数比都为1:2
D.Na2O、Na2O2都是淡黄色固体。
难度: 简单查看答案及解析
-
将30mL0.5mol.L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
A.0.3 mol.L-1 B.0.03 mol.L-1 C.0.04mol.L-1 D.0.05mol.L-1
难度: 简单查看答案及解析
