-
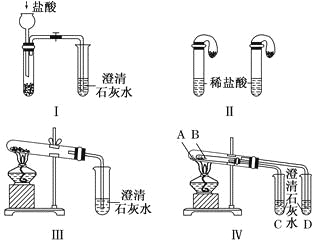
关于Na2CO3和NaHCO3性质的说法错误的是( )
A. 热稳定性:NaHCO3<Na2CO3
B. 与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3
C. 相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D. 等物质的量的Na2CO3、NaHCO3分别与足量盐酸反应产生的CO2质量相同
难度: 简单查看答案及解析
-
分别将一小块钠投入下列溶液中,只有气体放出没有沉淀生成的是( )
A.饱和NaCl溶液 B.稀NaHSO4溶液
C.MgCl2溶液 D.CuSO4溶液
难度: 简单查看答案及解析
-
将饱和FeCl3溶液加入沸水中能制得Fe(OH)3胶体,下列有关说法正确的是
A. 溶液和胶体的本质区别是能否发生丁达尔效应
B. 含0.1 mol FeCl3溶质的溶液形成胶体后,胶体粒子为0.1 mol
C. 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
D. 可通过观察液体是否澄清透明,来区别溶液和胶体
难度: 中等查看答案及解析
-
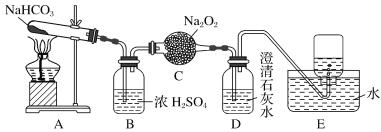
过量的NaHCO3与Na2O2混合,在密闭容器中充分加热后排出气体,残留的物质应是
A. Na2O和Na2O2 B. Na2O2和Na2CO3 C. Na2CO3 D. Na2O
难度: 中等查看答案及解析
-
下列各组离子中能大量共存,溶液呈现无色,且加入一小块钠后仍然能大量共存的是
A. K+、MnO4—、SO42—、H+ B. Ba2+、Na+、HCO3—、NO3—
C. Na+、NO3—、K+、Cl− D. Ca2+、NO3—、Cl−、CO32—
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. 氢氧化钡与稀硫酸反应:Ba2++OH-+H++SO42-==BaSO4↓+H2O
B. Al2O3溶于盐酸中:O2-+2H+===H2O
C. 铜和硝酸银溶液反应:Cu+Ag+===Cu2++Ag
D. Cu(OH)2中加入硝酸:Cu(OH)2+2H+===Cu2++2H2O
难度: 中等查看答案及解析
-
下列有关氧化还原反应的叙述正确的是
A. 在一定条件下能发生反应:3O2===2O3,该反应不属于氧化还原反应
B. 氧化反应一定先于还原反应发生
C. 氧化还原反应中一种物质被氧化,另一种物质一定被还原
D. 氧化性强的物质与还原性强的物质接触一定能发生反应
难度: 中等查看答案及解析
-
溶液中含Na+、SO42-、CO32-、HCO3-四种离子,加入过氧化钠固体后,假设反应前后溶液的体积不变,则离子浓度不变的是
A. HCO3- B. Na+ C. CO32- D. SO42-
难度: 中等查看答案及解析
-
除去NaHCO3溶液中混有的少量Na2CO3可采取的方法是:
A. 通入二氧化碳气体 B. 加入氢氧化钡溶液
C. 加入澄清石灰水 D. 加入稀盐酸
难度: 中等查看答案及解析
-
下列有关焰色反应实验的叙述正确的是
A. 可用铜丝代替铂丝进行实验 B. 观察钾的焰色反应要透过蓝色钴玻璃
C. 实验结束后用碳酸钠溶液洗净铂丝 D. 焰色反应是物质的化学性质
难度: 简单查看答案及解析
-
已知水和苯不互相溶,苯不与钠反应,在烧杯中加水和苯,将一小块钠投入烧杯中,观察到的现象可能是
A. 钠在水层中反应并四处游动 B. 钠停留在苯层中不发生反应
C. 钠在苯的液面上反应并四处游动 D. 钠在苯与水的界面处反应,可能做上下跳动
难度: 中等查看答案及解析
-
PbO2与Cr3+反应生成Cr2O
和Pb2+,则与1.5 mol PbO2反应所需的Cr3+物质的量为
A. 3.0 mol B. 1.5 mol C. 1.0 mol D. 0.75 mol
难度: 简单查看答案及解析
-
下列对于Na2O、Na2O2的比较正确的一项是
A. Na2O、Na2O2都是碱性氧化物 B. Na2O、Na2O2都是易溶于水的白色固体
C. Na2O2在反应中只作氧化剂 D. 1 mol Na2O2与水反应时转移1 mol电子
难度: 中等查看答案及解析
-
常温下,在水溶液中发生如下反应:①16H++10C-+2XO
===2X2++5C2+8H2O ②2A2++B2===2A3++2B-;③2B-+C2===B2+2C-。下列说法错误的是
A. 反应C2+2A2+===2A3++2C-可以进行 B. 反应③是置换反应
C. 氧化性由强到弱的顺序是XO
>C2>B2>A3+ D. 还原性由强到弱的顺序是C->A2+>B->X2+
难度: 中等查看答案及解析
-
在2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O反应中,下列说法正确的是
A. 氧化产物与还原产物物质的量之比5∶2
B. 2mol KMnO4完全反应,转移的电子数为16NA
C. 该反应中HCl做还原剂,KCl、MnCl2是氧化产物
D. 氧化剂与还原剂的物质的量之比5∶1
难度: 中等查看答案及解析
-
Mg、Al混合物与足量盐酸反应,产生标况下的氢气4.48 L,下列说法不正确的是
A. 参加反应的Mg、Al共0.2 mol B. 参加反应的HCl为0.4 mol
C. Mg、Al在反应中共失去0.4 mol电子 D. 若与足量的稀硫酸反应能产生0.2 mol H2
难度: 困难查看答案及解析
-
下列关于Na2CO3和NaHCO3的叙述中错误的是
A.等质量的两种盐分别与足量的盐酸反应,在相同情况下,Na2CO3产生的二氧化碳多。
B.等物质的量的Na2CO3和NaHCO3分别与足量的盐酸反应,在相同情况下产生的二氧化碳体积相等。
C.等物质的量的Na2CO3和NaHCO3分别与同浓度的盐酸反应,Na2CO3消耗盐酸的体积是NaHCO3消耗盐酸体积的2倍
D.将石灰水加入NaHCO3溶液中会产生白色沉淀,而加入Na2CO3溶液中也会产生白色沉。
难度: 困难查看答案及解析