-
下列叙述错误的是( )
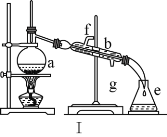
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过1/3容积的试管加热
③把鼻孔靠近容器口去闻气体的气味
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤取用放在细口瓶中液体时,取下瓶塞倒放在桌面上,倾倒液体时,瓶上标签对着地面
⑥将滴管垂直伸进试管内滴加液体
⑦用坩埚钳夹取加热后的蒸发皿
⑧稀释浓硫酸时,把水迅速倒入盛有浓硫酸的量筒中
⑨检验装置的气密性时,把导管的一端浸入水中,用手捂住容器的外壁或用酒精灯微热
A. ②③⑤⑥⑧ B. ①④⑦⑨ C. ①④⑤⑦ D. ②④⑦⑨
难度: 中等查看答案及解析
-
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
A.p(Ne)>p(H2)>p(O2) B.p(O2)>p(Ne)>p(H2)
C.p(H2)>p(O2)>p(Ne) D.p(H2)>p(Ne)>p(O2)
难度: 中等查看答案及解析
-
下列对实验过程的评价正确的是( )
A.某溶液中滴加Ba(NO3)2溶液产生白色沉淀,再加入足量稀盐酸后沉淀不溶解,该溶液中一定含SO42-
B.某固体中加入稀盐酸,产生了无色气体,证明该固体一定是碳酸盐或碳酸氢盐
C.某无色溶液中滴入无色酸酞显红色,该溶液一定显碱性
D.验证烧減溶液中是否有Cl-,先加足量盐酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含Cl-
难度: 中等查看答案及解析
-
下列实验中,所采取的分离方法与对应原理都正确的是( )
选项
目的
分离方法
原理
A
分离溶于水的碘
乙醇萃取
碘在乙醇中的溶解度较大
B
除去KNO3固体中混杂的NaCl
降温结晶
NaCl在水中的溶解度很大
C
分离汽油和水
分液
汽油和水的密度不同
D
由海水(含NaCl)获得蒸馏水
蒸馏
水的沸点与NaCl的沸点不司
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
某KCl样品中含有少量K2CO3、K2SO4和不溶于水的杂质,为了提纯KCl,先将样品溶于适量水中,搅拌、过滤,再将滤液按如图所示步骤进行提纯(过滤操作已略去)。下列说法不正确的是( )

A.起始滤液常温下pH>7
B.试剂Ⅰ为BaCl2溶液
C.该提纯过程中必须经2次过滤
D.步骤③目的是除去CO32-
难度: 中等查看答案及解析
-
下列溶液中所含Cl-浓度与30mL0.1mol/L的AlCl3相同的是( )
A.10mL0.3mol/L的FeCl3溶液
B.30mL0.1mol/L的CaCl2溶液
C.30mL0.3mol/L的KCl溶液
D.300mL0.1mol/L的NaCl溶液
难度: 中等查看答案及解析
-
下列各种仪器:①漏斗②容量瓶③表面皿④分液漏斗⑤天平⑥量筒⑦胶头滴管⑧蒸馏烧瓶。常用于物质分离的是( )
A.①③⑦ B.②⑥⑦
C.①④⑧ D.④⑥⑧
难度: 中等查看答案及解析
-
二氧化硫、氮气、二氧化碳组成的混合气体在同温、同压下与笑气(N2O)的密度相同,则该混合气体中二氧化硫、氮气、二氧化碳的质量比为( )
A.4:5:6 B.22:1:14
C.64:35:13 D.29:8:13
难度: 中等查看答案及解析
-
V mL Al2(SO4)3溶液中含Al3+ a g,取
mL溶液稀释到4V mL,则稀释后溶液中SO42-的物质的量浓度是( )
A.
mol·L-1 B.
mol·L-1
C.
mol·L-1 D.
mol·L-1
难度: 中等查看答案及解析
-
欲配制100mL1.0 mol/L Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4,溶于100mL水中
②将32.2g Na2SO4•10H2O溶于少量水中,再用水稀释至100 mL
③将20 mL 5.0 mol/L Na2SO4溶液用水稀释至100 mL
A.①② B.②③ C.①③ D.①②③
难度: 中等查看答案及解析
-
下列两种气体的原子数一定相等的是 ( )
A. 质量相等、密度不等的NO和C2H6 B. 等体积、等密度的CO2和N2
C. 等温等体积的O2和N2 D. 等压、等体积、等质量的N2和CO
难度: 中等查看答案及解析
-
如图所示,室温下分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2 和O2 的混合气体,若将H2、O2 的混合气体点燃引爆。活塞先左弹,恢复室温后,活塞右滑停留于容器的中央。则原来H2、O2 的物质的量之比可能为①4∶5 ② 2∶5 ③3∶8 ④7∶2
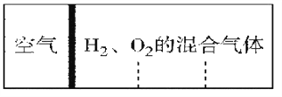
A.①② B.①④ C.②③ D.③④
难度: 困难查看答案及解析
-
将标准状况下,将VL A气体(摩尔质量为Mg/mol)溶于0.1L水中,所得溶液密度为ρg/cm3,则此溶液的物质的量浓度(mol/L)为( )
A.
B.
C.
D.100VρM(MV+2240)
难度: 中等查看答案及解析