-
2018年5月18日,习近平总书记在全国生态环境保护大会上提出“加大力度推进生态文明建设”的要求。下列做法不符合这一要求的是( )
A. 开发利用清洁能源 B. 改进汽车尾气净化技术
C. 直接排放工业废水 D. 研发易降解的农药和塑料
难度: 简单查看答案及解析
-
下列各组物质是按单质、氧化物、混合物的顺序排列的是()
A.金刚石、碘酸钾、赤铁矿
B.氮气、氯酸钾、钢
C.铁水、干冰、冰水混合物
D.氧气、蒸馏水、生铁
难度: 简单查看答案及解析
-
下列实验基本操作中,正确的是
A.
检查装置气密性 B.
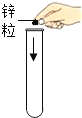 向试管中加入锌粒
向试管中加入锌粒C.
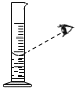 读取液体体积 D.
读取液体体积 D.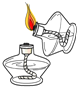 点燃酒精灯
点燃酒精灯难度: 简单查看答案及解析
-
(2011年·衡阳)我国台湾地区近期查出了在饮料等六大类食品中违法添加对人体有害的邻苯二甲酸酯类物质,邻苯二甲酸二(2—乙基己基)酯的化学式为C24H38O4,下列有关说法正确的是( )
A.该物质的碳、氢、氧元素的质量比为24:38:4
B.该物质的分子中碳、氢、氧原子个数比12:19:2
C.该物质的相对分子质量为76
D.该物质中碳、氢、氧三种元素的质量分数有大到小的顺序为氢、碳、氧
难度: 简单查看答案及解析
-
下图是一定条件下某化学反应的微观示意图,其中相同的球代表同种原子,小球间的短线代表原子间的结合.下列说法错误的是:
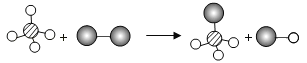
A. 该反应是分解反应
B. 该反应前后原子个数不变
C. 图示有4种分子
D. 参加反应的两种物质的分子个数比为1:1
难度: 中等查看答案及解析
-
下列实验操作能达到实验目的是( )
选项
实验目的
实验操作
A
除去一氧化碳中的二氧化碳
将气体通入灼热的氧化铁中
B
比较 Fe、Cu、Ag的金属活动性
铁丝浸入CuSO4溶液,铜丝浸入AgNO3溶液
C
除去铁制品上的铁锈
将铁制品浸泡在足量的稀硫酸中
D
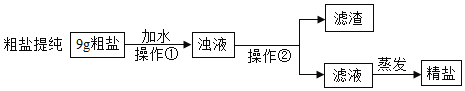
除去粗盐中的难溶性杂质
将粗盐研碎、溶解、蒸发
A.A B.B C.C D.D
难度: 困难查看答案及解析