-
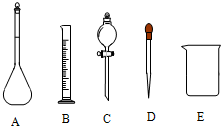
关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水.这些叙述中正确的是( )
A.①②③④
B.②③
C.①②④
D.②③④难度: 中等查看答案及解析
-
下列实验操作中错误的是( )
A.进行蒸发操作时,蒸发皿中出现大量固体时,即可停止加热
B.进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大难度: 中等查看答案及解析
-
关于分散系的有关说法正确的是( )
A.分散质粒子的半径大小顺序为:溶液>胶体>浊液
B.可利用过滤的方法分离胶体和溶液
C.可以利用丁达尔效应鉴别溶液和胶体
D.分散系都是可以稳定存在的物质难度: 中等查看答案及解析
-
如今人们把食品分为绿色食品、蓝色食品、白色食品等类型.绿色植物通过光合作用转化的食品叫绿色食品;而直接从海洋获取的食品叫蓝色食品;通过微生物发酵制得的食品叫白色食品.下面属于蓝色食品的是( )
A.食醋
B.面粉
C.海带
D.白酒难度: 中等查看答案及解析
-
下面是人们对于化学科学的各种常见认识,其中错误的是( )
A.化学将在能源、资源的合理开发和安全应用方面大显身手
B.化学是一门具有极强实用性的科学
C.化学是一门以实验为基础的自然科学
D.化学面对现代日益严重的环境问题显得无能为力难度: 中等查看答案及解析
-
下列说法正确的是( )
A.电解质是指在任何条件下均能导电的化合物
B.蔗糖、酒精在液态和水溶液里均不导电,所以它们是非电解质
C.NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质
D.铜、石墨均导电,所以它们是电解质难度: 中等查看答案及解析
-
氧化还原反应在生产、生活中具有广泛的用途,下列生产生活中的事例不属于氧化还原反应的是( )
A.金属冶炼
B.燃放鞭炮
C.食物腐败
D.用汽油除去油污难度: 中等查看答案及解析
-
能够直接鉴别Na2CO3、BaCl2、NaCl三种溶液的试剂是( )
A.AgNO3溶液
B.稀硫酸
C.稀硝酸
D.NaOH溶液难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.1 mol任何物质都含有6.02×1023个原子
B.0.012 kg12C约含有6.02×1023个碳原子
C.硫酸的摩尔质量是98g
D.常温常压下,1 mol氧气的体积约为22.4L难度: 中等查看答案及解析
-
下列关于氧化还原反应的说法正确的是( )
A.一定有氧气参加
B.一定有电子转移
C.一定属于置换反应
D.氧化反应先于还原反应难度: 中等查看答案及解析
-
下列反应属于氧化还原反应的是( )
A.CaCO3+2HCl=CaCl2+CO2↑+H2O
B.CaO+H2O=Ca(OH)2
C.2H2O22H2O+O2↑
D.CaCO3CaO+CO2↑
难度: 中等查看答案及解析
-
在溶液中能大量共存,且溶液为无色透明的离子组是( )
A.K+、MnO4-、Na+、Cl-
B.H+、Na+、NO3-、CO32-
C.Na+、H+、NO3-、SO42-
D.Ba2+、Na+、OH-、SO42-难度: 中等查看答案及解析
-
如图所示的实验操作中正确的是( )
A.
氢氧化钠放在纸片上称量
B.
向试管中加固体粉末
C.
点燃酒精灯
D.
加热试管中的液体难度: 中等查看答案及解析
-
设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
A.36g水中含有的水分子数是2NA
B.标准状况下,33.6L O2中含有的氧原子数是3NA
C.0.5L 0.2mol/L的NaCl 溶液中含有的Na+数是0.1NA
D.1mol OH-中含电子数目为9NA难度: 中等查看答案及解析
-
以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是( )

A.化合、置换、分解、复分解
B.置换、复分解、化合、分解
C.置换、化合、分解、复分解
D.置换、化合、复分解、分解难度: 中等查看答案及解析
-
下列电离方程式,书写正确的是( )
A.Al2(SO4)3=2Al3++3SO42-
B.AlCl3=Al3++Cl3-
C.Mg(NO3)2=Mg+2+2NO3-
D.KMnO4=K++Mn7++4O2-难度: 中等查看答案及解析
-
能用H++OH-=H2O来表示的化学反应是( )
A.氢氧化镁和稀盐酸反应
B.Ba(OH)2溶液滴入稀硫酸中
C.澄清石灰水和稀硝酸反应
D.二氧化碳通入澄清石灰水中难度: 中等查看答案及解析
-
下列反应的离子方程式书写不正确的是( )
A.稀硫酸与氢氧化钠溶液反应:H++OH-=H2O
B.稀盐酸与铁粉反应:Fe+2H+=Fe2++H2↑
C.碳酸钙与稀盐酸反应:CO32-+2H+=H2O+CO2↑
D.BaCl2溶液与Na2SO4溶液反应:Ba2++SO42-=BaSO4↓难度: 中等查看答案及解析
-
下列各组均有4种物质,选出1个选项,它跟另外3个选项属于不同的分类,其中不正确的是( )
组别 备选项 挑选项 A H2 O2 H2O N2 H2O B C S P K K C SO2 CO2 SO3 Na2O SO3 D H2SO4 NH4Cl KNO3 Na2CO3 H2SO4
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
现行的道路交通安全法规定,醉酒后驾驶机动车的,处15日以下拘留和暂扣3个月以上6个月以下机动车驾驶证,并处500元以上2000元以下罚款.用重铬酸钾检验酒精的反应原理如下:2K2Cr2O7+3CH3CH2OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
关于该反应的说法正确的是( )
A.该反应不是氧化还原反应
B.K2Cr2O7是氧化剂
C.K2Cr2O7是还原剂
D.K2Cr2O7表现还原性难度: 中等查看答案及解析
-
R、X、Y和Z是四种常见的金属.已知XSO4与单质R不反应;XSO4+Z=X+ZSO4;Y+ZSO4=YSO4+Z.四种金属的还原性顺序正确的是( )
A.R>X>Y>Z
B.X>R>Y>Z
C.Y>Z>X>R
D.Z>X>R>Y难度: 中等查看答案及解析
-
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
A.体积比为16:11
B.分子数目比为16:11
C.密度比为16:11
D.物质的量比为16:11难度: 中等查看答案及解析