-
下列说法正确的是( )
A.“酸雨”主要是由空气中的二氧化碳和甲烷引起的
B.汽车使用乙醇汽油可减轻尾气污染,节约石油资源
C.为防止水体污染,目前的农业生产应全面禁止使用任何化肥和农药
D.被腐蚀的铁制品属于不可回收垃圾难度: 中等查看答案及解析
-
下列事实及对这些事实的解释,不相符合的是( )
A.食物腐败;分子本身发生了变化
B.热胀冷缩:分子间的间隔发生了变化
C.酒精挥发:分子大小发生了变化
D.丹桂飘香:分子总是在不断运动着难度: 中等查看答案及解析
-
下列物质的应用,利用的性质与其它三种有本质区别的是( )
A.用醋酸除去茶壶中的水垢
B.用小苏打治疗胃酸过多
C.用镁粉制作焰火和照明弹
D.用活性炭净化水难度: 中等查看答案及解析
-
下列关于生活中常用材料的认识,正确的是( )
A.聚乙烯、聚氯乙烯塑料都可用于制作食品袋
B.区别毛织品和棉织品的简易方法是点燃少许样品并闻气味
C.掩埋、焚烧废旧塑料袋是减少“白色污染”的简捷而有效的方法
D.合金一般比组成它的纯金属的熔点低、硬度小难度: 中等查看答案及解析
-
下列化学实验操作,正确的是( )
A.
加热液体
B. 称量NaOH固体
称量NaOH固体
C.
滴管的使用
D.
取用NaCl固体难度: 中等查看答案及解析
-
下面是某学生练习化学用语时的部分内容,其中正确的是( )
A.1个二氧化硫分子:SOz
B.2个亚铁离子:Fe;’
C.3个氖原子:3Ar
D.氢氧化铝的化学式:AlOH难度: 中等查看答案及解析
-
康康同学在探究燃烧条件时,进行了如图所示的实验.下列关该实验的说法不正确的是( )
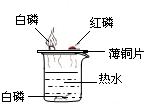
A.铜片上的白磷燃烧而红磷不燃烧,说明燃烧需要达到可燃物的着火点
B.铜片上的白磷燃烧而热水中的白磷不燃烧,说明燃烧需要空气(或氧气)
C.即使向热水中的白磷通入氧气,白磷也不可能燃烧
D.由本实验推知,消除可燃物燃烧的任何一个条件,都可达到灭火的目的难度: 中等查看答案及解析
-
星际分子的不断发现可帮助人们了解生命的起源.美国科学家在银河星系中央的星云中发现了新的星际分子.Z,其化学式为C3H40.下列有关Z的说法正确的是( )
A.该物质属于氧化物
B.该物质中碳、氢、氧三种元素的质量比为3,4,1
C.该物质一个分子中共有8个原子
D.该物质中氧元素的质量分数为50%难度: 中等查看答案及解析
-
下面是部分元素原子或离子的结构示意图.下列相关判断正确的是( )
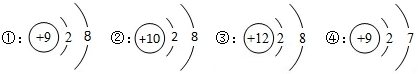
A..①②③属于同一种元素
B._②是阴离子,③是阳离子
C..④在化学反应中容易失去电子
D..③的硫酸盐可表示为RSO4(用R表示该粒子)难度: 中等查看答案及解析
-
下列说法中不正确的是( )
A.一氧化碳可用于工业炼铁,说明一氧化碳具有还原性
B.石油、煤、酒精都是由多种成分组成的混合物
C.常温下碳酸钠溶液能使无色酚酞变红,则其溶液的pH一定大于7
D.制取成本高和贮存困难是目前制约氢能源广泛使用的重要因素难度: 中等查看答案及解析
-
下图是某反应“nX+3Y=Z+6W”的微观示意图.下列说法不正确的是( )

A.反应过程中n一3
B.Y、Z均为单质
C.该反应属于置换反应
D.W的化学式为HCl难度: 中等查看答案及解析
-
要除去下列各物质中的少量杂质(括号内),所选用的试剂、方法正确的是( )
A.盐酸(硫酸):加适量NaOH溶液
B.N2(O2):通过灼热的碳
C.CuO(Cu):加足量稀硫酸、过滤
D.NaCl(泥沙):加水溶解、过滤难度: 中等查看答案及解析