-
下列实验操作中正确的是 ( )
A. 蒸发操作时,应使混合物中的水分完全蒸干后才能停止加热
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出后,再将上层液体从下口放出到另一个烧杯
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
-
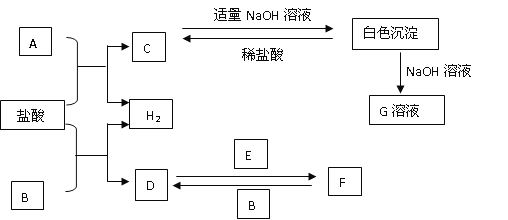
实验室中,要使AlCl3溶液中的Al3+离子全部沉淀出来,适宜的试剂是
A.NaOH溶液 B.氨水 C.盐酸 D.Ba(OH)2溶液
-
下列说法正确的是( )
A.因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性KMnO4溶液、石蕊试液褪色
B.酸雨的pH小于5.6
C.SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色,其原理相同
D.将SO2与Cl2混合后通入品红溶液中漂白效果更好
-
下列氯化物中既能由单质直接化合制得,又可由金属和盐酸反应制得的是( )
A.FeCl3 B.FeCl2 C.CuCl2 D.AlCl3
-
在水溶液中能大量共存,且加入过量稀硫酸溶液时,有气体生成的是
A.Na+、Ag+、CO32-、Cl﹣ B.K+、Ba2+、SO42-、Cl﹣
C.Na+、K+、CO32-、Cl﹣ D.Na+、K+、Cl﹣、SO42-
-
能正确表示下列反应的离子方程式的是( )
A.Cl2通入NaOH溶液:Cl2+OH-=Cl-+ClO-+H2O
B.NaHCO3溶液中加入稀盐酸:CO32-+2H+=CO2↑+H2O
C.往水玻璃中通入二氧化碳:Na2SiO3+H2O+CO2=H2SiO3↓+2Na++CO32﹣
D.Na2CO3溶液中滴加少量的稀盐酸:H++CO32-=HCO3-
-
下列各组物质中,因为反应条件或用量不同而发生不同化学反应的是( )
① C与O2 ② Na与O2 ③ Fe与Cl2 ④ AlCl3溶液与氨水 ⑤ CO2与NaOH溶液
A.除③外 B.除③⑤外 C.除③④外 D.除②外