-
在多电子原子中,轨道能量是由以下哪些因素决定( )
①能层 ②能级 ③电子云的伸展方向 ④电子自旋状态
A. ①② B. ①④ C. ②③ D. ③④
难度: 简单查看答案及解析
-
对碳原子核外两个未成对电子的描述,正确的是( )
A. 电子云形状不同 B. 自旋方向相同
C. 能量不同 D. 在同一轨道
难度: 简单查看答案及解析
-
下列有机物命名正确的是
A. 3,3—二甲基丁烷 B. 3—乙基丁烷
C. 2,2—二甲基丁烷 D. 2,3,3—三甲基丁烷
难度: 简单查看答案及解析
-
同分异构现象是有机物种类繁多的原因之一。与CH3CH2CH2CH2OH互为同分异构体的是( )
A. (CH3)3CHO
B. (CH3)2CHCH2COOH
C. CH3CH2CH2CHO
D. CH3CH2CH2CH2CH2OH
难度: 简单查看答案及解析
-
下列各组混合物中,可以用分液漏斗分离的是( )
A. 苯和水 B. 乙酸和乙醇 C. 酒精和水 D. 溴苯和苯
难度: 简单查看答案及解析
-
下列各组元素都属于p区的是( )
A. 原子序数为1,6,10的元素 B. N,S,P
C. Na,Li,Mg D. Fe,Cr, Cl
难度: 简单查看答案及解析
-
美国《Science》上发表论文,宣布发现了一种 Al 的超原子结构,这种超原子(Al13)是以 1 个 Al 原子 在中心,12 个 Al 原子在表面形成的三角二十面体结构。这种超原子具有 40 个价电 子(价电 子即主族元 素的最外层电子数)时最稳定。请预测稳定的 Al13 所带的电荷为
A.-1 B.+2 C.+3 D.0
难度: 中等查看答案及解析
-
下列说法正确的是
A.正丁烷和异丁烷均有两种一氯取代物
B.乙烯和苯都能与H2发生加成反应,说明二者的分子中均含碳碳双键
C.乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈
D.乙醛能被还原成乙醇,但不能被氧化成乙酸
难度: 中等查看答案及解析
-
下列粒子中,与NH4+具有相同质子数和电子数的是
A.OH— B.F- C.Na+ D.NH3
难度: 中等查看答案及解析
-
在2p能级上最多只能排布6个电子,其依据的规律是
A.能量最低原理 B.泡利不相容原理
C.洪特规则 D.能量最低原理和泡利不相容原理
难度: 中等查看答案及解析
-
2016 年命名第七周期VIIA元素Ts为钿(tian)。下列利用元素周期律的相关推测错误的是
A.Ts为金属元素 B.原子半径:Ts>Br>O
C.Ts的主要化合价一1、+7 D.酸性:HClO4>HTsO4
难度: 中等查看答案及解析
-
下列各项叙述中,正确的是( )
A.Na 的简化电子排布式: [Na]3s1
B.价电子排布为4s24p3的元素位于第四周期第VA族,是p区元素
C.2P和3P轨道形状均为哑铃形,能量也相等
D.氮原子的最外层电子轨道表示式:
难度: 中等查看答案及解析
-
以下能级符号不正确的是
A.3s B.3d C.3p D. 3f
难度: 简单查看答案及解析
-
下列化学用语正确的是( )
A. 氧原子的最外层电子排布式:
B. 四氯化碳的比例模型:
C. 氮气的电子式:
D. 铝原子的结构示意图:
难度: 中等查看答案及解析
-
有机锗具有抗肿瘤活性,锗元素的部分信息如右图,则下列说法错误的是
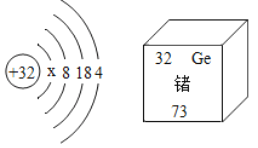
A.在元素周期表中锗元素与硫元素位于同一族 B.x=2
C.锗原子的核外电子数为32 D.锗原子的中子数为41
难度: 简单查看答案及解析
-
我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如图:

下列说法不正确的是( )
A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C5~C11的烃类混合物
D.图中a的名称是2-甲基丁烷
难度: 中等查看答案及解析
-
如图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是

A.Y、R两种元素的气态氢化物稳定性:Y>R
B.简单离子的半径:X<Z<M
C.最高价氧化物对应水化物的酸性:R<N
D.由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
难度: 中等查看答案及解析
-
聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图
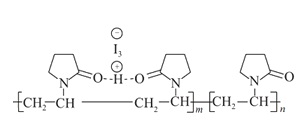 ,下列说法不正确的是( )
,下列说法不正确的是( )A.聚维酮的单体是
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质 D.聚维酮在一定条件下能发生水解反应
难度: 中等查看答案及解析

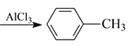 +HCl
+HCl