-
下列关于金属的叙述中正确的是( )
A.所有的金属都是固态的 B.金属具有导电性、导热性和延展性
C.常温下所有金属都能与酸反应 D.金属元素在自然界中都是以化合态形式存在的
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.氨水、铝热剂都是混合物
B.CO2、Al2O3能和NaOH反应,所以它们是酸性氧化物
C.Na2O、Na2O2都能和HCl反应,所以它们是碱性氧化物
D.烧碱可作为治疗胃酸过多的一种药剂
难度: 简单查看答案及解析
-
焰火“脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。下列说法中正确的是( )
A.焰色反应是化学变化
B.用稀盐酸清洗做焰色反应的铂丝(或铁丝)
C.焰色反应均应透过蓝色钴玻璃观察
D.利用焰色反应可区分NaCl与Na2CO3固体
难度: 简单查看答案及解析
-
利用下图装置做铝热反应实验。下列说法不正确的是
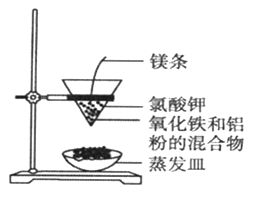
A.该反应的化学方程式是2Al+Fe2O3
2Fe+Al2O3
B.该反应会产生高温、发出强光
C.根据铝热反应的原理,可以冶炼某些金属
D.若反应中转移3 mol电子,则消耗氧化剂的物质的量是1 mol
难度: 中等查看答案及解析
-
除去镁粉中混有的少量铝粉,可选用下列溶液中的( )
A.盐酸 B.稀硝酸 C.氨水 D.浓氢氧化钾溶液
难度: 中等查看答案及解析
-
下列反应中,氯元素被氧化的是( )
A. 2KClO3
2KCl+3O2↑ B. 2P+5Cl2
2PCl5
C. MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑ D. H2+Cl2
 2HCl
2HCl难度: 简单查看答案及解析
-
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.酸性溶液中:Mg2+、K+、SO42-、NO3-
B.无色溶液中:Na+、A13+、NO3-、MnO4-
C.加入Na2O2的溶液中:Na+、Cl-、CO32-、HSO3-
D.与Al反应放出H2的溶液中:NH4+、Na+、NO3-、CO32-
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.钠和冷水反应 Na+2H2O=Na++2OH+H2↑
B.Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-=2AlO2-+H2O
C.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
D.FeCl2溶液通入足量的Cl2反应:Fe2++Cl2=Fe3++2Cl-
难度: 中等查看答案及解析
-
以NA表示阿伏加德罗常数,下列说法中不正确的是( )
A.Na与水反应,每生成1mol H2,转移的电子数为2NA
B.1 mol Al与足量强酸完全反应或与足量强碱完全反应,失去电子数目都为3NA
C.58.5 g氯化钠固体中含有NA个氯化钠分子
D.1 mol Na2O和Na2O2的混合物中含有阴离子数为NA
难度: 中等查看答案及解析
-
己知在碱性溶液中可发生如下反应:
2R(OH)3+ 3C1O-+ 4OH-= 2RO4n-+3Cl-+5H2O。则RO4n-中R的化合价是( )
A.+3 B.+4 C.+5 D.+6
难度: 简单查看答案及解析
-
将a g甲烷(CH4)完全燃烧后的气体(此时温度高于100℃)通入装有足量Na2O2的试管中,则该试管增重多少( )
A.a g B.大于a g C.小于a g D.无法判断
难度: 中等查看答案及解析
-
等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是( )
A.甲、乙中都是铝过量
B.甲中铝过量,乙中碱过量
C.甲中酸过量,乙中铝过量
D.甲中酸过量,乙中碱过量
难度: 中等查看答案及解析
-
下列各组物质不能用括号内的试剂等鉴别的是( )
A.NaHCO3和Na2CO3两种溶液( (CaCl2溶液)
B.MgCl2溶液AlCl3两种溶液(NaOH溶液)
C.NaCl和Na2SO4两种溶液(激光笔)
D.KCl和Na2SO4两种溶液(焰色反应)
难度: 中等查看答案及解析
-
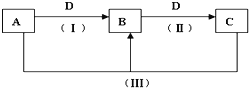
下表所列各组物质中,物质之间不能通过一步反应就能实现如图所示转化的是( )

物质
a
b
c
A
Al2O3
AlCl3
Al(OH)3
B
NaAlO2
Al(OH)3
AlCl3
C
CO2
NaHCO3
Na2CO3
D
Na
Na2O
Na2O2
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
加热10.0 g碳酸钠与碳酸氢钠的固体混合物至质量不再发生变化,剩余固体的质量为6.9 g,则混合物中碳酸钠的质量分数为( )
A.16% B.32% C.58% D.84%
难度: 中等查看答案及解析
-
由铁、锌、铝、镁四种金属中的两种组成的混合物10g,与足量盐酸反应产生的氢气在标准状况下为11.2L,则混合物中一定含有的金属是( )
A. 铁 B. 锌 C. 铝 D. 镁
难度: 困难查看答案及解析


 B.
B. 
 D.
D.