-
14C常用于测定生物遗骸的年份。下列说法正确的是
A. 14C含有14个中子 B. 14C与14N含有相同的质子数
C. 14C与C60互为同位素 D. 14C与12C是两种不同的核素
难度: 简单查看答案及解析
-
几种短周期元素的原子半径及主要化合价如下表:
元素代号
X
Y
Z
W
原子半径/pm
160
143
70
66
主要化合价
+2
+3
+5、+3、-3
-2
下列叙述正确的是
A、X、Y元素的金属性X<Y
B、一定条件下,Z单质与W的常见单质直接生成ZW2
C、Y的最高价氧化物对应的水化物能溶于稀氨水
D、一定条件下,W单质可以将Z单质从其氢化物中置换出来
难度: 中等查看答案及解析
-
下列说法正确的是
A. 浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸
B. 在KI淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应
C. 在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中一定含SO42-
D. 将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化
难度: 中等查看答案及解析
-
关于元素周期表,下列叙述中正确的是( )
A. 在金属元素与非金属元素的分界线附近可以寻找制备超导体材料的元素
B. 在过渡元素中可以寻找制备催化剂及耐高温、耐腐蚀材料的元素
C. 在过渡元素区域可以寻找制备新型农药材料的元素
D. 非金属性最强的元素在元素周期表的最右上角
难度: 简单查看答案及解析
-
元素周期表是化学学习的工具。如图是镁元素在周期表中的表示,下列有关镁元素信息不正确的是( )
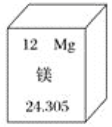
A. 原子序数是12
B. 它是金属元素
C. 原子结构示意图为
D. 镁元素在地壳中的含量为24.305%
难度: 简单查看答案及解析
-
下列各表是元素周期表的一部分,表中数字表示的原子序数与其在周期表中的位置相符的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
A、B、C为三种短周期元素,A、B在同一周期,A、C的最低价离子分别为A2-、C-,离子半径A2-大于C-,B2+和C-具有相同的电子层结构。下列判断正确的是( )
A. 原子序数由大到小的顺序是C>A>B
B. 原子半径由大到小的顺序是r(B)>r(A)>r(C)
C. 离子半径由大到小的顺序是r(C-)>r(B2+)>r(A2-)
D. 原子最外层电子数由多到少的顺序是B>A>C
难度: 中等查看答案及解析
-
下列对于某些离子的检验及结论中一定正确的
A. 加入稀盐酸产生无色的气体,将气体通入澄清石灰水中,溶液变浑浊,一定有
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
难度: 简单查看答案及解析
-
氯气是一种重要的工业原料,工业上利用反应:3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
A. 若管道漏气,遇氨就会产生白烟 B. 该反应利用了氯气具有的氧化性
C. 该反应属于复分解反应 D. 生成1 mol 氮气有6 mol的电子转移
难度: 中等查看答案及解析
-
关于离子键、共价键的各种叙述中,下列说法中正确的是( )
A. 在离子化合物里,只存在离子键,没有共价键
B. 非极性键只存在于双原子的单质分子(如Cl2)中
C. 在共价化合物分子内,一定不存在离子键
D. 由不同元素组成的多原子分子里,一定只存在极性键
难度: 中等查看答案及解析
-
下列电子式或用电子式表示化合物形成过程正确的是( )
A.
B.
C.
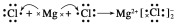 D.
D. 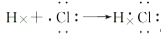
难度: 中等查看答案及解析
-
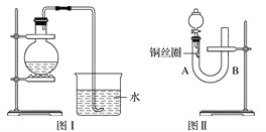
利用如图装置,在锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )
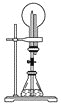
A. 铜与稀盐酸 B. 碳酸氢钠与氢氧化钠溶液
C. 碳酸钙与稀硫酸 D. 碳酸氢铵与稀盐酸
难度: 中等查看答案及解析
-
下列说法中正确的是( )
A. 质子数相同的粒子一定属于同种元素
B. 原子序数相同的微粒电子数一定相同
C. 原子序数相同的两种粒子,性质一定相同
D. 电子数相同的粒子不一定是同一种元素
难度: 中等查看答案及解析
-
1L稀硝酸和稀硫酸的混合溶液,其溶质的物质的量浓度分别为0.1mol/L 和0.4mol/L。若向该混合溶液中加入足量的铜粉。则最多能溶解铜粉的质量为( )
A. 2.4 g B. 3.2 g C. 6.4 g D. 9.6 g
难度: 困难查看答案及解析