-
对人类生存环境会造成危害的是
A.生活污水处理达标后排放
B.化肥和杀虫剂的乱施滥用
C.废旧电池回收
D.使用太阳能热水器
难度: 简单查看答案及解析
-
检验一瓶长期暴露在空气中氢氧化钠是否变质,下列可作为检验试剂的是
A.稀盐酸
B.无色酚酞
C.紫色石蕊试液
D.水
难度: 中等查看答案及解析
-
下列有关四个基本反应类型的说法,正确的是
A.化合反应一定只有一种生成物
B.有单质参加的反应一定是置换反应
C.分解反应一定有气体生成
D.生成两种化合物的反应一定是复分解反应
难度: 简单查看答案及解析
-
在CuCl2和MgCl2的混合液中,加入过量的锌粉,充分反应后过滤,留在滤纸上的物质是( )
A.Cu B.Cu和Zn C.Cu和Mg D.Zn、Mg和Cu
难度: 中等查看答案及解析
-
CO和CO2的混合气体10g和足量的O2反应后,所得气体的质量比原来增加了4g,则原混合气体中二氧化碳的含量是
A.20%
B.30%
C.60%
D.70%
难度: 中等查看答案及解析
-
分类法是化学学习和研究的重要方法之一, 下列分类正确的是
A.盐:纯碱、小苏打、硫酸铝
B.非金属元素:Mg、Hg、Si
C.混合物:空气、石油、冰水共存物
D.合成材料:塑料、羊毛、合金
难度: 简单查看答案及解析
-
下列实验操作正确的是
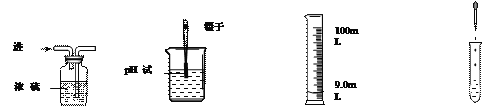
A.干燥氧气 B.测定溶液pH C.量取9.0mL液体 D.向试管中滴加液体
难度: 简单查看答案及解析
-
已知20℃时氯化钠的溶解度为36g,现向50g水中加入20g氯化钠,充分搅拌后能得到20℃时的溶质的质量分数为( )
A. 40% B. 28.6% C. 26.5% D. 36%
难度: 中等查看答案及解析
-
A、B、C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是

A.t 1℃时,A的饱和溶液65g中含有溶剂50g
B.要从B溶液中得到B,通常可采用蒸发溶剂使其结晶的方法
C.在t 2℃,A,B两种溶液中溶质的质量分数相同
D.将t 2℃A,B,C三种物质的饱和溶液降温至t 1℃时,C溶液中溶质的质量分数保持不变
难度: 中等查看答案及解析
-
推理是一种重要的研究和学习方法.下列推理正确的是( )
A.碱中都含有氢氧根,所以碱中一定含有氢元素
B.分子是构成物质的微粒,因此物质都是由分子构成的
C.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
D.铁丝能在氧气中燃烧,空气中有氧气,所以铁丝也能在空气中燃烧
难度: 简单查看答案及解析
-
用括号中的试剂除去下列物质中所含杂质,所用药品错误的是
A.NaOH溶液中混有Na2CO3 (稀硫酸)
B.NaCl溶液中混有Na2SO4 (BaC12 溶液)
C.KCl溶液中混有K2CO3 (稀盐酸)
D.CO中混有CO2 (NaOH 溶液)
难度: 中等查看答案及解析
-
下列化学知识运用错误的是
A.施加熟石灰可以改良酸性土壤
B.用氢氧化钠溶液清除餐具上的油污
C.用干冰作制冷剂
D.被雨淋湿的自行车应立即擦干以防生锈
难度: 简单查看答案及解析
-
装有50g稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量。有关量的变化情况见图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化)。其中肯定不正确的是( )
A.
 B.
B.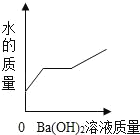
C.
 D.
D.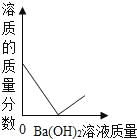
难度: 困难查看答案及解析
-
在FeO、Fe2O3和CaCO3的混合物中,已知铁元素的质量分数为56%,则CaCO3的质量分数可能是:
A. 10% B. 30% C. 25% D. 35%
难度: 中等查看答案及解析
-
根据你所学化学知识,判断下列做法正确的是
A.铵态氮肥与熟石灰混合使用
B.补钙防止甲状腺肿大
C.进入久未开启的菜窑前做灯火试验
D.用工业盐亚硝酸钠(NaNO2)代替食盐烹调
难度: 简单查看答案及解析