-
化学在资源利用、环境保护等与社会可持续发展密切相关的领域发挥着积极作用。下列做法与社会可持续发展理念相违背的是
A. 回收利用废旧金属 B. 加强植树造林,增大绿化面积
C. 大力开发不可再生资源 D. 改进汽车尾气净化技术
难度: 简单查看答案及解析
-
硅是带来人类文明的重要元素之一。下列物质中主要成分是硅酸盐的是
A. 陶瓷 B. 金刚石 C. 光导纤维 D. 大理石
难度: 简单查看答案及解析
-
下列变化中,必须加入氧化剂才能发生的是
A. SO2→S B. Cl2→HClO C. Fe2+→Fe3+ D. HCO3-→CO32-
难度: 简单查看答案及解析
-
下列说法不正确的是
A. 要想使AlCl3溶液中的Al3+几乎全部沉淀出来,可以加入过量的氨水
B. 向FeCl2溶液中加入氨水,最终会看到红褐色沉淀
C. 漂白粉的有效成分是次氯酸钙
D. 氢氧化钠、纯碱溶液要存放在带磨砂玻璃塞的试剂瓶中
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. 氯气和水反应:Cl2+H2O=2H++Cl-+ClO-
B. 腐蚀铜制印刷电路板:3Cu+2Fe3+=3Cu2++2Fe
C. 过量SO2气体通入澄淸石灰水中:SO2+OH-=HSO3-
D. 向水玻璃中滴加盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+
难度: 简单查看答案及解析
-
以下物质间的每步转化能通过一步反应就能实现的是
A. Al2O3→Al(OH)3→NaAlO2 B. Si→SiO2→H2SiO3
C. S→SO2→H2SO4 D. HCl→Cl2→FeCl2
难度: 简单查看答案及解析
-
下列有关物质的性质与用途对应关系正确的是
A. 明矾易溶于水,可用作净水剂 B. HClO显酸性,可用于杀菌消毒
C. SO2具有氧化性,可用于纸浆漂白 D. 铁粉具有还原性,可用作食品抗氧化剂
难度: 简单查看答案及解析
-
根据下列实验操作和现象所得到的结论正确的是
操作和现象
结论
A
室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色
氧化性:Fe3+>I2
B
将新制氯水光照,溶液中有气泡产生
HCl在光照条件下分解
C
向蔗糖(C12H22O11)固体中加入浓硫酸,蔗糖变黑
浓硫酸具有吸水性
D
将某气体通入澄清石灰水,石灰水变浑浊
该气体一定是CO2
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列有关化学用语表示正确的是
A. 中子数为10的氧原子:108O B. 电离方程式NH3·H2O=NH4++ OH-
C. Mg2+的结构示意图:
D. 电离方程式:Ca(OH)2=Ca2++(OH)22-
难度: 简单查看答案及解析
-
除去镁粉中少量的铝粉,最适宜的试剂是
A. 氨水 B. AgNO3溶液 C. NaOH溶液 D. 盐酸
难度: 简单查看答案及解析
-
下列各种冶炼方法中,可制得相应金属的为
A.高温分解碳酸钙 B.电解熔融氯化镁
C.氧化铝和焦炭混合加热 D.电解饱和食盐水
难度: 中等查看答案及解析
-
下列关于SO2的说法中,不正确的是
A.SO2能使品红溶液褪色,是因为SO2具有漂白性
B.SO2在空气中极易被氧化为SO3
C.SO2通入Na2SO3或NaHCO3溶液中均能发生反应
D.SO2是形成酸雨的大气污染物之一,主要来自于化石燃料的燃烧和工厂排放的废气
难度: 中等查看答案及解析
-
下列反应中,水只作还原剂的是
A. 2H2O
2H2 ↑+ O2↑ B. 2Na+ 2H2O=2NaOH + H2↑
C. 2F2+ 2H2O = 4HF + O2 D. Na2O + H2O = 2NaOH
难度: 中等查看答案及解析
-
下列有关Na2CO3和NaHCO3的性质说法正确的是
A. 溶解度:Na2CO3>NaHCO3
B. 右图所示装置可证明稳定性:Na2CO3>NaHCO3
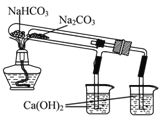
C. 用澄清石灰水可鉴别Na2CO3溶液和NaHCO3溶液
D. 等质量的Na2CO3和NaHCO3分别与过量盐酸反应,放CO2质量相同
难度: 简单查看答案及解析
-
设NA为阿伏加徳罗常数的值,下列说法正确的是
A. 常温常压下,16gO3含氧原子数为NA
B. 7.1gCl2与足量NaOH反应转移的电子数为0.2NA
C. 足量的Fe 与1mol氯气充分反应,转移的电子数为0.3NA
D. 标准状况下,22.4LCCl4中含有的原子数目为5NA
难度: 中等查看答案及解析
-
某无色溶液能与铝作用生成H2,则溶液中一定可以大量共存的离子组是
A. Cl-、Ba2+、Mg2+、ClO- B. Cl-、SO42-、Cu2+、Mg2+
C. Cl-、SO42-、K+、Na+ D. HCO3-、NO3-、Na+、Cl-
难度: 中等查看答案及解析
-
将适量铜粉放入硫酸铁溶液中,完全反应后,溶液中的Cu2+和Fe3+的物质的量浓度相等,则已反应的Fe3+和原溶液中Fe3+总物质的量之比是
A.2 :3 B.3 :2 C.2 :5 D.1 :2
难度: 中等查看答案及解析
-
a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:①a、c均能与稀硫酸反应放出气体;②b与d 的硝酸盐反应,置换出单质d;③c与强碱反应放出气体;④c、e在冷浓硝酸中发生钝化。由此判断a、b、c、d、e分别是
A. Fe、Cu、Al、Ag、Mg
B. Al、Cu、Mg、Ag、Fe
C. Mg、Ag、Al、Cu、Fe
D. Mg、Cu、Al、Ag、Fe
难度: 中等查看答案及解析
-
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量比为
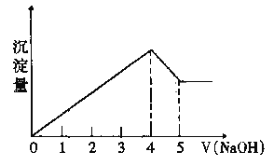
A. 2∶1 B. 4∶1 C. 1∶1 D. 1∶2
难度: 困难查看答案及解析