-
下列实验操作正确的是
A. 使用容量瓶配制溶液,移液时应洗涤烧杯2~3次 B. 用100 mL量筒量取5.5 mL稀盐酸
C. 用托盘天平称量11.50 g NaCl固体 D. 配制一定浓度的溶液时,固体物质可以直接在容量瓶中溶解
难度: 简单查看答案及解析
-
下列化学变化中,需加入氧化剂才能实现的是( )
A. C→CO2 B. CO2→CO C. CuO→Cu D. H2SO4→BaSO4
难度: 中等查看答案及解析
-
朱自清先生在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里…月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影…”月光穿过薄雾所形成的美景仙境,其本质原因是( )
A. 夜里的月色本身就很美
B. 颗粒直径约为1nm~100nm的小水滴分散在空气中
C. 光线是一种胶体
D. 雾是一种胶体,能产生丁达尔现象
难度: 简单查看答案及解析
-
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴上危险警告标签。下面所列物质贴错了标签的是( )
A
B
C
D
物质
氢氧化钠
金属汞
碳酸钠
烟花爆竹
危险警告标签




A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列物质分类的正确组合是( )

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列关于物质属于电解质的是( )
A. 稀硫酸 B. 酒精 C. 熔融的氯化钠 D. 石墨
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 由于碘在酒精中的溶解度大,可以用酒精把碘水中的碘萃取出来
B. 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
C. 由于沙子是难溶于水的固体,因此可用过滤法分离沙子与水的混合物
D. 可以用冷却法从热的含少量KNO3的NaCl浓溶液中分离得到纯净的NaCl
难度: 中等查看答案及解析
-
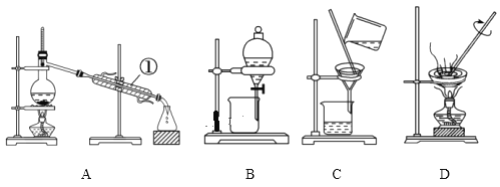
下列操作中正确的是( )
A. 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部
C. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
D. 分液操作时,分液漏斗下端紧靠烧杯内壁
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 氯化钠溶液在电流作用下电离成钠离子和氯离子
B. 溶于水后能电离出氢离子的化合物一定是酸
C. 二氧化碳溶于水能导电,故二氧化碳属于电解质
D. 硫酸钡难溶于水,但硫酸钡属于电解质
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 1molOH-的质量为17g
B. 二氧化碳的摩尔质量为44g
C. 铁原子的摩尔质量等于它的相对原子质量
D. 标准状况下,1mol 任何物质的体积均为22.4L
难度: 简单查看答案及解析
-
下列对实验过程的评价正确的是( )
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体一定是CaCO3
B. 某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO42-
C. 常温下,某无色溶液滴入无色酚酞试液显红色,该溶液一定显碱性
D. 验证烧碱溶液中是否含有Cl-,先加稀硫酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl-
难度: 简单查看答案及解析
-
意大利罗马大学的FulvioCacsce 等人获得了极具理论研究意义的N4 分子,下列说法正确的是( )
A. N4属于一种新型的化合物
B. N4与N2的摩尔质量相等
C. 标准状况下,等体积的N4与N2所含的原子个数比为1:2
D. 等质量的N4与N2所含的原子个数比为1:1
难度: 中等查看答案及解析
-
用NA 代表阿伏加德罗常数的值,下列说法正确的是( )
A. 阿伏伽德罗常数是6.02×1023
B. 标准状况下,11.2LCCl4所含分子数为0.5NA
C. 1.8g的NH4+中含有的电子数为NA
D. 0.1mol·L-1的MgCl2溶液中,所含Cl-的数目为0.2NA
难度: 简单查看答案及解析
-
在相同的温度和压强下,A容器中的CH4气体和B容器中的NH3气体所含的氢原子总数相等,则两个容器的体积比为( )
A. 4:5 B. 1:1 C. 4:3 D. 3:4
难度: 中等查看答案及解析
-
下列溶液中,Na+浓度最大的是( )
A. 1mol·L-1Na2SO4溶液100mL B. 0.9mol·L-1Na3PO4溶液10mL
C. 2.5mol·L-1NaOH溶液50mL D. 1 mol·L-1NaHCO3溶液100mL
难度: 简单查看答案及解析
-
某校化学兴趣小组在实验中发现一瓶溶液,标签上标有“CaCl20.1mol·L-1”的字样,下面是该小组成员对溶液的叙述,正确的是( )
A. 配制1L溶液,可将0.1mol的CaCl2溶于1L水
B. 取少量该溶液加水至溶液体积为原来的二倍,所得溶液c(Cl−)=0.1mol·L-1
C. Ca2+和Cl-的浓度都是1mol·L-1
D. 取该溶液的一半,则所取溶液c(CaCl2)=0.05mol·L-1
难度: 中等查看答案及解析
-
含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl-1.5mol,K+和Na+共1.5mol,Mg2+为0.5mol,则SO42-的物质的量为
A. 0.2mol B. 0.5mol C. 0.25mol D. 0.15mol
难度: 中等查看答案及解析
-
下列各组离子反应可用H++OH-=H2O 表示的是( )
A. 氢氧化钡和硫酸 B. 氢氧化铁和盐酸
C. 醋酸和氢氧化钠 D. 硫酸氢钠和氢氧化钠
难度: 简单查看答案及解析
-
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较, 水的作用不相同的是( )
①Cl2+H2O=HCl+HClO ②4Fe(OH)2+O2 +2H2O=4Fe(OH)3
③2F2 +2H2O=4HF+O2 ④2Na+2H2O=2NaOH+H2↑
A. ③④ B. ①④ C. ①③ D. ②④
难度: 简单查看答案及解析
-
在下列条件的水溶液中可以大量共存的离子组是( )
A. 使酚酞变红的溶液中:Na+、Mg2+、Cl-、NO3–
B. 无色透明的溶液中:K+、SO42-、Na+、MnO4-
C. 无色透明的溶液中:SO42-、Cl-、Al3+、NH4+
D. 含大量H+的溶液中:CO32-、SO42-、K+、Cl-
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是( )
A. 向碳酸钠溶液中加入足量的盐酸:CO32-+2H+=CO2↑+H2O
B. 氢氧化钡溶液中加入足量稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O
C. 向三氯化铁溶液中逐滴加入过量的氨水:Fe3++3OH-=Fe(OH)3↓
D. 氧化铜与盐酸反应:O2-+2H+=H2O
难度: 中等查看答案及解析
-
下列反应中的酸,既表现出酸性又表现出氧化性的是( )
A. Zn+2HCl=ZnCl2+H2↑
B. 4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O
C. 3Cu+8HNO3(稀)
3Cu(NO3)2+2NO↑+4H2O
D. NaOH +HCl=NaCl+H2O
难度: 简单查看答案及解析
-
根据反应:①2Fe3++2I-=2Fe2++I2②Br2+2Fe2+=2Fe3++2Br-③Br2+2I-=I2+2Br-,判断离子的还原性由强到弱的顺序正确的是( )
A. Br-、Fe2+、I- B. I-、Fe2+、Br-
C. Br-、I-、Fe2+ D. Fe2+、I-、Br-
难度: 中等查看答案及解析
-
已知30mL浓度为0.5mol·L-1的Na2SO3溶液恰好与50mL浓度为0.1mol·L-1的KRO4溶液完全反应转化为Na2SO4。则R元素在产物中的化合价是( )
A. +1 B. +2 C. +3 D. +4
难度: 中等查看答案及解析