-
下列现象与胶体的性质无关的是
A. 河流入海口处易形成三角洲
B. 将盐卤或石膏加入豆浆,制成豆腐
C. 向 FeCl3 溶液中加入 NaOH 溶液,会出现红褐色沉淀
D. 清晨,人们经常看到的阳光穿过茂密的树木枝叶所产生的美丽景象
难度: 简单查看答案及解析
-
同温同压下,20 mL A2气体与30 mL B2气体恰好完全反应生成20 mL某气体X,则X的化学式为( )
A. A2B3 B. AB2 C. AB3 D. A3B2
难度: 中等查看答案及解析
-
“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
A.①④⑥ B.②③④ C.②③⑤ D.①③④⑥
难度: 中等查看答案及解析
-
下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是 ( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶中转移液体
A.①和② B.①和③ C.③和④ D.①和④
难度: 简单查看答案及解析
-
下列实验操作中错误的是( )
A.蒸发操作时,当蒸发至有大量晶体析出时即可停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
难度: 中等查看答案及解析
-
下列说法中正确的是
A.铁的摩尔质量就是铁的相对原子质量
B.SO42-的摩尔质量是96g/mol
C.1molO2的质量是32g/mol
D.CO2的摩尔质量是44g
难度: 中等查看答案及解析
-
下列溶液中Cl-浓度最小的是( )
A.200mL 2mol/L MgCl2溶液 B.300mL 2.5mol/L FeCl3溶液
C.500mL 2.5mol/L NaCl溶液 D.250mL 1mol/L AlCl3溶液
难度: 简单查看答案及解析
-
在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子。同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
A.物质的量之比为16:11 B.密度之比为11:16
C.摩尔质量之比为11:16 D.体积之比为11:16
难度: 中等查看答案及解析
-
NA表示阿伏加德罗常数。下列叙述中正确的是( )
A.标准状况下,22.4 L水中含有的水分子数为NA
B.4.0 g NaOH固体溶于100 mL水中,得到1 mol·L−1的NaOH溶液
C.常温、常压下,22 g CO2中含有的氧原子数为NA
D.1 L 0.5 mol·L−1 Na2SO4溶液中,含有的氧原子总数为2NA
难度: 简单查看答案及解析
-
NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,下列分类标准不正确的是
A. 钠的化合物 B. 可与硝酸反应 C. 可溶于水 D. 电解质
难度: 中等查看答案及解析
-
关于物质的类别,下列说法正确的是
A.食盐水、糖水、冰水都属于混合物
B.烧碱、火碱、消石灰都属于碱
C.KHSO4、HCl、HNO3在水中都能电离出氢离子,都属于酸
D.溶液、胶体、浊液都属于稳定的分散系
难度: 简单查看答案及解析
-
胶体区别于其它分散系的本质特征是()
A.胶体在一定条件下能稳定存在
B.光束通过胶体时有丁达尔效应
C.胶体粒子直径在1-100 mm之间
D.胶体的分散质能通过滤纸空隙,而悬浊液的分散系不能
难度: 中等查看答案及解析
-
某溶液中大量存在以下五种离子:NO3-、SO42-、Fe3+、H+、M,其物质的量之比为n(NO3-):n(SO42-):n(Fe3+ ):n(H+):n(M)=2:3:1:3:1,则M可能为( )
A.Mg2+ B.K+ C.CO32- D.Ba2+
难度: 中等查看答案及解析
-
下列电离方程式正确的是( )
A.硫酸氢钠的电离方程式:NaHSO4=Na++HSO4-
B.MgCl2的电离方程式:MgCl2=Mg2++Cl22-
C.氯酸钾的电离方程式:KClO3=K++Cl-+O2-
D.碳酸钠的电离方程式:Na2CO3=2Na+ +CO32-
难度: 中等查看答案及解析
-
不能用H++OH-=H2O表示的反应是
A.硫酸与氢氧化钾溶液反应 B.硫酸与氢氧化钡溶液反应
C.硝酸与氢氧化钠溶液反应 D.盐酸与稀氢氧化钙溶液反应
难度: 中等查看答案及解析
-
下列化学反应的离子方程式正确的是
A.碳酸钙与盐酸溶液反应:2H+ + CO32- = H2O + CO2
B.铁钉放入稀硫酸中:2Fe+ 6H+ = 2Fe 3+ + 3H2↑
C.碳酸氢钠与稀盐酸反应:HCO3-+ H+ = CO2↑ + H2O
D.氢氧化钡溶液与稀硫酸反应:Ba2+ + SO42- + H+ + OH- = BaSO4↓ + H2O
难度: 中等查看答案及解析
-
氧化还原反应的实质是( )
A.分子中的原子重新组合 B.氧原子的得失
C.化合价的升降 D.电子的得失或偏移
难度: 简单查看答案及解析
-
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是
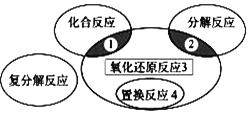
A.2H2+O2
2H2O
B.2NaHCO3
Na2CO3+H2O+CO2↑
C.2Na2O2+2H2O═4NaOH+O2↑
D.Zn+H2SO4=ZnSO4+H2↑
难度: 中等查看答案及解析
-
下列反应进行分类时,既属于氧化还原反应又属于置换反应的是 ( )
A. CH4+2O2
CO2+2H2O B. 2KClO3
2KCl+3O2↑
C. S+O2
SO2 D. 8NH3+3Cl2=6NH4Cl+N2↑
难度: 中等查看答案及解析
-
氮化铝(AlN)广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN的合成反应为:Al2O3+N2+3C=2AlN+3CO,该反应中发生氧化反应的物质是
A.Al2O3 B.N2 C.C D.Al2O3 和C
难度: 中等查看答案及解析
-
下列氧化还原反应中,水作为还原剂的是( )
A.3Fe+4H2O
Fe3O4+4H2 B.3NO2+H2O = 2HNO3+ NO
C.2Na2O2+2H2O = 4NaOH+O2↑ D.2F2+2H2O = 4HF+O2
难度: 简单查看答案及解析
-
下列有关实验的叙述正确的是( )
A.实验室蒸馏石油
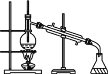
B.实验室稀释浓硫酸

C.配制100mL0.1mol/L的盐酸

D.可用于分离或提纯胶体

难度: 中等查看答案及解析
-
下列实验操作能达到实验目的是( )
实验目的
实验操作
A
配制1.0mol/LCuSO4溶液
把25g胆矾晶体溶于水配成100mL溶液
B
证明某溶液中含有SO42-
向该溶液中滴入BaCl2溶液
C
实验室制大量CO2
向稀硫酸中加入大理石
D
制备Fe(OH)3胶体
将饱和的FeCl3溶液滴加到热NaOH溶液中
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是
A.Ca2+、Na+、NO3-、CO32- B.Mg2+、Cl-、NH4+、SO42-
C.K+、Cl-、HCO3-、NO3- D.Ca2+、Na+、Fe3+、NO3-
难度: 中等查看答案及解析
-
在下列各溶液中,离子一定能大量共存的是
A.强碱性溶液中:K+、Al3+、Cl-、SO42-
B.在无色透明的溶液中:K+、Cu2+、NO3-、SO42-
C.含有0.1mol·L−1Ca2+的溶液中:Na+、K+、CO32-、Cl-
D.室温下,pH=1的溶液中:Na+、Fe3+、Cl-、SO42-
难度: 中等查看答案及解析
-
在反应
中,若7 g A和一定量B完全反应生成8.5 g C,则A、B、C的摩尔质量之比为( )
A.
B.
C.
D.无法确定
难度: 中等查看答案及解析
-
有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如图实验,从实验可以判断:( )

A.该固体粉末中一定不含有BaCl2
B.该固体粉末中一定含有KNO3
C.它的组成可能是CaCO3、BaCl2、Na2SO4
D.它的组成一定是CaCO3、Na2SO4、KNO3
难度: 中等查看答案及解析