-
下列物质与危险化学品标志的对应关系不正确的是( )
A
B
C
D
乙醇
天然气
浓硫酸
氢氧化钠

A.A B.B C.C D.D
难度: 简单查看答案及解析
-
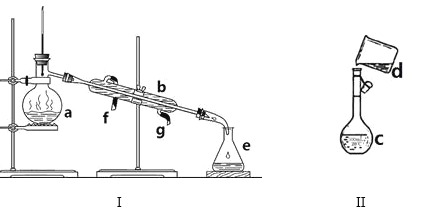
化学是以实验为基础的学科,化学实验设计和操作中必须十分重视安全问题和环境保护问题。下列操作不是围绕上述问题的是 ( )
A. 用氯酸钾和二氧化锰制氧气时用排水法收集后,应从水中撤出导管后再停止加热
B. 在氢气还原氧化铜停止加热后,还要继续通一会儿氢气
C. 实验室制备CO气体必须在通风橱中进行
D. 一些有机溶剂极易被引燃,使用时必须远离明火和热源,用毕立即塞紧瓶塞
难度: 简单查看答案及解析
-
下列分离和提纯的实验操作中,正确的是
A.
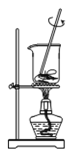 蒸发 B.
蒸发 B. 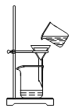 过滤
过滤C.
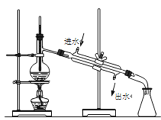 蒸馏 D.
蒸馏 D. 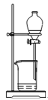 分液
分液难度: 简单查看答案及解析
-
现有三组混合液:①苯和水 ②乙醇和丁醇 ③单质溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
难度: 简单查看答案及解析
-
下列溶液中的Cl-与20mL1.0mol•L-1NaCl溶液中的Cl-物质的量浓度相等的是
A.1mL0.5mol•L-1CuCl2溶液 B.5mL0.4mol•L-1FeCl3溶液
C.10mL2.0mol•L-1KCl溶液 D.10mL1.0mol•L-1MgCl2溶液
难度: 简单查看答案及解析
-
阿伏加德罗常数的值为NA,下列叙述中错误的是( )
①标准状况下,2.24 L水中含有0.1 NA个水分子
②常温常压下,32g SO2 含有的分子数约为3.01×1023
③2 mol NaOH的摩尔质量为80g/mol
④H2的气体摩尔体积约为22.4L/mol
⑤标况下,22.4L由N2和N2O组成的混合气体中,所含有的氮原子的物质的量为2mol
⑥2mol/L的CaCl2溶液中Cl-的数目为4NA
⑦常温常压下,1mol氦气含有的原子数为NA
⑧11.2 L氯气中含有 NA个氯原子
A. ①③④⑥⑧ B. ①④⑤⑥⑧ C. ①②④⑥⑧ D. ②③④⑤⑦
难度: 困难查看答案及解析
-
下列实验操作中正确的是( )
A.蒸发操作时,应使溶液中的溶剂完全蒸干后,才能停止加热
B.蒸馏操作时,应把温度计的水银球插入溶液中
C.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水的大
难度: 中等查看答案及解析
-
10 g 10%的氢氧化钠溶液稀释成50 mL,所得氢氧化钠溶液的物质的量浓度为
A.0.02 mol·L-1 B.0.05 mol·L-1
C.0.25 mol·L-1 D.0.5 mol·L-1
难度: 简单查看答案及解析
-
同温同压下,相同体积的CO和N2具有相同的
①分子数 ②质量 ③原子数 ④物质的量 ⑤密度
A.②④ B.①②④ C.①②③④⑤ D.①②③⑤
难度: 中等查看答案及解析
-
取100 mL 1.0mol·L-1和200 mL 2.0 mol·L-1的盐酸混合后,全部注入500 mL的容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是
A.0.5 mol·L-1 B.1.0 mol·L-1 C.1.5mol·L-1 D.2.0 mol·L-1
难度: 简单查看答案及解析
-
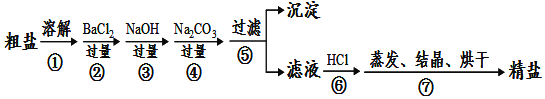
实验室进行NaCl溶液蒸发结晶时,一般有以下操作过程
①固定铁圈位置 ②放置酒精灯 ③放上石棉网 ④放上蒸发皿
⑤加热搅拌⑥停止加热.余热蒸干,其正确的操作顺序为
A.①②③④⑤⑥ B.②①③④⑤⑥ C.②①④⑤⑥ D.②①③④⑤
难度: 简单查看答案及解析
-
对于某些离子的检验及结论一定正确的是
A.向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32-
B.向某溶液中加入BaCl2溶液有白色沉淀产生,再加稀硝酸,沉淀不消失,则原溶液中一定有Ag+
C.向某溶液中先加入盐酸酸化,没有明显现象,再加入BaCl2溶液,有白色沉淀产生,则原溶液中一定有SO42-
D.向某溶液中加入碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,则原溶液一定有Ba2+
难度: 中等查看答案及解析
-
同温同压下,xg的甲气体和yg的乙气体占有相同的体积,根据阿伏加德罗定律判断,下列叙述错误的是
A.甲与乙的相对分子质量之比等于x:y
B.等质量的甲与乙的分子个数之比等于x:y
C.同温同压下甲与乙的密度之比等于x:y
D.同温同体积下等质量的甲与乙的压强之比等于y:x
难度: 中等查看答案及解析
-
相同质量的SO2和SO3,它们之间的关系正确的是
A.所含硫原子的物质的量之比为1:1
B.所含硫元素的质量比为5:4
C.所含氧元素的质量比为4:5
D.所含氧原子的物质的量之比为3:2
难度: 中等查看答案及解析
-
在标准状况下有:①6.72LCH4,②3.01×1023个HCl分子,③13.6gH2S,④0.2molNH3。下列对这四种气体的描述不正确的是( )
A.体积②>③>①>④ B.密度②>③>④>①
C.质量②>③>④>① D.氢原子个数①>③>④>②
难度: 中等查看答案及解析
-
浓度均为1mol/L的KCl、CuCl2、AlCl3三种溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3:2:1时,所用KCl、CuCl2、AlCl3三种溶液的体积比为
A.9:6:2 B.9:3:1 C.6:3:2 D.6:3:1
难度: 中等查看答案及解析