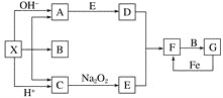
-
把5%的碳酸钠溶液蒸发掉64.3 g水后,溶液变为31 mL,浓度变为14%,没有晶体析出,则浓缩后碳酸钠溶液的物质的量浓度为( )
A. 8.52 mol·L-1 B. 4.26 mol·L-1
C. 1.52 mol·L-1 D. 3.04 mol·L-1
难度: 中等查看答案及解析
-
下列关于蒸馏实验操作说法中,不正确的是( )
A. 蒸馏是利用液态物质沸点不同将其混合物分离的实验方法
B. 蒸馏时,混合物中沸点低的物质先气化逸出,再冷凝变为液体
C. 蒸馏可用来分离各种沸点不同的液态或固态混合物
D. 用蒸馏的方法可以除去混合物中沸点低、易挥发的杂质
难度: 简单查看答案及解析
-
科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10—9m)恢复了磁性,其结构和性质与人体内的血红素及植物内的叶绿素非常相似。下列关于“钴酞菁”分子的说法中正确的是
A.“钴酞菁”分子在水中所形成的分散系属悬浊液
B.“钴酞菁”分子既能透过滤纸,也能透过半透膜
C.“钴酞菁”分子在水中形成的分散系能产生丁达尔现象
D.在分散系中,“钴酞菁”分子直径比Na+的直径小
难度: 中等查看答案及解析
-
在标准状况下,密度最小的气体是( )
A.NO2 B.SO2 C.O2 D.CH4
难度: 简单查看答案及解析
-
在xR2++yH++O2=mR3++nH2O的离子方程式中,对系数m和R3+的判断正确的是
A.m=4;R3+是还原剂 B.m=y;R3+是氧化产物
C.m=2;R3+是氧化剂 D.m=y;R3+是还原产物
难度: 简单查看答案及解析
-
飘尘是物质燃烧时产生的粒状漂浮物,颗粒很小,不易沉降。它与空气中的SO2和O2接触时,SO2会部分转化为SO3,使空气的酸度增加,环境污染更为严重。其中飘尘所起的作用可能是
A.氧化剂 B.还原剂 C.催化剂 D.载体
难度: 简单查看答案及解析
-
下列有关试剂的保存方法错误的是( )
A. 氢氧化钠溶液保存在具有玻璃塞的试剂瓶中
B. 少量的钠保存在煤油中
C. 硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中
D. 浓硝酸保存在棕色玻璃试剂瓶中
难度: 中等查看答案及解析
-
下列各组物质,前者逐滴滴加到后者中至过量,先出现白色沉淀,后来沉淀又全部消失的是( )
A.硫酸滴加到偏铝酸钠溶液中
B.氢氧化钡溶液滴加到硫酸铝溶液中
C.氨水滴加到硫酸铝溶液中
D.硫酸铝溶液滴加到氢氧化钠溶液中
难度: 中等查看答案及解析
-
下列反应中不是氧化还原反应的是
A. 3Cl2+6KOH===5KCl+KClO3+3H2O
B. CuO+H2
Cu+H2O
C. 2KMnO4
K2MnO4+MnO2+O2↑
D. 2AgNO3+BaCl2===2AgCl↓+Ba(NO3)2
难度: 简单查看答案及解析
-
amol O2和amol O3相比较一定相同的是( )
A. 体积 B. 原子数 C. 分子数 D. 质量
难度: 简单查看答案及解析
-
离子方程式CO32—+2H+=CO2↑+H2O可表示( )
A.碳酸盐与盐酸之间的反应 B.一切碳酸盐与一切酸之间的反应
C.可溶性碳酸盐与酸之间的反应 D.可溶性碳酸盐与强酸之间的反应
难度: 简单查看答案及解析
-
下列有关气体摩尔体积的描述中,正确的是( )
A. 单位物质的量的气体所占的体积就是气体摩尔体积
B. 气体摩尔体积一定是22.4L·mol-1
C. 1 mol气体体积为22.4L,则一定是标准状况
D. 相同物质的量的气体摩尔体积也相同
难度: 简单查看答案及解析
-
实验室中需要配制2 mol·L-1的NaCl溶液950mL,配制时应选用的容量瓶的规格和称量的NaCl的质量分别是( )
A.950mL,111.2g B.500mL,117g C.1000 mL,l17g D.任意规格,117g
难度: 简单查看答案及解析
-
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的 水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能是 ( )
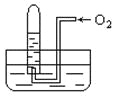
A.N2与NO2的混和气体 B.O2与NO2的混和气体
C.NO与NO2的混和气体 D.NO2一种气体
难度: 简单查看答案及解析
-
对纯碱(碳酸钠)采用不同分类法分类:①碱、②含氧酸盐、③钠盐、④碳酸盐,其中正确的是( )
A.①②③ B.①③④ C.①②④ D.②③④
难度: 简单查看答案及解析
-
下列离子方程式正确的是( )
A.稀硝酸与氢氧化钙溶液反应:H++OH-=H2O
B.铝与稀盐酸反应:Al+2H+=Al3++H2↑
C.铁与稀硫酸反应:2Fe+6H+=2Fe2++3H2↑
D.碳酸钠溶液与稀盐酸反应:CO32-+H+=H2O+CO2↑
难度: 简单查看答案及解析
-
氮化铝(AlN,Al和N的相对原子质量分别为27和14)广泛用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C
2AlN+3CO合成。下列叙述正确的是( )
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1mol AlN需转移3mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41g
难度: 中等查看答案及解析
-
下列关于酸、碱、盐的说法中正确的是( )
A.酸根中不可能含有氧元素 B.能与碱发生反应生成水的化合物是酸
C.电离时有金属阳离子产生的化合物一定是盐 D.酸不可能电离产生金属阳离子
难度: 中等查看答案及解析
-
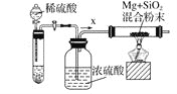
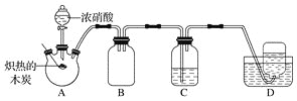
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
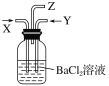
①洗气瓶中产生的沉淀中有碳酸钡
②在Z导管出来的气体中无二氧化碳
③洗气瓶中产生的沉淀是硫酸钡
④在Z导管口有红棕色气体出现
A.①② B.③④ C.①④ D.②③
难度: 中等查看答案及解析
-
为确定某溶液中是否存在Cl﹣、SO42-和CO32-,进行如下实验:
①取少量溶液滴加Ba(NO3)2溶液,产生白色沉淀。
②然后继续加入稀盐酸至溶液呈酸性,产生无刺激性气味且能使澄清石灰水变浑浊的气体;白色沉淀部分溶解。
③取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。
根据实验,以下推测不正确的是( )
A.一定有SO42- B.一定有CO32-
C.不能确定Cl﹣是否存在 D.不能确定SO42-是否存在
难度: 简单查看答案及解析
-
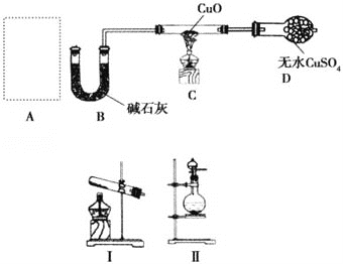
小王要制备纯净的二氧化碳气体,可供选用的仪器如图所示。可供选用的药品如下:①石灰石②澄清石灰水③稀硫酸④浓硫酸⑤盐酸溶液⑥烧碱溶液⑦蒸馏水。下列装置连接顺序及组合最恰当的是( )
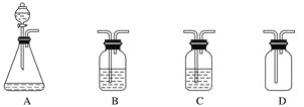
A. A(①⑤)、B(④)、C(⑦)、D B. A(①③)、B(④)、C(⑦)、D
C. A(①⑤)、B(⑦)、C(④)、D D. A(①⑤)、B(⑥)、C(④)、D
难度: 中等查看答案及解析
-
自来水厂常用氯气对生活用水进行杀菌消毒。市场上有些不法商贩为牟取暴利,用这样的自来水冒充纯净水(离子的浓度非常低)出售,给人们的生活造成了一定的不良影响。在下列化学试剂中,可以用于鉴别这种自来水和纯净水的是( )
A.酚酞溶液 B.氯化钡溶液 C.氢氧化钠溶液 D.硝酸银溶液
难度: 简单查看答案及解析
-
下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是( )
A. 浓硫酸的体积增大 B. 铝的表面生成致密的薄膜
C. 澄清的石灰水变浑浊 D. 氢氧化钠的表面发生潮解
难度: 中等查看答案及解析
-
下列说法不正确的是
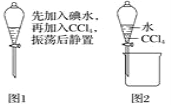
A. 从碘水中提取单质碘时,不能用无水乙醇代替四氯化碳
B. 进行如图1操作后,实验现象为液体分层,下层呈无色
C. 利用如图2装置可以分离四氯化碳和水
D. 萃取操作时,应选择有机萃取剂,且萃取剂不溶于水
难度: 中等查看答案及解析
-
在标准状况下,将NO、NO2、O2三种气体按一定比例充满一固定容积的容器,并将该容器倒置在水槽中,充分反应后,容器中无气体剩余,所得溶液的浓度为Mmol/L。则M的取值范围是
A.0<M<1/22.4 B.1/39.2<M<1/22.4
C.1/28<M<1/22.4 D.1/39.2<M<1/28
难度: 中等查看答案及解析