-
在科学史上每一次重大的发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于
A. 开发了合成氨的生产工艺
B. 提出了元素周期律
C. 揭示了燃烧的本质
D. 提取了治疟药物青蒿素
难度: 简单查看答案及解析
-
钾和钠的化学性质相似。下列说法能最好地解释这个事实的是
A.都是金属元素 B.原子半径相差不大
C.最外层电子数相同 D.电子层数相同
难度: 简单查看答案及解析
-
决定化学反应速率的主要因素是
A.反应物的浓度 B.是否使用合适的催化剂
C.外界温度的高低 D.反应物的本身性质
难度: 简单查看答案及解析
-
实验室用锌粒与2mol/L硫酸溶液制取氢气,下列措施不能增大化学反应速率的是
A.用锌粉代替锌粒 B.改用3mol/L硫酸溶液
C.改用热的2mol/L硫酸溶液 D.向该硫酸溶液中加入等体积的水
难度: 简单查看答案及解析
-
2017年诺贝尔化学奖授予用冷冻电镜测定分子结构的科学家。下列物质由分子构成的是
A.氯化钠 B.铜 C.水 D.金刚石
难度: 简单查看答案及解析
-
在农业上常用于辐射育种。该原子的质子数是
A.27 B.33 C.60 D.87
难度: 简单查看答案及解析
-
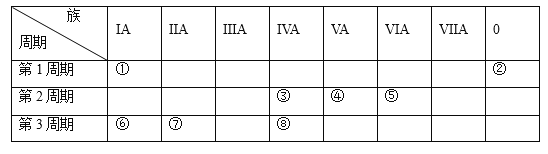
某元素原子的最外层电子数是内层电子数的3倍,该元素是
A.C B.Si C.O D.S
难度: 简单查看答案及解析
-
元素X的原子有3个电子层,最外层电子数是5。这种元素位于周期表
A.第4周期ⅢA族 B.第4周期 ⅦA族
C.第3周期ⅤB族 D.第3周期ⅤA族
难度: 简单查看答案及解析
-
下列物质是离子化合物的是
A.H2O B.NH3·H2O C.C60 D.NaCl
难度: 简单查看答案及解析
-
在元素周期表中最容易找到半导体材料的合理位置是
A.金属元素和非金属元素交界处 B.过渡元素区
C.周期表的右上角 D.周期表的左下角
难度: 简单查看答案及解析
-
下列有关说法不正确的是
A.元素周期表中有7个主族、7个副族
B.稀有气体元素原子的最外层电子数均为8
C.氢是原子半径最小的元素
D.硫元素位于第3周期ⅥA族
难度: 简单查看答案及解析
-
Na与Na+两种粒子中,相同的是
A.化学性质 B.质子数 C.最外层电子数 D.核外电子层数
难度: 简单查看答案及解析
-
下列化学用语表示不正确的是
A.苏打的化学式为:NaHCO3
B.水的结构式:H—O—H
C.硫原子结构示意图:
D.氯化氢的电子式:
难度: 简单查看答案及解析
-
下列物质中,既有离子键,又有共价键的是
A.KCl B.Ba(OH)2 C.H2O D.CH4
难度: 简单查看答案及解析
-
用下列方法制取氢气,反应速率最大的是
A.冬天,块状锌与2 mol·L一1硫酸溶液反应
B.冬天,粉末状锌与2 mol·L一1硫酸溶液反应
C.夏天,块状锌与2 mol·L一1硫酸溶液反应
D.夏天,粉末状锌与2mol·L一1硫酸溶液反应
难度: 简单查看答案及解析
-
下列反应中,属于吸热反应的是
A.碳酸钙高温分解 B.金属钠与水反应
C.盐酸与氢氧化钠溶液反应 D.氢气在氧气在燃烧
难度: 简单查看答案及解析
-
科学家使用普通氧分子和带正电的氧离子可以制造出一种含有四个氧原子的新型氧分子,利用质谱仪探测可以证实它的存在。你认为下列说法正确的是
A.该分子带2个单位正电荷
B.该分子构成的物质与臭氧是同一种物质
C.该分子是一种新的氧化物分子
D.该物质与氧气、臭氧互称为同素异形体
难度: 简单查看答案及解析
-
己知反应X+Y=M+N为放热反应,下列有关说法中正确的是
A.X的能量一定低于M B.X和Y的总能量一定高于M和N的总能量
C.Y的能量一定低于N D.该反应一定不需要加热就能发生
难度: 简单查看答案及解析
-
下列物质互为同分异构体的一组是
A.35 Cl和37 Cl B.O2 和O3
C.CH3CH2OH和CH3OCH3 D.CH4和C2H6
难度: 简单查看答案及解析
-
某元素的气态氢化物的化学式H2X,该元素最高价氧化物对应水化物的化学式是
A.HXO3 B.H3XO4 C.H2XO3 D.H2XO4
难度: 简单查看答案及解析
-
N2+3H2
 2NH3是工业上制造氮肥的重要反应。下列有关说法不正确的是
2NH3是工业上制造氮肥的重要反应。下列有关说法不正确的是A.增加N2的浓度能加快反应速率
B.升高体系温度能加快反应速率
C.使用合适的催化剂能加快反应速率
D.若增大N2的浓度可以使H2的转化率达到100%
难度: 简单查看答案及解析
-
某兴趣小组设计的简易原电池装置如下图所示。该电池工作时,下列说法不正确的是
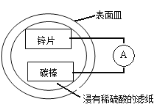
A.锌片作负极
B.碳棒上有气泡产生
C.电子由锌片经导线流向碳棒
D.可将电能转化为化学能
难度: 简单查看答案及解析
-
短周期主族元素X、Y、Z、W的原子序数依次增大。X、Z所在的族序数等于周期数,Y与W同主族,X、Z原子的核外电子数之和与Y、W原子的核外电子数之和的比为7∶12。下列说法正确的是
A.原子半径:r(X)< r(Y)< r(Z)< r(W)
B.Z的氧化物能溶于W最高价氧化物的水化物
C.W的简单气态氢化物的热稳定性比Y的强
D.X、Y、Z形成的化合物为强碱
难度: 中等查看答案及解析