-
临近中考,小明为自己制定了如下食谱.主食:米饭;副食:红烧牛肉、清蒸鱼、花生米;饮料:牛奶.从均衡营养的角度我们建议在小明的食谱中,应该增加下列哪项食物( )
A.炒鸡蛋 B.煎豆腐 C.糖醋排骨 D.凉拌黄瓜
难度: 简单查看答案及解析
-
化学是你,化学是我,化学深入我们生活,下列说法正确的是( )
A.铵态氮肥与熟石灰混合使用可以明显提高肥效
B.回收各种废弃材料,能有效解决“白色污染”问题
C.腌制的泡菜虽然富含亚硝酸盐,但多吃无妨
D.焊接金属时用氧气作保护气
难度: 简单查看答案及解析
-
稀盐酸是化学实验中常用的试剂,但下列实验中,不宜使用稀盐酸的是( )
A.除去氯化钠溶液中的碳酸钠 B.除去铜粉中混有的铁粉
C.除去熟石灰中的石灰石 D.验证金属锌和铁的活动性顺序
难度: 中等查看答案及解析
-
下列对实验现象和结论描述都正确的是( )
A.打开浓盐酸瓶口产生白烟,说明盐酸具有挥发性
B.二氧化碳通入紫色石蕊试液中,溶液变红,说明二氧化碳具有酸性
C.硫在空气中燃烧发出明亮的蓝紫色火焰,说明硫具有可燃性
D.滴有品红的水加入活性炭后变无色,说明活性炭具有吸附性
难度: 简单查看答案及解析
-
推理是学习化学的一种重要方法,下列推理正确的是( )
A.氧化物中含有氧元素,所以含有氧元素的化合物都是氧化物
B.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小
C.碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
难度: 中等查看答案及解析
-
在“P+Q→盐和水”的反应中,物质P和Q不可能是
A.HCl,Ca(OH)2 B.SO2,NaOH C.Fe2O3,H2SO4 D.H2SO4,ZnCl2
难度: 中等查看答案及解析
-
下列离子组在强酸性和强碱性溶液中都能大量共存的是( )
A.Ca2+、Cu2+、NO3-、Cl-
B.Na+、Mg2+、SO42-、Cl-
C.Na+、Ba2+、Cl-、NO3-
D.Na+、K+、CO32-、SO42-
难度: 中等查看答案及解析
-
甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
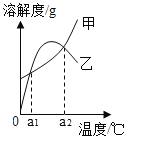
A.a1℃时甲的饱和溶液,升温至a2℃时仍是饱和溶液
B.乙的溶解度随温度的升高而增大
C.相同温度时,甲的溶解度一定大于乙的溶解度
D.分别将甲、乙的饱和溶液从a2℃将至a1℃时,所得溶液中溶质的质量分数相等
难度: 中等查看答案及解析
-
在氯化铜和氯化亚铁的混合溶液中加入一定的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是()
A.滤出的固体中一定含有铜,可能含有铁和镁
B.滤出的固体中一定含有铜,一定不含有铁和镁
C.滤液中一定含有氯化镁和氯化亚铁,一定没有氯化铜
D.滤液中一定含有氯化镁、氯化亚铁、氯化铜
难度: 困难查看答案及解析
-
下列除杂(括号内为杂质)设计,所选试剂和操作方法均正确的是( )
选项
物质
所选试剂
操作方法
A
HCl气体(H2O)
固体氢氧化钠
通过装有试剂的干燥管,收集
B
CaCl2溶液(HCl)
碳酸钙粉末
加过量试剂,充分反应,过滤
C
KNO3溶液(CuSO4)
Ba(OH)2溶液
加过量试剂,充分反应,过滤
D
CaCO3固体(CaCl2)
水
加足量试剂,溶解、过滤、蒸发结晶
A.A B.B C.C D.D
难度: 困难查看答案及解析
-
下列各组溶液,只用组内物质不能鉴别的是( )
A.NaNO3 KCl Na2CO3 HCl
B.HCl Na2CO3 K2SO4 BaCl2
C.MgSO4 KOH KNO3 CuSO4
D.KOH MgCl2 H2SO4 NH4Cl
难度: 困难查看答案及解析
-
下列图象中能正确表示其变化过程的是( )
A.向pH=10的KOH溶液中不断加水稀释
B.用一定质量的KClO3和MnO2的混合物制取O2
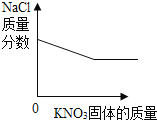
C.向FeCl3和HNO3的混合溶液中加入NaOH溶液直至过量
D.20℃时,向一定质量的NaCl溶液中加入KNO3固体
A.A B.B C.C D.D
难度: 中等查看答案及解析