-
下列说法错误的是 ( )
A.液氯是氯气的水溶液
B.铝是活泼的金属,其合金抗腐蚀能力强
C.AgI和干冰都可用于人工降雨
D.钠的还原性强,可以用来冶炼金属钛、锆、铌等
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数。下列说法正确的是( )
A.同温同压同体积的卤素单质所含原子个数相等
B.常温常压下,11.2LO2所含的氧原子数为NA
C.1molFeCl3跟水反应完全转化成氢氧化铁胶体后,生成胶体粒子的数目为NA
D.铝热反应中,1molFe2O3参与反应得到的电子数为6NA
难度: 简单查看答案及解析
-
化学概念在逻辑上存在如图所示的关系,下列说法正确的是( )
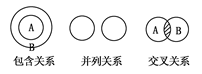
A.纯净物与混合物属于包含关系
B.化合物与氧化物属于包含关系
C.单质与化合物属于交叉关系
D.氧化还原反应与化合反应属于并列关系
难度: 简单查看答案及解析
-
将9.2g金属钠投入到足量水中,得ag溶液;9.6g镁投入到足量盐酸中(与水等质量),得到bg溶液,则反应后两溶液质量的关系是 ( )
A.a>b B.a=b C.a<b D.无法判断
难度: 简单查看答案及解析
-
在生活、生产及化学研究中,人们经常需要根据不同原子、分子或离子的某些特征应对物质进行检验,以确定物质的组成。下列有关物质检验的说法正确的是( )
A.MnO2、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸不能将它们区别开
B.(NH4)2SO4、K2SO4、NH4C1三种物质不能用一种试剂通过化学反应区别开
C.可以用焰色反应来检验氯化钾固体和氯化钠固体
D.用湿润的KI淀粉试纸可以检验溴蒸气中是否含有氯气
难度: 简单查看答案及解析
-
我国所生产的碘盐中含有少量的碘酸钾(KIO3),以补充人体所需的碘元素而预防甲状腺疾病,而核应急专用碘片中含有的主要成分是碘化钾(KI),食用一定的碘片可以阻止放射性碘被人体甲状腺所吸收,那碘化钾中碘元素的化合价为( )
A.+5 B.+1 C.—5 D.—1
难度: 简单查看答案及解析
-
下列各项比较中,正确的是( )
A.含碳量:生铁>钢 B.熔点:铁<汞
C.氢氧化钙的溶解度:80℃>20℃ D.核外电子数:钠原子<钠离子
难度: 简单查看答案及解析
-
下列物质一定有固定熔沸点的是( )
A.C5H10 B.CH3Cl C.C2H4Cl2 D.C2H4O2
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A.溶液和胶体的本质区别是有无丁达尔效应
B.玻璃、水泥和光导纤维的主要成分都是硅酸盐
C.常用危险化学品酒精和甲烷的标志都是易燃液体
D.氧化钠和过氧化钠含有的化学键种类不完全相同
难度: 简单查看答案及解析
-
下列说法正确的是( )
A.同周期相邻主族原子序数一定相差一
B.生石灰与水混合的过程只发生物理变化
C.O3是由3个氧原子构成的化合物
D.可用丁达尔效应区分溶液与胶体
难度: 简单查看答案及解析
-
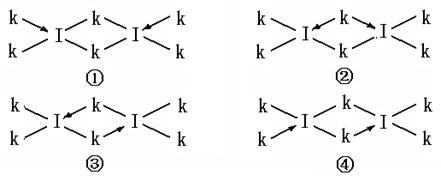
一定条件下硝酸铵受热分解的未配平化学方程式为:NH4NO3 - HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为( )
A.5∶3 B.5∶4 C.1∶1 D.3∶5
难度: 简单查看答案及解析
-
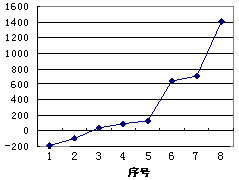
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中可能含有的阳离子是( )
A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
难度: 简单查看答案及解析
-
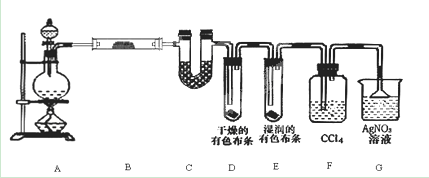
如图,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象;当打开B阀后,C处红布条逐渐褪色。则D瓶中装的是 ( )

A.浓盐酸 B.NaOH溶液
C.H2O D.饱和NaCl溶液
难度: 简单查看答案及解析
-
下列有关实验的操作及描述正确的是( )
A.可以利用烧碱溶液除去混在MgO中的Al2O3
B.用四氯化碳萃取碘水中的碘单质,上层显紫红色
C.将Fe(OH)3沉淀溶于沸水可制得Fe(OH)3胶体
D.测定Na2CO3溶液的pH值,操作时应将先pH试纸润湿
难度: 简单查看答案及解析
-
在FeCl3、CuCl2和HCl的混合液中加入铁粉,待反应结束,所剩固体滤出后不能被磁铁吸引,则反应后溶液不可能大量存在的阳离子是( )
A.H+ B.Fe3+ C.Fe2+ D.Cu2+
难度: 简单查看答案及解析
-
无色透明的强酸性溶液中,能大量共存的离子组是( )
A.CO32-、Br-、K+、Na+ B.NH4+、SO42-、Cl-、NO3-
C.K+、Na+、ClO-、Cl- D.K+、SO42-、HCO3-、Mg2+
难度: 简单查看答案及解析
-
配制100mL1.0mol·L-1的NaOH溶液,下列情况不会影响溶液浓度的是( )
A.容量瓶使用前有蒸馏水
B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒
C.俯视确定凹液面与刻度线相切
D.称量NaOH固体时使用了称量纸
难度: 简单查看答案及解析
-
碘(ICl)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,能与许多非金属单质反应生成相应卤化物,能与水反应等。其与水反应的方程式为ICl+H2O
HCl+HIO。 下列关于ICl的叙述中不正确的是( )
A.ICl是一种有色物质
B.在许多反应中ICl是强氧化剂
C.在ICl与水的反应中,它既是氧化剂又是还原剂
D.与NaOH溶液反应生成的产物中有NaIO和NaCl
难度: 简单查看答案及解析