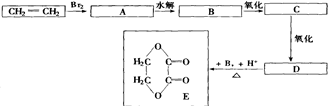
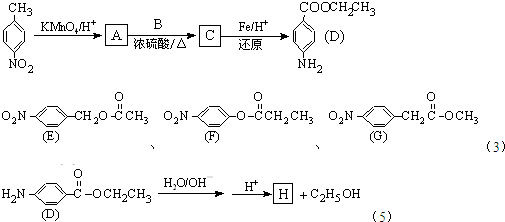
-
甲烷中混有乙烯,欲除去乙烯,得到纯净的甲烷,最好依次通过的试剂瓶为( )
A.澄清石灰水,浓H2SO4
B.酸性KMnO4溶液,浓H2SO4
C.溴水,浓H2SO4
D.浓H2SO4,酸性KMnO4溶液难度: 中等查看答案及解析
-
鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性.已知角鲨烯分子中含有30个碳原子及6个C=C且不含环状结构,则其分子式为( )
A.C30H60
B.C30H56
C.C30H52
D.C30H50难度: 中等查看答案及解析
-
已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
A.2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l);△H=-4b kJ/mol
B.C2H2(g)+O2(g)→2CO2(g)+H2O(l);△H=2b kJ/mol
C.2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l);△H=-2b kJ/mol
D.2C2H2(g)+5O2(g)→4CO2(g)+2H2O(l);△H=b kJ/mol难度: 中等查看答案及解析
-
下列四个反应中,与其它三个反应类型不同的是( )
A.CH3CHO+2Cu(OH)2CH3COOH+Cu2O↓+2H2O
B.CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag↓+3NH3+H2O
C.CH3CHO+H2CH3CH2OH
D.CH3CHO+CuOCH3COOH+Cu
难度: 中等查看答案及解析
-
下列描述中,不符合生产实际的是( )
A.电解法精炼粗铜,用纯铜作阴极
B.电解熔融的氧化铝制取金属铝,用铁作阳极
C.在镀件上电镀锌,用锌作阳极
D.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极难度: 中等查看答案及解析
-
用惰性电极电解下列各溶液,经一段时间后,溶液的浓度增大,而溶液pH值保持不变的是( )
A.CuCl2溶液
B.NaCl溶液
C.H2SO4溶液
D.Na2SO4溶液难度: 中等查看答案及解析
-
实验室为除去苯中含有的少量苯酚,通常采用的方法是( )
A.加氢氧化钠溶液,用分液漏斗分离
B.加乙醇,用分液漏斗分离
C.加热蒸馏,用分馏法分离
D.加浓溴水,用过滤法分离难度: 中等查看答案及解析
-
用两根铜棒做电极,电解硝酸银溶液,跟电源正极相连的一极发生的电极反应是( )
A.Cu-2e-=Cu2+
B.4OH--4e-=2H2O+O2↑
C.2H++2e-=H2↑
D.Ag++e-=Ag难度: 中等查看答案及解析
-
塑料制品废弃物严重污染环境,常称为“白色污染”.为了防止这种污染,一条重要途径是将合成高分子化合物重新变成小分子化合物.目前,对结构为
OCH2CH2OOC-
-CO
的物质已成功实现了这种处理.试分析,若用CH3OH来处理它,得到的有机物可能是( )
A.
B.HOCH2CH2COOH
C.-COOH
D.CH3OOC--COOCH3
难度: 中等查看答案及解析
-
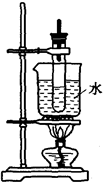
按右图的装置进行电解实验:A极是铜锌合金,B极为纯铜,电解质中含有足量的铜离子.通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A合金中Cu、Zn原子个数比为( )
A.1:3
B.3:1
C.2:1
D.任意比难度: 中等查看答案及解析
-
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.下列叙述正确的是( )
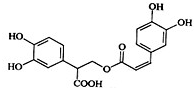
A.迷迭香酸属于芳香烃
B.1mol迷迭香酸最多能和含6mol Br2的浓溴水反应
C.迷迭香酸可以发生水解反应、取代反应和酯化反应
D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应难度: 中等查看答案及解析
-
菜刀上沾有食盐水后,置于空气中一段时间会生锈,其原理是( )
正极 负极 A Fe-2e=Fe2+ 2H2O+O2+4e=4OH- B 2H++2e=H2↑ Fe-2e=Fe2+ C 2H2O+O2+4e=4OH- Fe-3e=Fe3+ D 2H2O+O2+4e=4OH- Fe-2e=Fe2+
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
某学生做乙醛的还原性实验时,取1mol/L CuSO4溶液和0.5mol/L NaOH溶液各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL 40%的乙醛,结果无红色沉淀出现.导致该实验失败的原因可能是( )
A.未充分加热
B.加入乙醛太少
C.加入NaOH溶液的量不够
D.加入CuSO4溶液的量不够难度: 中等查看答案及解析
-
某原电池总反应为2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质溶液为FeCl3
B.正极为C,负极为Fe,电解质溶液为Fe(NO)3
C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3
D.正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3难度: 中等查看答案及解析
-
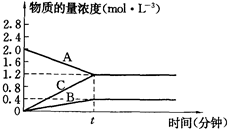
将 4mol A气体和 2mol B气体在 2L 固定体积的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)⇌2C(g).若经2s后测得 C 的浓度为 0.6mol•L-1,现有下列几种说法,其中正确的是( )
A.用物质A表示的反应的平均速率为0.3mol•L-1•s-1
B.用物质B表示的反应的平均速率为0.6mol•L-1•s-1
C.2s时物质A的转化率为70%
D.2s时物质B的浓度为0.7mol•L-1难度: 中等查看答案及解析