-
下列有关溶液的说法正确的是( )
A.蒸干溶液均能得到固体
B.只含一种溶质的溶液为纯净物
C.溶液的均一性是指溶液中各处的浓度相同
D.溶液的稳定性是指溶液不与其他物质发生反应
难度: 简单查看答案及解析
-
下列有关溶液的说法中,正确的是( )
A. 溶液都是无色的
B. 将NaCl放入植物油中搅拌,能形成溶液
C. 将40%的NaOH溶液均分成两份,每份溶液的溶质质量分数都为20%
D. 溶液是稳定的混合物
难度: 简单查看答案及解析
-
下列与洗涤有关的做法不合理的是
A.用洗洁精洗去餐具上的油污
B.用汽油洗去沾在衣服上的油渍
C.用白醋洗去水壶中的水垢(水垢的主要成分是碳酸钙和氢氧化镁)
D.用纯碱溶液洗去铁制品表面的铁锈
难度: 简单查看答案及解析
-
压强为101kPa下,硝酸钾和氨气在不同温度下的溶解度如下表。下列说法正确的是
温度/℃
10
20
30
60
溶解度/g
KNO3
20.9
31.6
45.8
110
NH3
70
56
44.5
20
A.两种物质的溶解度均随温度升高而增大
B.20℃时, KNO3饱和溶液中溶质的质量分数为31.6%
C.60℃的KNO3饱和溶液降温至30℃,有晶体析出
D.NH3的溶解度与压强大小无关
难度: 困难查看答案及解析
-
下列物质不是溶液的是( )
A.食醋 B.泥浆 C.生理盐水 D.澄清石灰水
难度: 简单查看答案及解析
-
下列物质溶解或稀释过程中,溶液温度没有明显改变的是( )
A.NaOH B.NH4NO3 C.浓硫酸 D.NaCl
难度: 简单查看答案及解析
-
如图,将红砂糖倒入一杯开水中,充分溶解。能作为判断砂糖水是饱和溶液的依据是( )
A.砂糖水颜色很深 B.砂糖水味道很甜
C.砂糖溶解得很快 D.砂糖固体有剩余
难度: 简单查看答案及解析
-
(2019河南逆袭卷)实验室需配制标签如图所示的氯化钠注射液。则下列说法不正确的是( )
氯化钠注射液
[成分]氯化钠 水
[规格]1000 mL质量分数0.9%
[密度]1.0 g/cm3
A.配制该注射液的步骤为计算、称量、溶解、量取、装瓶
B.配制该注射液需要氯化钠9 g
C.若量取水时仰视读数,会使所得溶液的溶质质量分数小于0.9%
D.将配制的该溶液稀释为0.5%的氯化钠溶液,需要加水的体积为800 mL
难度: 简单查看答案及解析
-
KNO3 的溶解度曲线如下图所示。下列说法错误的是( )

A.0~60℃,KNO3 的溶解度随温度升高而增大
B.60℃时的 KNO3 饱和溶液降温至 20℃,有晶体析出
C.20℃,100g 水中最多能溶解 31.6g KNO3
D.60℃时,可配制溶质质量分数为 60%的 KNO3 溶液
难度: 中等查看答案及解析
-
下图是X、Y两种固体物质的溶解度曲线。下列叙述正确的是

A.温度低于t2℃时,物质Y的溶解度小于X
B.X、Y的溶解度都随温度升高而增大
C.a点表示t1℃时X、Y的溶液都、不饱和
D.Y的饱和溶液降低温度后,溶质质量分数不变
难度: 中等查看答案及解析
-
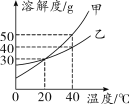
(2019重庆A改编)甲、乙的溶解度曲线如图所示(不考虑水的变化)。下列说法正确的是( )

A.依据溶解度曲线可判断,甲的溶解度比乙的大
B.t2 ℃时,甲的饱和溶液中溶质质量分数为40%
C.t2 ℃时,将甲、乙的饱和溶液分别降温到t1 ℃,析出晶体甲的质量大
D.t2℃时将70 g甲的饱和溶液稀释成20%,需加水的质量为30 g
难度: 简单查看答案及解析
-
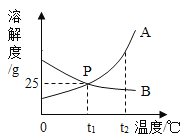
关于如图所示的溶解度曲线,下列说法正确的是( )
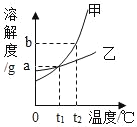
A.t1℃时,甲、乙两种物质的溶液,溶质质量分数相等
B.t1℃时,乙物质的饱和溶液,升高温度溶质质量分数增大
C.t2℃时,甲物质的饱和溶液,降温至t1℃析出晶体(b﹣a)g
D.t2℃时,甲物质饱和溶液的溶质质量分数为
 ×100%
×100%难度: 简单查看答案及解析
-
甲、乙两种固体的溶解度曲线如图所示。将①②两支试管中的甲、乙饱和溶液(均有少量未溶解的固体)放进盛有热水的烧杯里,升高温度后,下列有关说法正确的是( )

A.甲的溶解度大于乙的溶解度 B.①②两溶液均变为不饱和溶液
C.①溶液质量增加,②溶液质量减少 D.①溶液中溶质的质量分数一定大于②溶液
难度: 中等查看答案及解析
-
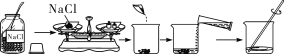
常温下,对100mL氯化钠饱和溶液进行图示实验。下列分析错误的是( )

A.实验1后,甲、乙中溶液的溶质质量分数相等
B.实验2后,乙中比甲中氯化钠的溶解度大
C.实验2后,甲中溶液为氯化钠的不饱和溶液
D.实验2后,甲、乙中溶液所含溶质质量相等
难度: 中等查看答案及解析
-
配制50g质量分数5%的KNO3溶液,作为无土栽培所需的营养液,溶解过程中KNO3的质量分数随时间变化关系如图所示,观察图象,分析形成这种结果的原因是( )
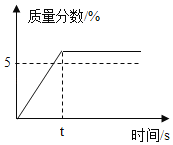
A.所用KNO3固体中含有水分
B.量简量水时俯视刻度线
C.KNO3固体溶解前所用烧杯内有水
D.配好的溶液装瓶时部分液体洒落在试剂瓶外
难度: 中等查看答案及解析
-
如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是( )
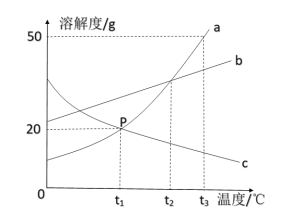
A.t1℃时,a、c两种物质饱和溶液的溶质质量分数为20%
B.将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法
C.将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c
D.将150g a物质的饱和溶液从t3℃降温至t1℃,可析出30g a物质
难度: 中等查看答案及解析
-
在蒸馏水中加入NaOH颗粒,不断搅拌,用温度传感器记录溶解过程的温度变化如图a、c两点观察到溶液中有固体存在,b点固体完全消失。下列说法不正确的是
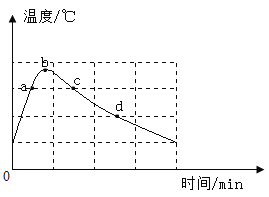
A.NaOH固体溶于水是放热过程
B.a、c两点时,NaOH的溶解度相同
C.b点时,该溶液一定是饱和溶液
D.c点时的溶剂质量等于a点时的溶剂质量
难度: 简单查看答案及解析