-
下列含有非极性键的共价化合物是
A.HCl B.Na2O2 C.C2H2 D.CH4
难度: 中等查看答案及解析
-
五种短周期元素的某些性质如表所示(其中只有W、Y、Z为同周期元素)。
元素代号
X
W
Y
Z
Q
原子半径(×10-12m)
37
71
74
75
186
主要化合价
+1
-1
-2
+5、-3
+1
下列说法正确的是( )
A.由Q与Y形成的化合物中只存在离子键
B.Z与X之间形成的化合物具有还原性
C.由X、Y、Z三种元素形成的化合物,一定是共价化合物
D.Y与W形成的化合物中,Y显负价
难度: 中等查看答案及解析
-
下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是( )
A.CH3CH2CH2CH3 B.CH3CH(CH3)2
C.CH3C(CH3)3 D.(CH3)2CHCH2CH3
难度: 简单查看答案及解析
-
在A(g)+2B(g) ⇌3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A. v(A)=0.5 mol·L-1·s-1
B. v(B)=0.5 mol·L-1·s-1
C. v(C)=0.8 mol·L-1·s-1
D. v(D)=1 mol·L-1·s-1
难度: 中等查看答案及解析
-
生活中遇到的某些现实问题,常常涉及化学知识,下列叙述不正确的是
A.鱼虾会产生令人不愉快的腥臭气味,应当用水冲洗,并在烹调时加入少量食醋
B.“酸可以除锈”“洗涤剂可以去油”都是发生了化学反应
C.被蜂蚁蛰咬会感到疼痛难忍,这是蜂蚁咬人的皮肤时将甲酸注入人体的缘故,此时,若涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛
D.苯酚溶液可用于环境消毒,医用酒精可用于皮肤消毒,其原因均在于可以使蛋白质变性
难度: 中等查看答案及解析
-
下列有关说法正确的是
A.煤的干馏和石油的分馏均属化学变化
B.液化石油气和天然气的主要成分都是甲烷
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.石油裂解可以得到更多的汽油,这种汽油是一种纯净物
难度: 中等查看答案及解析
-
下列叙述中,错误的是( )
A.苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯
B.乙苯能发生氧化反应,但不能发生还原反应
C.乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷
D.苯乙烯在合适条件下催化加氢可生成乙基环己烷
难度: 中等查看答案及解析
-
关于石油的说法中,不正确的是( )
A.石油主要含烃类物质,这些烃类物质随着烃分子含有的碳原子数的增加沸点升高
B.常压分馏得到的汽油是混合物,没有固定的沸点,但石油气为纯净的丙烷
C.石油分馏不是化学变化,但裂化是化学变化
D.裂化的目的是得到轻质油,裂解的目的是得到乙烯、丙烯等化工原料
难度: 中等查看答案及解析
-
在常温常压下,取下列等质量4种气态烃分别在足量的氧气中燃烧其中消耗氧气最多的是( )
A.CH4 B.C2H6 C.C3H8 D.C4H10
难度: 中等查看答案及解析
-
下列化学式只表示一种纯净物的是( )
A.C3H8 B.C4H10 C.C2H4Br2 D.C3H8O
难度: 中等查看答案及解析
-
在一可变容积的密闭容器中进行反应:C(s) + H2O(g)= CO(g) + H2(g),下列条件的改变能使反应速率减慢的是( )
A.增加C的量 B.将容器的体积缩小一半
C.保持体积不变,充入N2,使体系的压强增大 D.保持压强不变,充入N2,使容器的体积变大
难度: 简单查看答案及解析
-
少量铁粉与100 mL 0.01 mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl固体 ⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发) ⑧改用10 mL 0.1 mol/L盐酸
A.①⑥⑦ B.③⑤⑦⑧ C.③⑦⑧ D.③⑥⑦⑧
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
B.有气体参加的化学反应,若増大压强(即缩小反应容器的体积),可増加活化分子的百分数,从而使反应速率增大
C.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
难度: 中等查看答案及解析
-
有a、b、c、d四种金属.将a与b用导线接起来,浸入电解质溶液中,a不易腐蚀.将b、d分别投入等浓度的盐酸中,d比b反应强烈.将铜浸入a的盐溶液里,无明显变化.如果把铜浸入c的盐溶液里,有金属c析出.据此判断它们的活动性顺序由强到弱的为
A.a>c>d>b B.d>a>b>c C.d>b>a>c D.b>a>d>c
难度: 中等查看答案及解析
-
将反应 Cu(s)+2Ag+(aq) == Cu2+(aq)+2Ag(s)设计成如图所示原电池。下列说法中正确的是( )
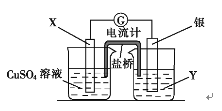
A.电极X是正极,其电极反应为Cu-2e-== Cu2+
B.银电极板质量逐渐减小,Y溶液中c(Ag+)增大
C.当X电极质量变化0.64 g时,Y溶液质量变化2.16 g
D.外电路中电流由银极流向铜极
难度: 中等查看答案及解析
-
下列反应属于放热反应的是( )
A.氢氧化钡晶体和氯化铵晶体的反应
B.生成物总能量低于反应物总能量的反应
C.化学键断裂吸收的热量比化学键生成放出的热量多的反应
D.不需要加热就能发生的反应
难度: 简单查看答案及解析
-
已知:物质的能量越低越稳定,白磷转化为红磷是放热的,据此下列说法中正确的是( )
A.白磷转化为红磷是物理变化
B.在相同条件下红磷比白磷稳定
C.相同条件下,红磷所具有的总能量比白磷的高
D.相同质量的红磷和白磷完全燃烧放出的能量相等
难度: 中等查看答案及解析
-
下列反应既属于氧化还原反应,又是吸热反应的是
A.生石灰与水作用制熟石灰 B.灼热的木炭与CO2反应
C.甲烷在氧气中的燃烧反应 D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
难度: 中等查看答案及解析
-
下列说法不正确的是
A.含有共价键的化合物一定是共价化合物
B.含有离子键的化合物一定是离子化合物
C.在离子化合物中可能存在共价键
D.在共价化合物中不可能存在离子键
难度: 中等查看答案及解析
-
下列结论正确的是( )
①离子半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si ⑦金属性:Be<Mg<Ca<K
A.只有②⑤⑦ B.②⑥⑦ C.②④⑤⑥⑦ D.②④⑥
难度: 中等查看答案及解析
-
下列分子中所有原子都满足最外层为8 电子结构的是( )
A.NH3 B.PC13 C.PCl5 D.BCl3
难度: 简单查看答案及解析
-
短周期元素的离子:aW3+、bX+、cY2-、dZ-具有相同的电子层结构,下列关系中不正确的是( )
A.半径:Y2->Z->X+>W3+
B.还原性:Y2->Z-
C.氧化性:W3+> X+
D.质子数:c>d>b>a
难度: 简单查看答案及解析
-
下列关于物质性质变化的比较,不正确的是
A.稳定性:HI>HBr>HCl>HF B.原子半径大小:Na>S>O
C.碱性强弱:KOH>NaOH>LiOH D.还原性强弱:Cl﹣<Br﹣<I﹣
难度: 简单查看答案及解析
-
下列化学用语中,不正确的是( )
A.钠离子结构示意图为:
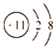 B.质子数为6,中子数为8的原子表示为:
B.质子数为6,中子数为8的原子表示为: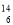 C
CC.H、D、T互为同位素 D.液态的氯气称为氯水
难度: 简单查看答案及解析
-
下列有关化学用语表示正确的是( )
A.Al3+的结构示意图:
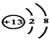 B.水的电子式:
B.水的电子式:
C.乙烯的结构简式:CH2CH2 D.含有7个中子的碳原子:
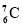
难度: 中等查看答案及解析
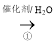 C2H5OH
C2H5OH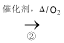 CH3CHO
CH3CHO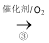 CH3COOH
CH3COOH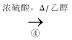 CH3COOCH2CH3
CH3COOCH2CH3