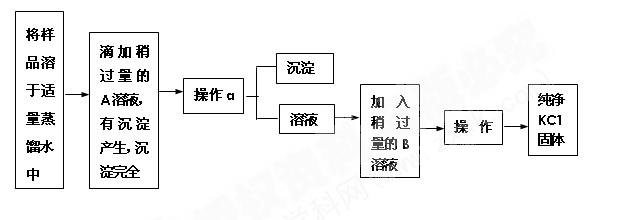
-
在反应X+2Y= R+2M 中,已知R和M的摩尔质量之比为22:9 ,当1.6g的X与Y完全反应后,生成4.4g的R,则此反应中Y和M的质量之比为( )
A. 16:9 B. 23:9 C. 1:2 D. 2:1
难度: 简单查看答案及解析
-
震惊全国的11.15上海市静安区胶州路728号一幢28层高的居民住宅发生火灾有58人丧生。当火灾发生时,你认为采取的下列措施中不恰当的是( )
A. 立即撤离火灾现场并拨打119报警
B. 若逃生通道被堵,应迅速转移到窗口边或阳台上等待救援
C. 若被困在室内,应立即封堵火、烟的进口,并站在室内最高处等待救援
D. 若被困在火灾现场,应尽可能贴近地面向火势小、烟雾少的方向撤离
难度: 简单查看答案及解析
-
下列仪器不能用酒精灯直接加热的是( )
①烧杯 ②坩埚 ③烧瓶 ④试管 ⑤锥形瓶 ⑥蒸发皿 ⑦容量瓶 ⑧表面皿
A.①③⑤⑦⑧ B.①③④⑤⑦ C.④⑦⑧ D.②③⑤⑦⑧
难度: 简单查看答案及解析
-
某学生发现滴瓶中溶液里有悬浊物,拟用右图所示操作进行过滤,错误的操作有( )
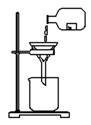
A. 4处 B. 3处
C. 2处 D. 1处
难度: 简单查看答案及解析
-
一定量的铁与足量的稀H2SO4及足量的CuO制单质铜,有人设计以下两种方案:
①Fe
H2
Cu, ②CuO
CuSO4
Cu。
若实验过程中,根据一般的实验方法和实验操作规则进行操作,则两者制得单质铜的量作比较正确的是( )
A.相等 B.②多 C.①多 D.无法判断
难度: 简单查看答案及解析
-
向某溶液中滴入BaCl2 溶液,产生白色沉淀,再滴入稀硝酸,沉淀不溶解,则该溶液中( )
A.可能有SO42-或Ag+ B. 一定有SO42- C.一定无Ag+ D.可能有CO32-
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 摩尔是国际科学界建议采用的一种物理量
B. 物质的摩尔质量等于该物质的相对分子质量
C. O22-离子的摩尔质量是32 g·mol-1
D. 1 mol H2O的质量为18 g·mol-
难度: 简单查看答案及解析
-
经测定,一瓶气体中只含有C、O两种元素,通常情况下这瓶气体不可能是( )
A. 两种单质 B. 一种单质和一种化合物的混合物
C. 两种化合物 D. 一种化合物
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 气体的摩尔体积约为22.4 mol·L-1 B. 标准状况下9gH2O体积约为11.2L
C. 在100 mL水中溶解5.85 g NaCl,则所得NaCl溶液的物质的量浓度为1 mol·L-1
D. 同温同压下,相同体积的任何气体所含物质分子的物质的量一定相同
难度: 简单查看答案及解析
-
按照物质的交叉分类法判断,H2SO4属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤二元酸 ⑥化合物 ⑦混合物
A. ①②③④⑤⑥ B. ①④⑤⑥ C. ①②③④ D. ①④⑤⑦
难度: 简单查看答案及解析
-
下列现象与胶体的性质无关的是( )
A. 将盐卤或石膏加入豆浆,制成豆腐
B. 一枝钢笔使用两种不同型号的蓝黑墨水,易出现堵塞
C. 向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀
D. 清晨,人们经常看到的阳光穿过茂密的树木枝叶所产生的美丽景象
难度: 简单查看答案及解析
-
下列电离方程式正确的是( )
A. CuSO4===Cu+2+SO4-2 B. NH4NO3===NH4++NO3-
C. Na2CO3===Na2++CO32- D. KClO3===K++Cl-+3O2-
难度: 简单查看答案及解析
-
下列化学方程式中,不能用H++OH-=H2O表示的是
A.KOH + HCl = KCl + H2O B.Ba(OH)2 + 2HCl = BaCl2 + 2H2O
C.2NaOH + H2SO4 = Na2SO4 + 2H2O D.Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
难度: 简单查看答案及解析
-
下列离子方程式的书写正确的是( )
A. 铜和稀硫酸反应:Cu+2H+=Cu2++H2↑
B. NaHCO3溶液与HCl溶液反应:H++HCO3-=CO2↑+H2O
C. 铝和硫酸铜溶液的反应Al+Cu2+=Al3++Cu
D. 氯化铁滴入沸水中生成氢氧化铁胶体Fe3++3H2O=Fe(OH)3↓+3H+
难度: 简单查看答案及解析
-
下列各组离子,在水溶液中能大量共存的是( )
A. K+、Ag+、NO3-、Cl- B. NH4+、Ba2+、Cl-、CO32-
C. H+、Ca2+、CO32-、NO3- D. Na+、Al3+、SO42-、NO3-
难度: 简单查看答案及解析
-
下列反应不属于氧化还原反应的是
A. 3Cl2+6KOH====5KCl+KClO3+3H2O B. 2NO2+2NaOH====NaNO3+NaNO2+H2O
C. Fe2O3+2Al
2Fe+Al2O3 D. SnCl4+2H2O===SnO2+4HCl
难度: 简单查看答案及解析
-
下列物质的水溶液能够导电,但属于非电解质的是( )
A. 二氧化硫 B. 碳酸氢铵 C.醋酸 D. 氯气
难度: 简单查看答案及解析
-
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/ml),所得溶液的密度为p g/ml,质量分数为W,物质的量浓度为c mol/L,则下列关系中不正确的是( )
A.
B.
C.
D. C=1000Vρ/(17V+22400)
难度: 简单查看答案及解析
-
在下列给定条件的溶液中,可能大量共存的离子组是( )
A.无色溶液:Cu2+、、H+、Cl-、NO3-
B.能使酚酞试液呈红色的溶液:Na+、K+、Cl-、CO32-
C.能与金属Fe反应放出H2的溶液中:Na+、Cl-、SO42-、NO3-
D.含有HCO
的溶液中:K+、OH-、NO
、Ba2+
难度: 简单查看答案及解析
-
设NA代表阿伏加德罗常数,下列说法正确的是( )
A. 0.1 mol金属钠变为钠离子时失去的电子数为NA
B. 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA
C. 0.1mol/L的MgCl2溶液中,含有Mg2+数目为0.1NA
D. 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3 NA
难度: 简单查看答案及解析
-
浓度均为0.1mol·L-1的三种溶液等体积混合,充分反应后没有沉淀的一组溶液是( )
A.BaCl2 NaOH NaHCO3 B.NaHCO3 CaCl2 HCl
C.AlCl3 MgCl2 NaOH D.Ba(OH)2 CaCl2 H2SO4
难度: 简单查看答案及解析