-
能正确表示下列化学反应的离子方程式的是
A. 氢氧化钡溶液与硫酸的反应:OH-+H+===H2O
B. 澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+===Ca2++2H2O
C. 铜片插入硝酸银溶液中:Cu+Ag+===Cu2++Ag
D. 碳酸钙溶于稀盐酸中:CaCO3+2H+="==" Ca2++H2O+CO2↑
难度: 中等查看答案及解析
-
下列实验操作中错误的是( )
A. 蒸发操作时,不能使混合物中的水分完全蒸干后才停止加热
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来
难度: 中等查看答案及解析
-
(3分)下列有关实验的叙述中,正确的是( )
A. 容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液
B. 用分液的方法分离水和酒精的混合物
C. 配制1L0.1mol/L的NaCl溶液时可用托盘天平称量5.85gNaCl固体
D. 用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁
难度: 中等查看答案及解析
-
将30 mL 0.5 mol·L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
A. 0.3 mol·L-1 B. 0.03 mol·L-1 C. 0.05 mol·L-1 D. 0.04 mol·L-1
难度: 简单查看答案及解析
-
一定条件下氨气和氧化铜可以发生如下反应:2NH3+3CuO △ 3Cu+N2+3H2O,对此反应的分析合理的是
A.该反应属置换反应
B.NH3被氧化为N2
C.反应体现了金属铜的还原性
D.每生成1mol H2O 就伴随着1mol电子转移
难度: 中等查看答案及解析
-
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
A. 950mL,11.2g B. 500mL,117g
C. 1000mL,117.0g D. 任意规格,111.2g
难度: 简单查看答案及解析
-
工业焊接钢管时常用
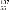 Cs进行“无损探伤”,这里的“137”是指该原子的( )
Cs进行“无损探伤”,这里的“137”是指该原子的( )A. 质子数 B. 中子数
C. 电子数 D. 质量数
难度: 简单查看答案及解析
-
下列各组微粒:①H3O+、NH、Na+;②OH-、NH、F-;③O2-、Na+、Mg2+;④CH4、NH3、H2O,具有相同质子数和电子数的是( )
A. ①②③ B. ①②④
C. ②③④ D. ①③④
难度: 简单查看答案及解析
-
2g NaOH固体溶于水配成250mL溶液,取出其中的50mL,该50mLNaOH溶液的物质的量浓度为( )
A.0.04 mol/L B.0.2 mol/L C.1 mol/L D.2 mol/L
难度: 中等查看答案及解析
-
下列离子的检验方法正确的是( )
A. 某溶液
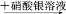 产生白色沉淀,说明原溶液中有Cl-
产生白色沉淀,说明原溶液中有Cl-B. 某溶液
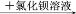 产生白色沉淀,说明原溶液中有SO
产生白色沉淀,说明原溶液中有SO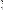
C. 某溶液
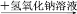 产生蓝色沉淀,说明原溶液中有Cu2+
产生蓝色沉淀,说明原溶液中有Cu2+D. 某溶液
 生成无色气体,说明原溶液中有CO
生成无色气体,说明原溶液中有CO
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 同位素
 、
、 具有相同的质量数
具有相同的质量数B.
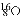 与
与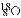 互称为核素
互称为核素C. 氟的元素符号为
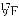
D. 10B的中子数和核外电子数相同
难度: 简单查看答案及解析
-
下列物质中同时含有氯分子和氯离子的是( )
A. 液氯 B. 新制氯水
C. CaCl2溶液 D. 次氯酸溶液
难度: 中等查看答案及解析
-
实验室制氯气时有如下操作,操作顺序正确的是( )
①连接好装置,检查气密性;②缓缓加热;③在烧瓶中加入少量的MnO2,向分液漏斗中加入浓盐酸;④通过分液漏斗慢慢向烧瓶中注入浓盐酸;⑤将多余氯气用浓NaOH溶液吸收;⑥当有连续气泡出现时,开始用向上排空气法收集氯气。
A. ①②③④⑤⑥ B. ③④②①⑥⑤
C. ①④③②⑥⑤ D. ①③④②⑥⑤
难度: 简单查看答案及解析
-
在氯水中存在许多分子和离子,它们在不同的反应中表现各自的性质,下列的实验和结论一致且正确的是
A. 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2的存在
B. 溶液呈浅黄绿色,且有刺激性气味,说明溶液中有Cl2的存在
C. 先加入盐酸酸化,再加入AgNO3溶液产生白色沉淀,说明氯水中有Cl-的存在
D. 加入NaOH溶液,氯水浅黄绿色消失,说明溶液中有HClO分子的存在
难度: 中等查看答案及解析
-
关于氧化还原反应的说法中正确的是( )
A. 失去电子的物质是氧化剂
B. 氧化反应的本质是得电子
C. 原子得到电子后,元素的化合价一定升高
D. 有单质参加或生成的反应不一定是氧化还原反应
难度: 简单查看答案及解析
-
下列化学反应中电子转移的表示方法不正确的是( )
A.
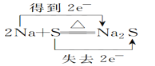 B.
B. 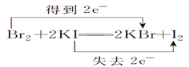
C.
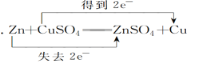 D.
D. 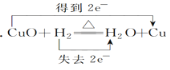
难度: 简单查看答案及解析
-
在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
A. Zn2+、Al3+、SO42-、Cl- B. Ag+、Na+、NO3-、Cl-
C. Fe3+、K+、Cl-、MnO4- D. Ba2+、NH4+、Cl-、HCO3-
难度: 中等查看答案及解析
-
从溴化钠中制取单质溴可采用的方法是( )
A. 蒸发至干,灼烧固体
B. 滴入新制的氯水,用汽油萃取
C. 通入新制的氯气,用酒精萃取
D. 加入碘水,用四氯化碳萃取
难度: 简单查看答案及解析
-
下列关于钠的叙述中,正确的是( )
A. 钠在自然界中存在游离态
B. 钠是一种灰色的固体
C. 钠可以保存在煤油或CCl4中
D. 钠着火时可以用沙土扑灭
难度: 简单查看答案及解析
-
下列有关Na2CO3和NaHCO3性质比较中,正确的是
A. 热稳定性:Na2CO3<NaHCO3
B. 常温时水溶液中的溶解度:Na2CO3<NaHCO3
C. 与稀盐酸反应快慢:Na2CO3<NaHCO3
D. 物质的量相同时,消耗盐酸:Na2CO3<NaHCO3
难度: 中等查看答案及解析
 Rn),对人体产生伤害。请回答:
Rn),对人体产生伤害。请回答:
 Rn,故将
Rn,故将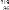 Rn,故将
Rn,故将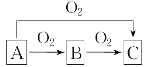
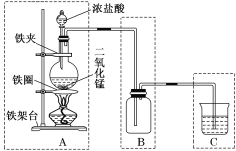
 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。