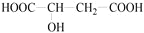-
“保护环境,就是保护人类自己”。下列环境问题与其产生的主要原因不相符有几个?( )
①“光化学烟雾”主要是由NOx等引起的
②“白色污染”主要是由聚乙烯塑料等引起的
③“温室效应”主要是由空气中CO2浓度增大引起的
④“臭氧空洞”主要是大量使用氟氯代烃等引起的
⑤“赤潮”主要是由水体中P、N等元素过量引起的
⑥“酸雨”主要是由空气中SO2、NOx、CO2浓度增大引起的
⑦“PM2.5”主要由化石燃料的燃烧(如机动车尾气、燃煤)等引起的
A.0个 B.1个 C.2个 D.3个
难度: 简单查看答案及解析
-
下列表述正确的有( )
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅
②化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐
③提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料
④有机玻璃的主要成分是硅酸盐
⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能
A.1个 B.2个 C.3个 D.4个
难度: 简单查看答案及解析
-
下列有关说法正确的是( )
A.高纤维食物是富含膳食纤维的食物,在人体内都可以通过水解反应提供能量
B.“熔喷布”可用于制作N95型等口罩,生产“熔喷布”的主要原料是聚丙烯,它属于纯净物
C.喝补铁剂(含Fe2+)时,加服维生素C效果更好,因维生素C具有还原性
D.“嘉州峨眉山有燕萨石,形六棱而锐首,色莹白明澈。”燕萨石的主要成分是硅酸盐
难度: 简单查看答案及解析
-
下列说法中不正确的有( )
①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质;
②氨溶于水得到的溶液能导电,所以NH3是电解质;
③液态HCl不导电,所以属于非电解质;
④NaHSO4在水溶液中电离时生成的阳离子有氢离子,但不属于酸;
⑤电解质放在水中一定能导电,非电解质放在水中一定不导电;
⑥强电解质的导电能力比弱电解质强;
⑦物质可根据在水中或熔化状态下的导电性分为电解质与非电解质。
A.4个 B.5个 C.6个 D.全部
难度: 简单查看答案及解析
-
下列说法错误的是( )
A.制取环氧乙烷:CH2=CH2+Cl2+Ca(OH)2→
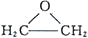 +CaCl2+H2O,原子利用率为53.8%
+CaCl2+H2O,原子利用率为53.8%B.煤在气化过程中脱硫可以减少污染
C.食品添加剂加入到食品中目的是防腐、保鲜等
D.锂电池应用广泛的主要原因是比能量高、可储存时间长
难度: 简单查看答案及解析
-
某小组同学配制480mL0.2mol/L的NaCl溶液,下列说法正确的是( )
A.选用500mL的容量瓶,且容量瓶必需干燥
B.用托盘天平准确称量5.85gNaCl固体
C.定容时俯视容量瓶的刻度线,会使实验结果偏高
D.定容摇匀后发现液面低于刻度线,应再加蒸馏水至刻度线
难度: 简单查看答案及解析
-
在Fe2(SO4)3溶液中,加入a g铜,完全溶解后,再加入b g铁,充分反应后得到cg残余固体,已知a>c,则下列说法正确的是( )
A.最后得到的溶液一定含有Cu2+
B.残余固体是铜和铁
C.将残余固体加入稀硫酸中一定有气泡产生
D.最后得到的溶液中可能含有Fe3+
难度: 中等查看答案及解析
-
下列有关Fe2(SO4)3溶液的叙述正确的是( )
A.该溶液中K+、Fe2+、SCN-、Br-可以大量共存
B.和H2S反应的离子方程式:2Fe3++H2S==FeS+2H+
C.和Ba(OH)2溶液反应的离子方程式:Fe3++
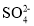 +Ba2++3OH-==Fe(OH)3↓+BaSO4↓
+Ba2++3OH-==Fe(OH)3↓+BaSO4↓D.1L 0.1mol·L-1该溶液和足量的Zn充分反应,生成11.2gFe
难度: 中等查看答案及解析
-
探究硫及其化合物的性质,下列说法正确是( )
A.SO2能杀菌消毒防腐,可以做食品添加剂
B.用pH试纸测量浓硫酸的pH
C.将H2S气体通入CuSO4溶液生成CuS沉淀,说明H2S为强电解质
D.FeSO4保存在棕色试剂瓶中,并加入少量Cu粉防止氧化
难度: 简单查看答案及解析
-
化学与生活息息相关。下表中有关物质用途与原因解释不正确的是( )
选项
现象或事实
解释
A.
肉制品中添加适量的亚硝酸钠
亚硝酸钠有防腐的作用
B.
甘油护肤保湿
甘油沸点高且能与水分子之间形成氢键
C.
硅是信息高速公路的骨架
硅具有良好的传递光信号的性能
D.
Al(OH)3用作塑料的阻燃剂
Al(OH)3受热分解吸收大量的热,且能起阻隔作用
A.A B.B C.C D.D
难度: 简单查看答案及解析
-
分子式为C3H6BrCl的有机物共有(不含立体异构)( )
A.4种 B.5种 C.6种 D.7种
难度: 简单查看答案及解析
-
以反应
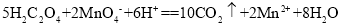 为例探究“外界条件对化学反应速率的影响"。实验时,分别量取
为例探究“外界条件对化学反应速率的影响"。实验时,分别量取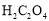 溶液和酸性
溶液和酸性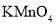 溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。
溶液,迅速混合并开始计时,通过测定溶液褪色所需时间来判断反应的快慢。编号
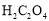 溶液
溶液酸性
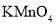 溶液
溶液温度/℃
浓度
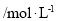
体积
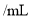
浓度
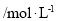
体积
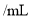
①
0.10
2.0
0.01
4.0
25
②
0.20
2.0
0.01
4.0
25
③
0.20
2.0
0.01
4.0
50
下列说法不正确的是( )
A.实验①、②、③所加的
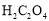 溶液均要过量
溶液均要过量B.实验①测得
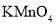 溶液的褪色时间为40 s,则这段时间内平均反应速率
溶液的褪色时间为40 s,则这段时间内平均反应速率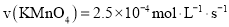
C.实验①和②探究浓度对反应速率的影响,实验②、③探究温度对反应速率的影响
D.3组实验中均发现起初反应较慢,过了一会儿速率突然增大,可能是生成的
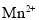 对反应起催化作用
对反应起催化作用难度: 中等查看答案及解析
-
T℃时,向1L固定容积的密闭容器中加入2molX和1molY,发生反应:2X(g)+Y(g)
 aZ(g)+W(g) ΔH=-QkJ/mol(Q>0)。当反应达到平衡状态后,放出的热量为Q1kJ;若平衡后再升高温度,混合气体的平均相对分子质量减小。下列说法正确的是( )
aZ(g)+W(g) ΔH=-QkJ/mol(Q>0)。当反应达到平衡状态后,放出的热量为Q1kJ;若平衡后再升高温度,混合气体的平均相对分子质量减小。下列说法正确的是( )A.a=3
B.T℃达到平衡状态时,X的转化率为
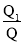
C.达到平衡状态后向容器中加入一定量的氦气,正逆反应速率均增大
D.当容器内气体的密度一定时表明反应已达到平衡状态
难度: 中等查看答案及解析
-
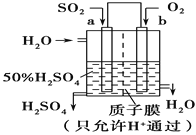
H2S是一种剧毒气体,如图为质子膜H2S燃料电池的示意图,可对H2S废气资源化利用。下列叙述错误的是
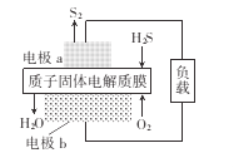
A.a是负极,电池工作时,电子的流动方向是:电极a-负载一电极b-质子膜一电极a
B.电池工作时,化学能转化为电能和热能
C.电极b上发生的电极反应式为O2+ 4e-+4H+ = 2H2O
D.当电路中通过4 mol电子时,有4 molH+经质子膜进入正极区
难度: 中等查看答案及解析
-
下列对相应有机物的描述完全正确的是( )
①甲烷:与氯气在光照条件下反应生成的CH2Cl2有两种结构
②乙烯:可发生加成反应和加聚反应,其产量可以用来衡量一个国家石油化工发展水平
③苯:12个原子共平面,1mol苯中含有3mol碳碳双键
④乙醇:常温下具有特殊香味的液体,常用作调味品,也可以用来杀菌消毒
⑤油脂:属于酯类,在碱性条件下发生水解反应生成甘油和高级脂肪酸,称为皂化反应
⑥蔗糖:糖尿病人尿液的成分之一,可以用新制Cu(OH)2检验
⑦蛋白质:水解的最终产物为氨基酸,部分蛋白质遇浓硝酸显黄色
A.②④⑤⑦ B.②④⑦ C.①②③⑤⑥⑦ D.②④⑤⑥⑦
难度: 中等查看答案及解析
-
有镁、铝、铁、铜四种金属,若两两混合,取混合物26克与足量稀硫酸反应,若产生标况下氢气11.2L,此混合物的可能组合方式最多有()
A.5种 B.4种 C.3种 D.2种
难度: 中等查看答案及解析
-
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应生成另外两种气体,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
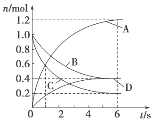
A.该反应的化学方程式为3B(g)+4D(g)
 6A(g)+2C(g)
6A(g)+2C(g)B.反应进行到1s时,v(A)=v(D)
C.反应进行到6s时,B的平均反应速率为0.05mol/(L·s)
D.反应进行到6s时,各物质的反应速率相等
难度: 中等查看答案及解析
-
氨基甲酸铵分解反应为NH2COONH4(s)
 2NH3(g)+CO2(g),在一体积恒定的容器里,发生上面的反应,可以判断该反应已经达到平衡的是
2NH3(g)+CO2(g),在一体积恒定的容器里,发生上面的反应,可以判断该反应已经达到平衡的是A.密闭容器中氨气的体积分数不变
B.1 mol NH2COONH4分解同时有17g NH3消耗
C.密闭容器中混合气体的密度不变
D.混合气体的平均分子量不变
难度: 简单查看答案及解析
-
已知:2H2(g)+O2(g)═2H2O(g)△H1
3H2(g)+Fe2O3(s)═2Fe(s)+3H2O(g)△H2
2Fe(s)+
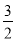 O2(g)═Fe2O3(s)△H3
O2(g)═Fe2O3(s)△H32Al(s)+
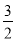 O2(g)═Al2O3(s)△H4
O2(g)═Al2O3(s)△H42Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
A.△H1<0,△H3>0 B.△H5<0,△H4<△H3
C.△H1=△H2+△H3 D.△H3=△H4+△H5
难度: 简单查看答案及解析
-
下列说法不正确的是( )
①
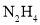 分子中既含极性键又含非极性键
分子中既含极性键又含非极性键②若
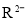 和
和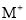 的电子层结构相同,则原子序数:
的电子层结构相同,则原子序数: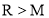
③
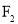 、
、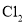 、
、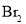 、
、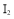 熔点随相对分子质量的增大而升高
熔点随相对分子质量的增大而升高④
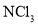 、
、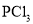 、
、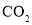 、
、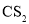 分子中各原子均达到
分子中各原子均达到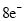 稳定结构
稳定结构⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥
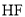 分子很稳定是由于
分子很稳定是由于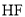 分子之间能形成氢键
分子之间能形成氢键⑦由于非金属性:
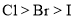 ,所以酸性:
,所以酸性: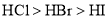
A.②⑤⑥⑦ B.①③④⑤ C.②④⑤ D.③⑤⑦
难度: 中等查看答案及解析
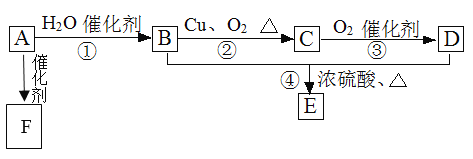
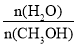 对甲醇水蒸气重整制氢的好处是___。
对甲醇水蒸气重整制氢的好处是___。