-
下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
A.地下钢管连接镁块
B.金属护栏表面涂漆
C.汽车底盘喷涂高分子膜
D.水中的钢闸门连接电源的负极
难度: 中等查看答案及解析
-
下列设备工作时,可以实现化学能转化为电能的是( )
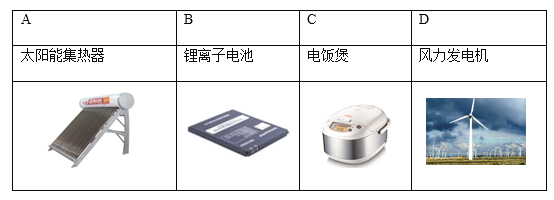
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
下列物质中,属于弱电解质的是( )
A.HCl B.NH4Cl C.KOH D.CH3COOH
难度: 简单查看答案及解析
-
下列溶液一定呈中性的是
A.c(H+) = c(OH–) B.pH=7 C.KW=10-14 D.c(H+) =10-7mol/L
难度: 中等查看答案及解析
-
在2A(g)+B(g)
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A.υ(A)= 0.5 mol/(L·s) B.υ(D)= 1 mol/(L·s)
C.υ(C)= 0.8 mol/(L·s) D.υ(B)= 0.3 mol/(L·s)
难度: 中等查看答案及解析
-
在中和热测定的实验中不需要用到的仪器是:
A. 天平 B. 温度计 C. 环形玻璃搅拌棒 D. 量筒
难度: 简单查看答案及解析
-
准确量取25.00mL高锰酸钾溶液,可选用的仪器是( )
A.50mL量筒 B.50mL烧杯
C.50mL酸式滴定管 D.50mL碱式滴定管
难度: 简单查看答案及解析
-
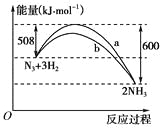
已知在1×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A.2H2(g)+O2(g)===2H2O(g) ΔH=+484 kJ·mol-1
B.H2O(g)===H2(g)+1/2O2(g) ΔH=+242 kJ·mol-1
C.H2(g)+1/2O2(g)===H2O(g) ΔH=+242 kJ·mol-1
D.2H2(g)+O2(g)===2H2O(l) ΔH=-484 kJ·mol-1
难度: 简单查看答案及解析
-
对已达平衡状态的反应:2X(g)+Y(g)
2Z(g),减小压强时,下列说法正确的是( )
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都增大,平衡向正反应方向移动
D.正、逆反应速率都减小,平衡向逆反应方向移动
难度: 简单查看答案及解析
-
体积相同、pH相同的盐酸和醋酸,与碱中和时消耗碱的量( )
A.相同 B.盐酸多 C.醋酸多 D.无法确定
难度: 简单查看答案及解析
-
关于0.1moL/L氯化铁溶液的说法正确的是( )
A.溶液显碱性
B.加少量浓盐酸能促进FeCl3水解
C.适当升高温度能促进FeCl3水解
D.加少量NaCl固体能促进FeCl3水解
难度: 中等查看答案及解析
-
某酸性燃料电池酒精检测仪原理如图所示。下列说法中正确的是( )

A.正极上发生的反应是:O2+4e-+2H2O===4OH-
B.负极上发生的反应是:CH3CH2OH-4e-+H2O ===CH3COOH+4H+
C.检测时,电解质溶液中的H+向负极移动
D.若有0.4 mol电子转移,则消耗标准状况下4.48 LO2
难度: 困难查看答案及解析
-
物质的浓度相同的三种盐,NaX、NaY、NaZ的溶液,其pH依次为9、9.5、10,则HX、HY、HZ 酸性由强到弱的顺序是( )
A.HX>HZ>HY B.HZ>HY>HX C.HX>HY>HZ D.HY>HZ>HX
难度: 中等查看答案及解析
-
关于化学平衡常数K的叙述正确的是( )
A.对任一可逆反应,K越大,表示反应物的转化率越大
B.对任一可逆反应,温度升高,则K值增大。
C.K越大,表示化学反应速率越大
D.加入催化剂或增大反应物的浓度时,K值就增大
难度: 中等查看答案及解析
-
已知在Ca3(PO4)2的饱和溶液中,c(Ca2+)=2.0×10-6mol•L-1,c(PO43-)=1.58×10-6mol•L-1,则Ca3(PO4)2的Ksp为( )
A.2.0×10-29 B.3.2×10-12 C.6.3×10-18 D.5.1×10-27
难度: 中等查看答案及解析
-
下列过程或现象与盐类水解无关的是( )
A.纯碱溶液去油污 B.铁在潮湿的环境下生锈
C.加热氯化铁溶液颜色变深 D.浓硫化钠溶液有臭味
难度: 简单查看答案及解析
-
氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结也可制取Cu2O。已知反应:
①2Cu(s) + O2(g) = 2CuO(s) ΔH = −314 kJ/mol
②2Cu2O(s) + O2(g) = 4CuO(s) ΔH = −292 kJ/mol
则反应CuO(s) 与Cu(s) 反应生成Cu2O(s) 的热化学方程式是( )
A.CuO(s) + Cu(s) = Cu2O(s) ΔH = −22 kJ/mol
B.CuO(s) + Cu(s) = Cu2O(s) ΔH = +22 kJ/mol
C.CuO(s) + Cu(s) = Cu2O(s) ΔH = −11 kJ/mol
D.CuO(s) + Cu(s) = Cu2O(s) ΔH = +11 kJ/mol
难度: 中等查看答案及解析
-
一定条件下发生下列反应,其中属于盐类水解反应的是( )
A.CH3COO—+H2O
CH3COOH+OH—
B.Cl2+H2O
H++Cl-+HClO
C.CH3COOH+NaOH
CH3COONa+H2O
D.HCO3—+H2O
H3O++CO32-
难度: 中等查看答案及解析
-
用滴有酚酞和氯化钠溶液的湿润滤纸分别做甲、乙两个实验,下列判断不正确的是( )

A.b极附近有气泡冒出 B.d极附近出现红色
C.a、c极上都发生氧化反应 D.甲中铁棒比乙中铁棒更易腐蚀
难度: 困难查看答案及解析
-
常温下,某正盐的溶液中,该溶液pH为9,则由水电离出的H+的浓度为( )
A.10ˉ9mol/L B.10ˉ5mol/L
C.10ˉ5mol/L或10ˉ9mol/L D.10ˉ5mol/L和10ˉ9mol/L
难度: 中等查看答案及解析