-
下列叙述,从化学角度分析不正确的是: ( )
A.在煤炭中加入生石灰可以减少SO2的排放,减少酸雨的发生
B.氟利昂(CCl2F2)或 NOx都可以破坏臭氧层,从而导致温室效应
C.食用植物油的主要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质
D.茂密树林中的道道光柱,既是一种自然现象又是光学现象,也与胶体知识有关
难度: 简单查看答案及解析
-
正确掌握化学用语是学好化学的基础。下列化学用语中正确的是 ( )
A.乙烯的结构简式为CH2CH2 B.果糖的实验式(最简式)为C6H12O6
C.氯化铯的晶体结构(晶胞)模型
D.NH4Cl的电子式为

难度: 简单查看答案及解析
-
下列图像能正确地表达可逆反应3A(g)+B(g)
2C(g)(△H <0)的是 ( )

难度: 简单查看答案及解析
-
某无色溶液,由Na+、Ba2+、Al3+、AlO2-、Fe3+、CO32-、SO42-中的若干种组成。取适量该溶液进行如下实验: ( )
①加入过量盐酸,有气体生成;
②在①所得的溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;
③在②所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。则原溶液中一定存在的离子是
A.Na+、AlO2-、CO32- B.Al3+、Fe3+、SO42-
C.Na+、AlO2-、SO42-、CO32- D.Na+、Ba2+、AlO2-
难度: 简单查看答案及解析
-
下列有关溶液的说法正确的是 ( )
A.10mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20mL
B.pH相等的CH3COONa、NaClO、Na2CO3三种溶液: c(Na2CO3) >c(CH3COONa) >c(NaClO)
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) +2c(OH-)=2c(H+) + c(CH3COOH)
D.0.1mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
难度: 简单查看答案及解析
-
下列曲线图(纵坐标为沉淀的量,横坐标为加入物的量)与对应选项不正确的是( )
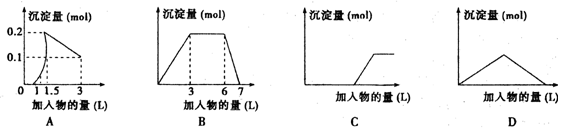
A.向1L浓度均为0.1mol/L的Ba(OH)2、NaAlO2混合液中加入0.1 mol/L稀H2SO4溶液
B.向含有0.1 mol/L AlCl3和0.3mol/L NH4Cl的1L混合液中加入0.1mol/LNaOH溶液
C.向烧碱溶液中滴加明矾溶液
D.向Ba(OH)2溶液中逐渐通入二氧化碳
难度: 简单查看答案及解析
-
已知外电路中,电子由铜流向a极。有关下图所示的装置分析合理的一项是 ( )

A.该装置中Cu极为正极
B.当铜极的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为2.24L
C.b极反应的电极反应式为:H2-2e-=2H+
D.一段时间后锌片质量减少
难度: 简单查看答案及解析
-
amolFeS与bmolFe3O4投入到VL cmol/L的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为 ( )
A.(a+3b)mol B.
C.
D.(cV-3a-9b)mol
难度: 简单查看答案及解析
 已知:常温下,CO能使一些化合物中的金属离子还原。
已知:常温下,CO能使一些化合物中的金属离子还原。


 ,聚丙交酯经抽丝可制成手术缝合线,在人体内可自动缓慢降解为W。聚丙交酯在体内降解的化学方程式是________。
,聚丙交酯经抽丝可制成手术缝合线,在人体内可自动缓慢降解为W。聚丙交酯在体内降解的化学方程式是________。