-
下列过程中所发生的化学变化属于取代反应的是( )
①光照射甲烷与氯气的混合气体
②乙烯通入溴水中
③在镍作催化剂的条件下,苯与氢气反应
④苯与液溴混合后撒入铁粉
A.①② B.①③ C.②④ D.①④
难度: 简单查看答案及解析
-
既可以用来鉴别甲烷和乙烯,又可以用来除去甲烷中混有的少量乙烯的操作方法是( )
A.混合气通过盛酸性高锰酸钾溶液的洗气瓶
B.混合气通过盛足量溴水的洗气瓶
C.混合气通过盛蒸馏水的洗气瓶
D.混合气跟适量氯化氢混合
难度: 简单查看答案及解析
-
由乙烯推测丙烯(CH2=CH—CH3)的结构或性质正确的是
A.不能使酸性高锰酸钾溶液褪色
B.不能在空气中燃烧
C.能使溴水褪色
D.与HCl在一定条件下能加成只得到一种产物
难度: 中等查看答案及解析
-
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)
A. 6种 B. 7种 C. 8种 D. 9种
难度: 中等查看答案及解析
-
下列对有机物结构或性质的描述中错误的是( )
A.将溴水加入苯中,溴水的颜色变浅,这是由于发生了加成反应
B.苯分子中的6个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键
C.乙烷和丙烯的物质的量共1mol,完全燃烧生成3molH2O
D.一定条件下,乙烯可以发生加聚反应,生成一种高分子物质
难度: 中等查看答案及解析
-
交警对驾驶员是否饮酒进行检测的原理是橙色的酸性K2Cr2O7水溶液遇呼出的乙醇蒸气迅速变蓝,生成蓝绿色的Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低,易挥发 ②乙醇密度比水小 ③乙醇具有还原性 ④乙醇是烃的含氧衍生物 ⑤乙醇可与羧酸在浓硫酸的作用下发生取代反应
A.②⑤ B.②③ C.①③ D.①④
难度: 简单查看答案及解析
-
某有机物的结构如图所示,下列各项性质中,它可能具有的是( )

①能发生取代反应 ②能使酸性高锰酸钾溶液褪色 ③能跟NaOH溶液反应 ④能发生酯化反应 ⑤能发生聚合反应
A.①③④ B.①②③④ C.①②③④⑤ D.①②③
难度: 中等查看答案及解析
-
某课外兴趣小组欲在实验室里制备少量乙酸乙酯,该小组的同学设计了以下四个制取乙酸乙酯的装置,其中正确的是 ( )
A.
 B.
B. 
C.
 D.
D. 
难度: 中等查看答案及解析
-
将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )
A.c(H+) B.Ka(HF) C.c(HF) D.n(H+)
难度: 简单查看答案及解析
-
稀氨水中存在着下列平衡:NH3·H2O⇌NH4++OH-,若要使平衡向逆反应方向移动,应加入的物质或采取的措施是( )
A.NH4Cl固体 B.硫酸 C.水 D.加热
难度: 简单查看答案及解析
-
下列物质中对水电离无影响的是( )
A.NaCl B.NaHCO3 C.FeCl3 D.H2SO4
难度: 简单查看答案及解析
-
室温下,0.01mol·L-1的NaOH溶液中由水电离生成的H+浓度( )
A.0.01mol·L-1 B.1×10-7mol·L-1 C.1×10-12mol·L-1 D.1×10-14mol·L-1
难度: 简单查看答案及解析
-
相同温度、相同浓度的下列溶液,其pH由小到大的顺序排列正确的是( )
A.NH4Cl (NH4)2SO4 CH3COONa NaHCO3 NaOH
B.(NH4)2SO4 NH4Cl CH3COONa NaHCO3 NaOH
C.(NH4)2SO4 NH4Cl NaOH CH3COONa NaHCO3
D.CH3COOH NH4Cl (NH4)2SO4 NaHCO3 NaOH
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.为了增加肥效,可将草木灰与铵态氮肥混合使用
B.配制氯化铁溶液时,将氯化铁固体直接溶于蒸馏水中即可
C.可用碳酸钠溶液和氯化钙溶液做泡沫灭火剂
D.可以用热的碳酸钠溶液洗涤油污
难度: 简单查看答案及解析
-
将氯化铝溶液加热蒸干并灼烧,最终得到的固体物质是( )
A.AlCl3 B.Al C.Al2O3 D.Al(OH)3
难度: 简单查看答案及解析
-
pH=2的盐酸和pH=1的盐酸,溶液中c(H+)之比为( )
A.2:1 B.1:2 C.10:1 D.1:10
难度: 简单查看答案及解析
-
已知25℃时有关弱酸的电离平衡常数K1(H2Y)>K(HX)>K2(H2Y),则物质的量浓度相同时,各溶液的pH关系为( )
A.pH(Na2Y)>pH(NaX)>pH(NaHY) B.pH(Na2Y)<pH(NaX)<pH(NaHY)
C.pH(Na2Y)>pH(NaHY)>pH(NaX) D.pH(Na2Y)<pH(NaHY)<pH(NaX)
难度: 简单查看答案及解析
-
常温下,下列有关电解质溶液的叙述正确的是( )
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH一定等于7
B.将10mLpH=11的NaOH溶液与100mL pH=11的氨水混合后,溶液的pH为11
C.将pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合,混合后溶液的pH约为10.7
D.pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性
难度: 中等查看答案及解析
-
下列说法正确的是( )
A.硫酸氢钠溶液中,c(Na+)>c(SO42-) B.醋酸钠溶液中,c(Na+)>c(CH3COO-)
C.碳酸钠溶液中,c(HCO3-)>c(OH--) D.碳酸氢钠溶液中,c(CO32-)>c(H+)
难度: 简单查看答案及解析
-
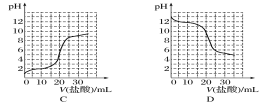
相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
A.
 B.
B.
C.
 D.
D.
难度: 简单查看答案及解析
-
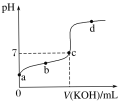
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示。据图判断正确的是

A. Ⅱ为盐酸稀释时pH值变化曲线 B. b点溶液的导电性比c点溶液的导电性强 C. a点Kw的数值比c点Kw的数值大 D. b点酸的总浓度大于a点酸的总浓度
难度: 中等查看答案及解析
-
下图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是
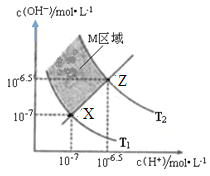
A.两条曲线间任意点均有c(H+)×c(OH-)=Kw
B.M区域内任意点均有c(H+)<c(OH-)
C.图中T1<T2
D.XZ线上任意点均有pH=7
难度: 中等查看答案及解析
-
现有室温下四种溶液,有关叙述不正确的是( )
序号
①
②
③
④
pH
11
11
3
3
溶液
氨水
氢氧化钠溶液
醋酸
盐酸
A.③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B.②③两溶液等体积混合,所得溶液显酸性
C.分别加水稀释10倍,四种溶液的pH 最大的是①
D.V1 L ④与V2 L ①混合,若混合后溶液pH=7,则V1< V2
难度: 中等查看答案及解析
-
室温下,用0.1000 mol·L-1NaOH溶液滴定20.00 mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示。下列说法正确的是( )
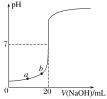
A.溶液中的氢离子浓度:a<b
B.盐酸的物质的量浓度为0.0100mol·L-1
C.指示剂变色时,说明盐酸与NaOH恰好完全反应
D.当滴加NaOH溶液10.00mL时(忽略反应前后体积变化),该混合液的pH=1+lg3
难度: 中等查看答案及解析
-
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是

A.a、c两点溶液的导电能力相同
B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-)
C.a、b、c三点溶液中水的电离程度a>b>c
D.用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc
难度: 中等查看答案及解析