-
碳元素是自然界中与人类关系最密切的元素之一,金刚石、石墨和石墨烯是碳元素常见的同素异形体。下列与碳元素相关的说法错误的是
A.金刚石是自然界中硬度最大的天然材料
B.石墨在一定条件下转化成金刚石是化学变化
C.石墨烯属于烯烃,能够发生加成反应
D.碳纤维质轻、强度大,可作为航空器材的结构材料
难度: 简单查看答案及解析
-
扭曲烷( Twistane)是一种具有挥发性的环烷烃,其结构和球棍模型如图所示。下列说法正确的是( )

A.分子式为C10H18
B.与邻二乙苯互为同分异构体
C.分子结构中含有4个六元环
D.二氯代物多于3种(不含立体异构)
难度: 困难查看答案及解析
-
下列实验方案能达到实验目的的是( )
选项
实验目的
实验方案
A
去除甲烷中少量的乙烯
气体依次通过酸性高锰酸钾溶液和浓硫酸洗气
B
去除乙酸乙酯中少量的乙酸
加入烧碱溶液洗涤、分液
C
蛋白质盐析
向硫酸铵饱和溶液中滴加几滴鸡蛋清溶液,再加入蒸馏水
D
制备无水酒精
向乙醇溶液中加入生石灰、过滤
A.A B.B C.C D.D
难度: 中等查看答案及解析
-
W、X、Y、Z是原子序数依次增大的四种短周期主族元素,X与Y位于同一主族,X与W能够形成多种化合物,其中一种为红棕色气体,Y与Z形成的一种化合物Y2Z2的分子结构模型为
 。下列叙述正确的是( )
。下列叙述正确的是( )A.X与W、Y及Z均能组合成多种化合物 B.简单离子半径:Y>Z>X>W
C.W的氧化物的水化物一定为强酸 D.化合物Y2Z2中Y不满足8电子稳定结构
难度: 简单查看答案及解析
-
已知pC=-lgc(B),室温下,某二元酸(H2A)中部分微粒的pC值随溶液pH值变化关系如图所示。下列说法错误的是( )

A.曲线a表示的微粒是H+
B.溶液中水的电离程度:m>n
C.pH=8时,溶液中,c(HA-)>c(H2A)
D.pH=1与pH=3时,H2A的浓度几乎相同
难度: 中等查看答案及解析
-
美国科学家JohnB.Goodenough荣获2019年诺贝尔化学奖,他指出固态体系锂电池是锂电池未来发展方向。Kumar等人首次研究了固态可充电、安全性能优异的锂空气电池,其结构如图所示。已知单位质量的电极材料放出电能的大小称为电池的比能量。下列说法错误的是( )
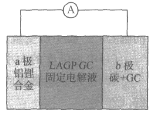
A.a极反应为“Li-e-=Li+,b极发生还原反应
B.充电时,Li+由a极通过固体电解液向b极移动
C.电路中转移4mol电子,大约需要标准状况下112L空气
D.与铅蓄电池相比,该电池的比能量大
难度: 中等查看答案及解析
-
《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠(Na2S2O8,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为NA,Ksp[Fe(OH)3]=2.7×10-39。下列叙述正确的是( )
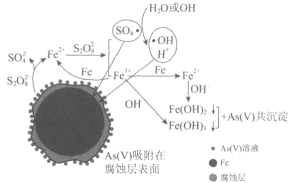
A.1mol过硫酸钠(Na2S2O8)含2NA个过氧键
B.若56gFe参加反应,共有NA个S2O82-被还原
C.室温下,中间产物Fe(OH)3溶于水所得饱和溶液中c(Fe3+)为2.7×10-18mol·L-1
D.pH越小,越有利于去除废水中的正五价砷
难度: 困难查看答案及解析


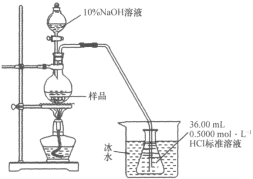
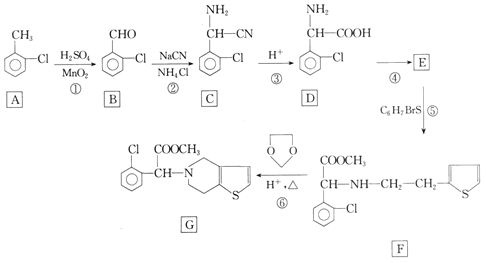
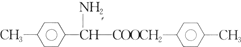 的合成路线(无机试剂任选)___。
的合成路线(无机试剂任选)___。