-
氢氧化钴[Co(OH)2]受热易分解,能与酸性溶液反应,可作涂料和清漆的干燥剂,制备方法为:①Co+2HCl=CoCl2+H2↑②CoCl2+2NaOH=Co(OH)2↓+2NaCl下列判断正确的是( )
A.钴的金属活动性比铜的弱 B.①为置换反应②为复分解反应
C.氢氧化钴的化学性质稳定 D.氢氧化钴可以干燥氯化氢气体
难度: 困难查看答案及解析
-
请用化学用语填空:
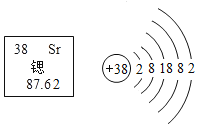
(1)钙元素_______________________。
(2)氧化铁_______________________。
难度: 简单查看答案及解析
-
请写出下列变化的化学方程式:
(1)硫在空气中燃烧:_______________________。
(2)“84消毒液”是以次氯酸钠(NaClO)为主要有效成分的消毒液,空气中的CO2溶解于NaClO溶液中,可以得到NaHCO3以及具有漂白性的HClO,请写出相关反应的化学方程式:__________。
难度: 简单查看答案及解析
-
如图是甲、乙两种固体的溶解度曲线。甲中含有少量的乙,若提纯甲应采用的结晶方法是____(填“降温结晶”或“蒸发结晶”);T2℃时,分别用甲、乙的固体配制相同质量甲、乙的饱和溶液,所需要水的质量关系为甲_________ (填“大于”“小于”或“等于”)乙。
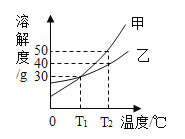
难度: 中等查看答案及解析
-
(1)增强身体免疫力,有效抗击新冠病毒,同学们在坚持体育锻炼的同时关注食品健康,请你设计一份营养均衡的午餐食谱___________(含糖类、蛋白质、维生素、油脂等)。
(2)为防止病毒飞沫传播,我们外出时会佩戴口罩,生产N95口罩的主要原料是聚丙烯,它属于_______(填“金属材料”或“合成材料”);使用过的一次性医用口罩应该如何处理?________(填字母代号)。
a.随意丢弃
b.水洗晾干后重复使用
c.放入湿垃圾桶
d.对折口罩,保持口鼻接触面朝外,扎捆成型后放人回收废弃口罩的专用垃圾桶
难度: 简单查看答案及解析
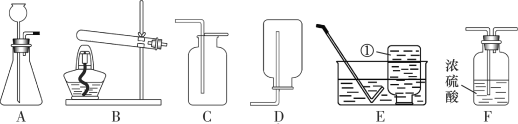
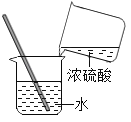 稀释浓硫酸 B.
稀释浓硫酸 B.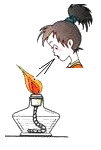 熄灭酒精灯
熄灭酒精灯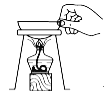 移走蒸发皿
移走蒸发皿